
【题目】用NA表示阿伏加德罗常数,下列说法正确的是
A. 1mol乙烯分子中含有共用电子对数为6NA
B. 常温常压下,32gO2、O3的混合物含有Na个氧原子
C. 标准状况下,2.24 L CH2Cl2含有的分子数等于0.1 NA
D. 7.1 g C12与足量NaOH溶液反应转移0.2×6.02×1023个电子
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】Na2CO3的制取方法及Na2CO3和NaHCO3综合实验探究
Ⅰ. (1)我国化学家侯德榜改革国外的纯碱生产工艺,其生产流程可简要表示如下:
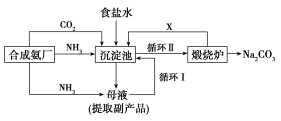
①往饱和食盐水中依次通入足量的NH3、CO2(氨碱法),而不先通CO2再通NH3的原因是_______________________________________________。
②写出沉淀池中反应的化学方程式_______________________________________________。
Ⅱ.某实验小组探究Na2CO3和NaHCO3的性质,发现实验室里盛放两种固体的试剂瓶丢失了标签。于是,他们先对固体A、B进行鉴别,再通过实验进行性质探究。
(2)分别加热固体A、B,发现固体A受热产生的气体能使澄清石灰水变浑浊。A受热分解的化学方程式为_______________________________________________。
(3)称取两种固体各2 g,分别加入两个小烧杯中,再各加10 mL蒸馏水,振荡,测量温度变化;待固体充分溶解,恢复到室温,向所得溶液中各滴入2滴酚酞溶液。
①发现Na2CO3固体完全溶解,而NaHCO3固体有剩余,由此得出结论:_______________________。
②同学们在两烧杯中还观察到以下现象。其中,盛放Na2CO3的烧杯中出现的现象是________(填字母序号)。
a.溶液温度下降
b.溶液温度升高
c.滴入酚酞后呈浅红色
d.滴入酚酞后呈红色
(4)同学们将两种固体分别配制成0.5 mol·L-1的溶液,设计如下方案并对反应现象做出预测:
实验方案 | 预测现象 | 预测依据 |
操作1:向2 mL Na2CO3溶液中滴加1 mL 0.5 mol·L-1 CaCl2溶液 | 有白色沉淀 | Na2CO3溶液中的CO浓度较大,能与CaCl2发生反应:Ca2++CO===CaCO3↓ (离子方程式) |
操作2:向2 mL NaHCO3溶液中滴加1 mL 0.5 mol·L-1 CaCl2溶液 | 无白色沉淀 | NaHCO3溶液中的CO浓度很小,不能与CaCl2反应 |
实施实验后,发现操作2的现象与预测有差异:产生白色沉淀和气体,则该条件下,NaHCO3溶液与CaCl2溶液反应的离子方程式为________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. 需要加热才能发生的反应一定是吸热反应
B. 任何放热反应在常温条件下一定能发生反应
C. 反应物和生成物所具有的总能量决定了放热还是吸热
D. 吸热反应只能在加热的条件下才能进行
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是由常见元素组成的一些单质及其化合物之间的转化关系图。各方框表示有关的一种反应物或生成物(部分物质已经略去)。其中A、B、D在常温下均为无色无味的气体,C是能使湿润的红色石蕊试纸变蓝的气体,M是最常见的无色液体。

(1)写出C→E的化学方程式: 。
(2)实验室常用加热两种固体混合物的方法制备物质C,其化学方程式为: ,干燥C常用 (填写试剂名称)。
(3)E物质遇到D物质时,会观察到 现象,若用排水法收集F,则最终集气瓶中收集到的气体为 (填写物质的化学式)。
(4)写出F→G的离子方程式: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各化合物的命名正确的是( )
A.CH2═CH﹣CH═CH2 1,3﹣二丁烯
B.CH3COOCH2CH2OOCCH3乙二酸二乙酯
C.CH3CH2CH(OH)CH3 3﹣丁醇
D.![]() 2﹣甲基丁烷
2﹣甲基丁烷
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图1表示一些晶体中的某些结构,他们分别是氯化钠、氯化铯、干冰、金刚石、石墨结构中的某一种的某一部分(黑点可表示不同或相同的粒子).

(1)其中代表金刚石的是 (填编号字母,下同),金刚石中每个碳原子与 个碳原子最接近且距离相等.
(2)其中代表石墨的是 ,其中每个正六边形占有的碳原子数平均为 个;
(3)其中表示氯化钠的是 ,每个钠离子周围与它最接近且距离相等的钠离子有 个;
(4)代表氯化铯的是 ,每个铯离子与 个氯离子紧邻;
(5)代表干冰的是 ,每个二氧化碳分子与 个二氧化碳分子紧邻;
(6)由Mg、C、Ni三种元素形成的一种具有超导性的晶体,晶胞如图2所示.Mg位于C和Ni原子紧密堆积所形成的空隙当中.与一个Ni原子距离最近的Ni原子的数目为 ,该晶体的化学式为 .若该晶体的相对分子质量为M,阿伏加德罗常数为NA,Mg、C、Ni三种元素的原子半径分别为r1pm、r2pm、r3pm,则该晶体的密度表达式为 gcm﹣3.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲醇是一种可再生能源,具有开发和应用的广阔前景,工业上一般可采用如下反应来合成甲醇: CO(g)+2H2(g) ![]() CH3OH(g),现在实验室模拟该反应并进行分析。
CH3OH(g),现在实验室模拟该反应并进行分析。
(1)下列各项中,不能够说明该反应已达到平衡的是__________(填序号)。
a.恒温、恒容条件下,容器内的压强不发生变化
b.一定条件下,CH3OH分解的速率和CH3OH生成的速率相等
c.一定条件下,CO、H2和CH3OH的浓度保持不变
d.一定条件下,单位时间内消耗2 mol CO,同时生成1 mol CH3OH
(2)右图是该反应在不同温度下CO的转化率随时间变化的曲线。

① 该反应的焓变ΔH____________0(填“>”、“<”或“=”)。
② T1和T2温度下的平衡常数大小关系是K1____________K2(填“>”、“<”或“=”)。
③ 若容器容积不变,下列措施可增加甲醇产率的是______________。
a.升高温度
b.将CH3OH(g)从体系中分离
c.使用合适的催化剂
d.充入He,使体系总压强增大
(3)2009年10月,中国科学院长春应用化学研究所在甲醇燃料电池技术方面获得新突破,甲醇燃料电池的工作原理如右图所示。

①请写出c口通入的物质发生的相应电极反应式_________
②工作一段时间后,当0.2 mol甲醇完全反应生成CO2 时,有___________个电子转移
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】王同学以不同的化学思维方式或者规律给下列化学反应的类型进行分类,你认为分类合理的一组是
①CaO+H2O=Ca(OH)2;②Ca(OH)2![]() CuO+H2O;
CuO+H2O;
③Ba(OH)2+2HCl=BaCl2+2H2O;
④Fe+H2SO4=FeSO4+H2↑;⑤2Mg+O2![]() 2MgO。
2MgO。
A.属于有热量放出的反应的是②③ B.属于化合反应的是①②
C.属于有化合价变化的反应是④⑤ D.属于复分解反应的是③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把3.9gNa2O2放入100mL水中,充分反应后,计算:
(1)生成O2的体积(标准状况);
(2)反应后所得NaOH的物质的量浓度(反应前后溶液体积变化忽略不计).
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com