
X��Y��Z��WΪ���ֶ���������Ԫ�أ�����X��Z
ͬ�壬Y��Zͬ���ڣ�W�Ƕ���������Ԫ����ԭ�Ӱ뾶���ģ�Xԭ�������������Ǻ�����Ӳ�����3����Y���������������۴�����Ϊ6������˵����ȷ���ǣ� ��
A��YԪ������������Ӧ��ˮ���ﻯѧʽH2YO4
B��ԭ�Ӱ뾶��С�����˳��Ϊ�� X< Z < Y
C��Y��Z����Ԫ����̬�⻯���У�Z����̬�⻯�����ȶ�
D��X��W�γɵ����ֻ������У��������������ʵ���֮�Ⱦ�Ϊ1��2
��֪ʶ�㡿ԭ�ӽṹ��Ԫ�������ɵĹ�ϵ
���𰸽�����D ������X��Y��Z��WΪ���ֶ���������Ԫ�أ�W�Ƕ���������Ԫ����ԭ�Ӱ뾶���ģ���WΪNaԪ�أ�Xԭ�������������Ǻ�����Ӳ�����3����ֻ���е��Ӳ���Ϊ2������������Ϊ6����XΪOԪ�أ�X��Zͬ�壬��ZΪSԪ�أ�Y���������������۴�����Ϊ6�������Ϊ+7�ۣ�Y��Zͬ���ڣ�YΪClԪ�ء�
A��ClԪ������������Ӧˮ���ﻯѧʽΪHClO4����A����
B��Ԫ�����ڱ��У�ͬ����Ԫ�ش�����ԭ�Ӱ뾶��С����ԭ�Ӱ뾶Z��Y����B����
C���ǽ�����Cl��S����Cl��S����Ԫ����̬�⻯���У�Cl����̬�⻯����ȶ�����C����
D��X��W�γɵ����ֻ�����ΪNa2O��Na2O2���������������ʵ���֮�Ⱦ�Ϊ1��2����D��ȷ��
�ʴ�ѡD
��˼·�㲦�����⿼��λ�ýṹ���ʵ����ϵӦ�ã��ѶȲ���ע����ջ��ϼ���ԭ�ӽṹ����������ϵ��ע�����Ԫ�������ɡ���ϤԪ�ؼ��仯��������ʣ�


 һ����������ϵ�д�
һ����������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����1����1 L 1��00 mol��L-1��Na2CO3��Һ��μ��뵽1 L 1��25 mol��L-1�������У�����2����1 L 1��25 mol��L-1��������μ���1 L 1��00 mol��L-1 ��Na2CO3��Һ�У����β����������������֮�ȣ�ͬ��ͬѹ�£���
A��5��2 B��2��5 C��1��1 D��2��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���������ǡ�DZͧ�ϵĺ˷�Ӧ����ʹ����Һ�����ƺϽ�(�����ƺ͵������ۺ϶���)�����Ƚ��ʣ��й�˵������ȷ����
A���Ͻ���۵�һ�����ֽ�����
B�����ƺϽ���Ͷ��һ������ˮ�пɵ���ɫ��Һ����n(Al)��n(Na)
C�����ƺϽ�Ͷ�뵽�����Ȼ�ͭ��Һ�У�����������ͭ����Ҳ������ͭ����
D����m g��ͬ��ɵ����ƺϽ�Ͷ�����������У��ų���H2Խ�࣬��������������ԽС
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
������������ȷ���ǣ� ��
A������ijԪ��ԭ�ӵ���������������������ȷ����Ԫ�ص����ԭ������
B��CaCl2��MgCl2���嶼���׳��⣬���dz����ʵ���Ǿ��������ˮ�γ���Һ
C�����ݽ������˳����������ƶ�ұ������ʱ���ܵķ���
D�������ᡢ��ε��ܽ��Ա��������ж�ijЩ��Һ�еĸ��ֽⷴӦ�ܷ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����˵����ȷ���ǣ� ��
A���������Ӽ����ۼ��Ļ�����һ�������ӻ�����
B��Ԫ��ԭ�ӵ��������������ڸ�Ԫ�ص���������ϼ�
C��Ŀǰ�����ѷ��ֵ�Ԫ��������Ŀ��ԭ��������Ŀ��ͬ
D�������ԭ���У�����˽Ͻ����������˶��ĵ��������ϸ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���ײ��϶�������(TiO2)���кܸߵĻ�ѧ���ԣ��������������Ĵ�����
��1����ҵ�϶������ѵ��Ʊ��ǣ�
I. �������Ľ��ʯ(��Ҫ�ɷ�TiO2,��Ҫ����SiO2)��̼�ۻ��װ���Ȼ�¯�У��ڸ�����ͨ��Cl2,�Ƶû���SiCl4���ʵ�TiCl4��
II. ������SiCl4���ʵ�TiCl4���룬�õ�������TiCl4��
III. ��TiCl4�м�ˮ�����ȣ�ˮ��õ�����TiO2•xH2O��
IV. TiO2·xH2O���·ֽ�õ�TiO2��
��TiCl4��SiCl4�ڳ����µ�״̬��_______��II������ȡ�IJ�������_______��
|

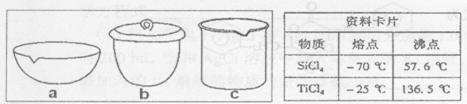
����ʵ��IV�У�Ӧ��TiO2.xH2O����_______ (���������)�м��ȡ�
��2���ݱ���������̬��·����������ʱ����һ������TiO2,TiO2��̫������������ĵ��ӱ�������ˮ�е�����ã�����H2O2,����̴������£�
a. O2��2O b. O+H2O��2OH(�ǻ�) c. OH+OH��H2O2
��b���ƻ���������������������������Թ��ۼ����Ǽ��Թ��ۼ�������
��H2O2�����·������е�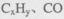 �ȣ�����Ҫ��������H2O2������������������ԡ���ԭ�ԡ�����
�ȣ�����Ҫ��������H2O2������������������ԡ���ԭ�ԡ�����
��3��������������Ҫ�Ļ�ѧ�Լ�������ˮ��Һ�ֳ�Ϊ˫��ˮ��������������ɱ����Ư�ȡ�ij��ѧ��ȤС��ȡһ�����Ĺ���������Һ��ȷ�ⶨ�˹�������ĺ�����
����д���пհף�
��ȡ10.00 mL�ܶ�ΪP g/mL�Ĺ���������Һϡ����250 mL��ȡϡ�ͺ�Ĺ���������Һ25.00mL����ƿ�У�����ϡ�����ữ��������ˮϡ�ͣ��������������ø�����ر���Һ�ζ������������䷴Ӧ�����ӷ���ʽ���£��뽫������ʵĻ�ѧ��������ƽ����ѧʽ��д�ڷ����
| |
 + H2O2+ H+= Mn2++ H2O+
+ H2O2+ H+= Mn2++ H2O+ �ڵζ�ʱ����������ر���Һע��______________�����ʽ����ʽ�����ζ����С��ζ������յ��������____________________________��
���ظ��ζ����Σ�ƽ������C mol/L KMnO4����Һ V mL,��ԭ����������Һ�й����������������Ϊ______________��
�����ζ�ǰ�ζ��ܼ����������ݣ��ζ���������ʧ����ⶨ���_________ ���ƫ�ߡ���ƫ�͡����䡱����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���ֶ�����Ԫ�ص�ijЩ���������ʾ������Z��M��WΪͬ����Ԫ�أ���
| Ԫ�ش��� | Y | X | W | M | Z |
| ԭ�Ӱ뾶����10-12 m�� | 64 | 73 | 78 | 96 | 113 |
| ��Ҫ���ϼ� | -1 | +5��-3 | +7��-1 | +4��-4 | +3 |
����˵������ȷ���ǣ� ��
A����M��W�γɵĻ������Ǻ��м��Լ��ļ��Է���
B�� X��M֮���γɵĻ�����侧����ԭ�Ӿ���
C����MԪ���γɵľ���,��̫���ܹ���������Ҫ���ϣ���ҵ����ȡM����,��ͨ���û���Ӧԭ��������
D��Y��ZԪ���γɵ�[ZY6]3-�������д�����λ���������ӹ��ͳ���������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
(1)д�����ӷ�Ӧ����ʽH����OH��===H2O����Ӧ��������ͬ���ͻ�ѧ����ʽ��
��________________________________________________________________________��
��________________________________________________________________________��
(2)�����з�Ӧ�У�
A��2F2��2H2O===4HF��O2
B��2Na��2H2O===2NaOH��H2��
C��CaO��H2O===Ca(OH)2
D��2H2O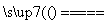 2H2����O2��
2H2����O2��
ˮֻ������������________��ˮֻ����ԭ������________��ˮ����������������ԭ������________��ˮ�Ȳ����������ֲ�����ԭ������________�����õ����ŷ���ʾB��Ӧ�ĵ���ת�Ʒ������Ŀ________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��Ҫ��д������ʽ��
(1) д��NaHCO3��ˮ��Һ��ĵ��뷽��ʽ
(2) ����ͭ������������Ӧ��д�����ӷ���ʽ��
(3) NaHSO4 + NaOH = Na2SO4 + H2O��д�����ӷ���ʽ��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com