
【题目】如图是H3AsO4水溶液中含砷的各物种分布分数(平衡时某物种的浓度占各物种浓度之和的分数)与pH的关系。下列说法错误的是( )
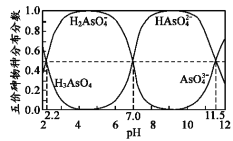
A.NaH2AsO4溶液呈酸性
B.向NaH2AsO4溶液滴加NaOH溶液过程中,c(H2AsO4-)/c(HAsO42-)先增加后减少
C.H3AsO4和HAsO42-在溶液中不能大量共存
D.Ka3(H3AsO4)的数量级为10-12
 孟建平小学滚动测试系列答案
孟建平小学滚动测试系列答案科目:高中化学 来源: 题型:
【题目】实验室可用NaBr、浓硫酸、乙醇等为原料制备少量溴乙烷(反应装置如图所示):C2H5—OH+HBr![]() C2H5—Br+H2O
C2H5—Br+H2O
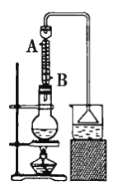
已知物质的用量:0.30molNaBr(s);0.25mol乙醇(密度为0.80g·cm-3);36mL浓硫酸(质量分数为98%,密度为1.84g·mL-1);25mL水。试回答下列问题:
(1)反应装置中烧瓶的容积应选择__(填序号)。
A.50mL B.100mL C.150mL D.250mL
(2)冷凝管中的冷凝水的流向应是__(填序号)。
A.A进B出 B.B进A出 C.从A进或B进均可
(3)实验完成后,需将烧瓶内的有机物蒸出,结果得到棕黄色的粗溴乙烷,欲得纯净的溴乙烷,应采取的操作是___。
(4)某同学在溴乙烷中加入NaOH乙醇溶液并加热,为判断其发生的是水解反应还是消去反应,则该同学向反应后的溶液中应加入的试剂是__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.将溴丙烷与氢氧化钾水溶液混合加热,再滴加硝酸银溶液,观察到有沉淀生成,可证明溴丙烷与氢氧化钾发生了反应
B.1mol·L-1CuSO4溶液2mL和0.5mol·L-1NaOH溶液4mL混合后加入40%的乙醛溶液0.5mL,加热煮沸可观察到砖红色沉淀
C.向试管中加入3~4![]() 无水乙醇,将试管浸入50℃左右热水浴中。将铜丝烧热,迅速插入乙醇中,反复多次,可以闻到刺激性气味
无水乙醇,将试管浸入50℃左右热水浴中。将铜丝烧热,迅速插入乙醇中,反复多次,可以闻到刺激性气味
D.热的苯酚溶液自然冷却变浑浊,是因为温度降低析出了苯酚晶体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】相同温度、相同浓度下的6种盐溶液,其pH由小到大的顺序如图所示,图中①②③代表的物质可能分别为
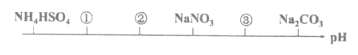
A.AlCl3 Al2(SO4)3 NaClOB.Al2(SO4)3 AlCl3 NaClO
C.Al2(SO4)3 AlCl3 NaOHD.CH3COOH AlCl3 Al2(SO4)3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究发现艾滋病治疗药物利托那韦对新型冠状病毒也有很好的抑制作用,它的合成中间体2-异丙基-4-(甲基氨基甲基)噻唑可按如下路线合成:

回答下列问题:
(1)A的结构简式是__________,C中官能团的名称为 ______________。
(2)①、⑥的反应类型分别是__________、_____。D的化学名称是______。
(3)E极易水解生成两种酸,写出E与NaOH溶液反应的化学方程式:_______。
(4)H的分子式为 __________________。
(5)I是相对分子质量比有机物 D 大 14 的同系物, 写出I 符合下列条件的所有同分异构体的结构简式:_____________。
①能发生银镜反应 ②与NaOH反应生成两种有机物
(6)设计由 ,和丙烯制备
,和丙烯制备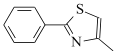 的合成路线______________(无机试剂任选)。
的合成路线______________(无机试剂任选)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关2个电化学装置的叙述正确的是

A. 装置①中,电子移动的路径是:Zn→Cu→CuSO4溶液→KCl盐桥→ZnSO4溶液
B. 在不改变总反应的前提下,装置①可用Na2SO4替换ZnSO4,用石墨替换Cu棒
C. 装置②中采用石墨电极,通电后,由于OH-向阳极迁移,导致阳极附近pH升高
D. 若装置②用于铁棒镀铜,则N极为铁棒
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,分别向体积相同、浓度均为1 mol/L的HA、HB两种酸溶液中不断加水稀释,酸溶液的pH与酸溶液浓度的对数(lg C)间的关系如图。下列对该过程相关分析正确的是
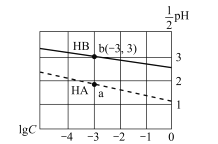
A. HB的电离常数(KA)数量级为10-3
B. 其钠盐的水解常数(Kh)大小关系是:NaB>NaA
C. a、b两点溶液中,水的电离程度b<a
D. 当lg C= -7时,两种酸溶液均有pH=7
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上常用铁碳混合物处理含Cu2+废水获得金属铜。当保持铁屑和活性炭总质量不变时,测得废水中Cu2+浓度在不同铁碳质量比(x)条件下随时间变化的曲线如下图所示。
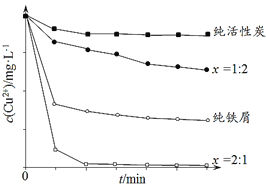
下列推论不合理的是
A. 活性炭对Cu2+具有一定的吸附作用
B. 铁屑和活性炭会在溶液中形成微电池,铁为负极
C. 增大铁碳混合物中铁碳比(x),一定会提高废水中Cu2+的去除速率
D. 利用铁碳混合物回收含Cu2+废水中铜的反应原理:Fe+Cu2+=Fe2++Cu
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com