
【题目】Ⅰ.在常温下,下列四种溶液:①0.1mol/L NH4Cl ②0.1mol/L CH3COONH4 ③0.1mol/L NH4HSO4④0.1mol/L NH3H2O,请根据要求填写下列空白:
(1)溶液①呈____ 性(填“酸”、“碱”或“中”),其原因是______(用离子方程式表示)。
(2)在上述四种溶液中,pH最小的是________。
(3)比较四种溶液中c(NH4+)的由大到小的顺序是______________(填序号)。
(4)四种溶液中,离子浓度为0.1 mol/L的是___________(填离子符号)。
Ⅱ. KMnO4溶液常用作氧化还原反应滴定的标准液,由于KMnO4的强氧化性,它的溶液很容易被空气中或水中的某些少量还原性物质还原,生成难溶性物质MnO(OH)2,因此配制KMnO4标准溶液的操作如下所述:称取稍多于所需要的KMnO4固体溶于水中,将溶液加热并保持微沸1h;用微孔玻璃漏斗过滤除去难溶的MnO(OH)2;过滤得到的KMnO4溶液贮存于棕色试剂瓶中并放在暗处;利用氧化还原反应滴定法,在70~80℃条件下用基准试剂溶液标定其浓度.
请回答下列问题:
(1)准确量取一定体积的KMnO4溶液需要使用的仪器是_____________。
(2)若选择H2C2O4 2H2O(M=126g/mol)作为基准试剂,准确称取Wg溶于水配成500mL溶液,配制溶液时,所用仪器除烧杯、胶头滴管和玻璃棒外,还需要_______。取25.00mL置于锥形瓶中,用KMnO4溶液滴定至终点,消耗KMnO4溶液VmL,则KMnO4溶液的物质的量浓度为________mol/L。
【答案】酸 NH4++H2O![]() NH3·H2O+H+ ③ ③﹥①﹥②﹥④ Cl- SO42- 酸式滴定管 500mL容量瓶
NH3·H2O+H+ ③ ③﹥①﹥②﹥④ Cl- SO42- 酸式滴定管 500mL容量瓶 ![]()
【解析】
Ⅰ.(1)①0.1mol/L NH4Cl溶液中铵根离子水解溶液显酸性。
(2)①0.1mol/L NH4Cl溶液中铵根离子水解溶液显酸性,②0.1mol/L CH3COONH4溶液中醋酸根离子和铵根离子水解程度相近溶液呈中性,③0.1mol/LNH4HSO4溶液电离出氢离子溶液显酸性,④0.1mol/LNH3·H2O 溶液中一水合氨电离溶液显碱性。
(3)铵根离子水解程度越大,离子浓度越小,④一水合氨难电离。
(4)四种溶液中,离子浓度为0.1mol/L的离子不发生水解。
Ⅱ.(1)高锰酸钾溶液具有强氧化性,不能使用碱式滴定管,可以选用酸式滴定管量取高锰酸钾溶液。
(2)配制一定浓度的溶液,应需要500mL容量瓶、烧杯、玻璃棒、胶头滴管等;先计算草酸的物质的量浓度,再根据草酸和高锰酸钾之间的关系式计算高锰酸钾的物质的量浓度。
Ⅰ.(1)①0.1mol/LNH4Cl溶液中铵根离子水解溶液显酸性,![]() 。
。
故答案为:酸, ![]() 。
。
(2)①0.1mol/L NH4Cl溶液中铵根离子水解溶液显酸性,c(H+)<0.1mol·L-1;
②0.1mol/L CH3COONH4溶液中醋酸根离子和铵根离子水解程度相近溶液呈中性;
③0.1mol/L NH4HSO4溶液电离出氢离子溶液显酸性,c(H+)=0.1mol·L-1;
④0.1mol/L NH3H2O溶液中一水合氨电离溶液显碱性,①③相比较,③酸性较强,则酸性最强的是③。
故答案为:③。
(3)①②③中,铵根离子水解程度越大,离子浓度越小,④一水合氨弱电离,则四种溶液中![]() 的由大到小的顺序是③>①>②>④。
的由大到小的顺序是③>①>②>④。
故答案为:③>①>②>④。
(4)四种溶液中,离子浓度为0.1mol/L的离子不发生水解,应为Cl- 、SO42-。
故答案为:Cl- 、SO42-。
Ⅱ.(1)高锰酸钾溶液具有强氧化性,量取时应该选用酸式滴定管。
故答案为:酸式滴定管。
(2)配制一定浓度的溶液,应需要500mL容量瓶、烧杯、玻璃棒、胶头滴管等,滴定时滴入最后一滴,高锰酸钾不反应,溶液变成紫红色并保持半分钟不褪色,说明滴定到达终点;草酸的物质的量浓度为: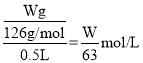 ,根据反应方程式
,根据反应方程式
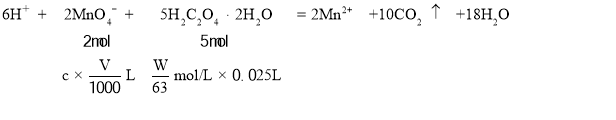
酸性高锰酸钾的物质的量浓度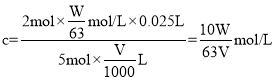 ,
,
故答案为:500mL容量瓶; ![]() 。
。


科目:高中化学 来源: 题型:
【题目】室温时,向20mL![]() 的醋酸溶液中不断滴入
的醋酸溶液中不断滴入![]() 的NaOH溶液,溶液的pH变化曲线,如图所示,在滴定过程中,关于溶液中离子浓度大小关系的描述不正确的是
的NaOH溶液,溶液的pH变化曲线,如图所示,在滴定过程中,关于溶液中离子浓度大小关系的描述不正确的是
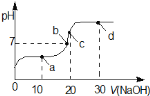
A.a点时:c![]()
![]()
![]()
![]()
![]() (OH-)
(OH-)
B.b点时:c![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
C.c点时:c![]()
![]()
![]()
![]()
![]()
![]()
![]()
D.d点时:c![]()
![]()
![]()
![]()
![]()
![]()
![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列方程式书写正确的是![]()
A.![]() 的水解离子方程式:
的水解离子方程式:![]()
B.以银为电极电解硫酸铜溶液离子方程式:![]()
![]()
![]()
C.向![]() 溶液中通入一定量
溶液中通入一定量![]() 的离子方程式可能为:
的离子方程式可能为:![]()
D.乙烯的燃烧热是![]() ,表示乙烯燃烧热的热化学方程式为:
,表示乙烯燃烧热的热化学方程式为:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,取![]() HY溶液与
HY溶液与![]()
![]() NaOH溶液等体积混合
NaOH溶液等体积混合![]() 忽略溶液体积的变化
忽略溶液体积的变化![]() ,测得混合溶液的
,测得混合溶液的![]() ,则下列说法正确的是
,则下列说法正确的是![]()
A.混合溶液中由水电离出的![]()
B.溶液中离子浓度由大到小的顺序为![]()
C.![]()
![]()
D.![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.![]() 的名称为2-乙基丁烷
的名称为2-乙基丁烷
B.35Cl和37Cl 互为同素异形体
C.![]() 经催化加氢后能生成2-甲基戊烷
经催化加氢后能生成2-甲基戊烷
D.CH3CH2COOH和HCOOCH3互为同系物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表代表周期表中的几种短周期元素,下列说法中错误的是
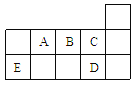
A. ED4分子中各原子均达8电子结构
B. AD3和ED4两分子的中心原子均为sp3杂化
C. A、B、C第一电离能的大小顺序为C>B>A
D. C、D气态氢化物稳定性强弱和沸点高低均为C>D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚硝酸钠被用作肉制品发色剂、防腐剂等,硝酸钠在肉制品加工中作发色剂。但亚硝酸钠是食品添加剂中急性毒性较强的物质之一,是一种剧毒药,摄取少量亚硝酸盐进入血液后,可使正常的血红蛋白变成正铁血红蛋白而失去携带氧的功能,导致组织缺氧。硝酸钠的毒性作用主要是由于它在食物中、在水中或在胃肠道内被还原成亚硝酸盐所致。亚硝酸钠生产方法是由硝酸生产过程中的氮氧化物气体![]() 、
、![]() 用氢氧化钠或碳酸钠溶液吸收制得。硝酸钠的生产方法是将硝酸生产中的尾气用碱液吸收后,经硝酸转化,再用碱中和、蒸发、结晶、分离制得。
用氢氧化钠或碳酸钠溶液吸收制得。硝酸钠的生产方法是将硝酸生产中的尾气用碱液吸收后,经硝酸转化,再用碱中和、蒸发、结晶、分离制得。
![]() 实验室可用加热亚硝酸钠与氯化铵的浓溶液制取氮气,写出该反应的化学方程式:______ ;将亚硝酸钠溶液滴加到含淀粉的酸性KI溶液中,可观察到溶液变蓝色,写出该反应的离子方程式:______ ;将亚硝酸钠溶液滴加到
实验室可用加热亚硝酸钠与氯化铵的浓溶液制取氮气,写出该反应的化学方程式:______ ;将亚硝酸钠溶液滴加到含淀粉的酸性KI溶液中,可观察到溶液变蓝色,写出该反应的离子方程式:______ ;将亚硝酸钠溶液滴加到![]() 酸性溶液中,可观察到溶液的颜色由 ______ 色变为绿色,写出该反应的离子方程式:______ 。
酸性溶液中,可观察到溶液的颜色由 ______ 色变为绿色,写出该反应的离子方程式:______ 。
![]() 写出氮氧化物
写出氮氧化物![]() 、
、![]() 与氢氧化钠溶液反应生成亚硝酸钠溶液的离子方程式:______ ;若用
与氢氧化钠溶液反应生成亚硝酸钠溶液的离子方程式:______ ;若用![]() 溶液吸收
溶液吸收![]() 可生成
可生成![]() ,
,![]() 和
和![]() 溶液完全反应时转移电子
溶液完全反应时转移电子![]() ,则反应的离子方程式为 ______ 。
,则反应的离子方程式为 ______ 。
![]() 从下列试剂中选用部分试剂鉴别亚硝酸钠、硝酸钠和氯化钠三种无色溶液,它们是 ______ 。
从下列试剂中选用部分试剂鉴别亚硝酸钠、硝酸钠和氯化钠三种无色溶液,它们是 ______ 。
A.稀盐酸![]() 溶液
溶液![]() 稀硝酸
稀硝酸![]() 氢氧化钠溶液
氢氧化钠溶液
![]() 等物质的量浓度的亚硝酸钠、氯化钠、碳酸钠三种溶液中阴离子总浓度由大到小的顺序是 ______
等物质的量浓度的亚硝酸钠、氯化钠、碳酸钠三种溶液中阴离子总浓度由大到小的顺序是 ______ ![]() 填溶液中溶质的化学式
填溶液中溶质的化学式![]() 。
。
![]() 工业品硝酸钠含少量杂质
工业品硝酸钠含少量杂质![]() 、
、![]() 、NaCl、水不溶物
、NaCl、水不溶物![]() ,某同学欲测定工业品硝酸钠的纯度,进行了如下实验:
,某同学欲测定工业品硝酸钠的纯度,进行了如下实验:
![]() 称取
称取![]() 干燥工业品硝酸钠,投入盛适量蒸馏水的烧杯中,充分搅拌后加入10mL
干燥工业品硝酸钠,投入盛适量蒸馏水的烧杯中,充分搅拌后加入10mL![]() 的A溶液
的A溶液![]() 足量
足量![]() ,充分反应后过滤;
,充分反应后过滤;
![]() 向滤液中加入足量KI溶液和适量稀硫酸,充分反应后将所得溶液配成1000mL溶液;
向滤液中加入足量KI溶液和适量稀硫酸,充分反应后将所得溶液配成1000mL溶液;
![]() 取
取![]() 所配溶液于锥形瓶中,加入少量B物质,再用
所配溶液于锥形瓶中,加入少量B物质,再用![]() 的
的![]() 溶液滴定,用去
溶液滴定,用去![]() 溶液
溶液![]() 。
。
(有关反应为:![]()
![]() 溶液中的溶质的化学式是 ______ ,加入A溶液的作用是 ______ 。
溶液中的溶质的化学式是 ______ ,加入A溶液的作用是 ______ 。
![]() 物质是 ______ ,滴定终点时的颜色变化是 ______ 。
物质是 ______ ,滴定终点时的颜色变化是 ______ 。
![]() 若该同学操作正确,但结果造成测定结果略偏高,其原因可能是
若该同学操作正确,但结果造成测定结果略偏高,其原因可能是![]() 任写一点
任写一点![]() ______ 。
______ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关说法不正确的是
A.催化剂既能改变化学反应速率又能改变化学反应限度
B.升高温度能改变工业合成氨的反应速率
C.把铜片和铁片紧靠在一起浸入稀硫酸中,铜片表面出现气泡
D.把锌粒放入盛有稀盐酸的试管中,加入几滴氯化铜溶液,能加快生成![]() 的速率
的速率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关热化学方程式的叙述中,正确的是( )
A.对于反应CO(g)+H2O(g) ![]() CO2(g)+H2(g) ΔH<0,升温ΔH不变
CO2(g)+H2(g) ΔH<0,升温ΔH不变
B.已知C(石墨,s)=C(金刚石,s)△H>0,则金刚石比石墨稳定
C.已知2H2(g)十O2(g)=2H2O(g) △H = -483.6 kJ/mol,则H2的燃烧热为 241.8 kJ/mol
D.已知2C(s)+2O2(g)=2CO2(g) △H1,2C(s)+O2(g)=2CO(g) △H2 ,则△H1>△H2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com