
【题目】汉代器物上的颜料“汉紫”至今尚没有发现其自然存在的记载。20世纪80年代科学家进行超导材料研究时,偶然发现其成分为紫色的硅酸铜钡(化学式:BaCuSi2Ox , Cu为+2价),下列有关“汉紫”的说法中不正确的是( )
A.用盐的形式表示:BaSiO3·CuSiO3
B.用氧化物形式表示:BaO·CuO·2SiO2
C.易溶于强酸、强碱
D.性质稳定,不易褪色
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】I 已知:HCN(aq)+NaOH(aq)═NaCN(aq)+H2O(l)△H=﹣12.1kJmol﹣1;HCl(aq)+NaOH(aq)═NaCl(aq)+H2O(l)△H=﹣55.6kJmol﹣1。则在水溶液中HCN![]() H++ CN-电离的△H为_______________kJmol﹣1
H++ CN-电离的△H为_______________kJmol﹣1
II 用右图所示装置进行中和热测定实验,请回答下列问题:
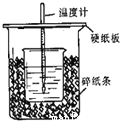
(1)大小烧杯之间填满碎泡沫塑料的作用是_____________,从实验装置上看,图中缺少的一种玻璃仪器______________。
(2)实验中若用60mL0.25mol·L-1H2SO4溶液跟50mL0.55mol·L-1NaOH溶液进行反应,与上述实验相比,所放出的热量___________ (填“相等”.“不相等”),所求中和热______________ (填“相等”.“不相等”),若用50mL0.50mol·L-1醋酸代替H2SO4溶液进行上述实验,测得反应前后温度的变化值会_____________ (填“偏大”、“偏小”、“不受影响”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】任一定温度下的定容容器中,当下列物理量不再发生变化时,能说明I2(g)+H2(g) ![]() 2HI(g)能说明达到平衡状态的有几个:①混合气体的压强②混合气体的密度③混合气体的总物质的量④混合气体的平均相对分子质量⑤混合气体的颜色⑥各反应物或生成物的浓度之比等于化学计量数之比⑦某种气体的百分含量。
2HI(g)能说明达到平衡状态的有几个:①混合气体的压强②混合气体的密度③混合气体的总物质的量④混合气体的平均相对分子质量⑤混合气体的颜色⑥各反应物或生成物的浓度之比等于化学计量数之比⑦某种气体的百分含量。
A. 2个 B. 3个 C. 4个 D. 5个
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知醋酸在水溶液中建立如下电离平衡: CH3COOH![]() H++ CH3COO-,若只改变一个条件,一定可以使c(CH3COOH)/c(H+)减小的是
H++ CH3COO-,若只改变一个条件,一定可以使c(CH3COOH)/c(H+)减小的是
A. 通氯化氢气体 B. 加入少量醋酸钾固体
C. 加入少量氢氧化钠固体 D. 通入少量冰醋酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学习小组用如图所示装置A,B分别探究金属锌与稀硫酸的反应,实验过程中A烧杯内的溶液温度升高,B烧杯的电流计指针发生偏转,请回答以下问题. 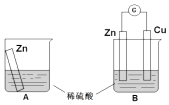
(1)A烧杯中反应的离子方程式为 .
(2)B中Zn板是极,发生的电极反应是 , Cu板上的现象是 , 发生的电极反应是 .
(3)从能量转化的角度来看,A,B中反应物的总能量(填“大于”、“小于”或“等于”)生成物总能量,A中是将化学能转变为 , B中主要是将化学能转变为 .
(4)该小组同学反思原电池的原理,其中观点正确的是(填字母序号).
A.原电池反应的过程中一定有电子转移
B.原电池装置需要2个电极
C.电极一定不能参加反应
D.氧化反应和还原反应可以拆开在两极发生.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物品或设备:①水泥路;②门窗玻璃;③水晶镜片;④石英钟表;⑤玛瑙手镯;⑥硅太阳能电池;⑦光导纤维;⑧计算机芯片。所用材料含有SiO2的是( )。
A.①②③④⑤⑦
B.①②⑦⑧
C.⑥⑧
D.全部
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室利用如图装置进行中和热的测定,请回答下列问题:
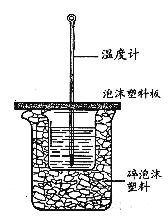
(1)大小烧杯之间填满碎泡沫塑料的作用是___________,做1次完整的中和热测定实验,温度计需使用________次,从实验装置上看,图中缺少的一种玻璃仪器是______________ 。
(2)使用补全仪器后的装置进行实验,取50mL0.25mol/LH2SO4溶液与 50mL0.55 mol/L NaOH溶液在小烧杯中进行中和反应,三次实验温度平均升高3.4℃。已知中和后生成的溶液的比热容c为 4.18J/ (g·℃),溶液的密度均为1g/cm3。通过计算可得中和热△H= ______ , H2SO4与NaOH反应的热化学方程式_______________ 。
(3)实验中若用60mL0.25mol·L-1H2SO4溶液跟50mL0.55mol·L-1NaOH溶液进行反应,与上述实验相比,所放出的热量___________ (填“相等”、“不相等”),所求中和热___________(填“相等”、“不相等”);若用50mL0.50mol·L-1醋酸代替H2SO4溶液进行上述实验,测得反应前后温度的变化值会_______。(填“偏大”、“偏小”、“不受影响”)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com