
下列反应类型中可以吸收能量的反应是 ( )。
①化合反应 ②分解反应 ③置换反应 ④复分解反应
⑤氧化还原反应
A.①②③④⑤ B.②④
C.①③④⑤ D.②
 轻松暑假总复习系列答案
轻松暑假总复习系列答案科目:高中化学 来源: 题型:
下列有关金属晶体的说法中不正确的是 ( )。
A.金属晶体是一种“巨型分子”
B.“电子气”为所有原子所共有
C.简单立方堆积的空间利用率最低
D.体心立方堆积的空间利用率最高
查看答案和解析>>
科目:高中化学 来源: 题型:
某化学兴趣小组欲研究当酶的浓度一定时,反应速率(v)与反应物浓度(c)、温度(T)的关系。以下两个图像是根据实验结论画出的。试根据图像回答下列问题:
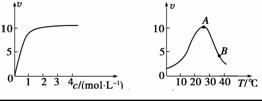
(1)图Ⅰ中,反应物达到某一浓度时,反应速率不再上升,其原因是_______________________。
(2)图Ⅱ中,A点所对应的温度是____________。
(3)图Ⅱ中,A点到B点曲线急剧下降,其原因是______________________________
________________________________________________________________________。
(4)将装有酶与反应物的甲、乙两试管分别放入12 ℃和75 ℃水浴锅内,20 min后取出转入37 ℃的水浴锅中保温,两试管反应反应速率变化分别为甲____________,乙____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
T ℃时,将气体X与气体Y置于一密闭容器中,反应生成气体Z,反应过程中各物质的浓度变化如图Ⅰ所示。保持其他条件不变,在T1、T2两种温度下,Y的体积分数变化如图Ⅱ所示。下列结论正确的是 ( )。
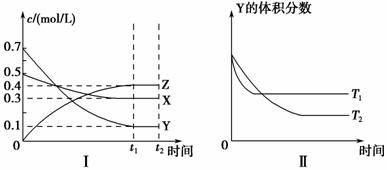
A.t2时,保持其他条件和物质状态不变,增大压强,化学平衡向逆反应方向移动
B.其他条件不变,若升高温度,正、逆反应速率均增大,且X的转化率增大
C.图Ⅱ中T1>T2,正反应是吸热反应
D.T ℃时,若密闭容器中各物质起始浓度为:0.4 mol/L X、0.4 mol/L Y、
0.2 mol/L Z,保持其他条件不变,达到平衡时Z的浓度为0.4 mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
在一定条件下,容积分别为1 L和2 L的甲、乙两密闭容器中同时充入2 mol A和2 mol B的混合气体,发生如下反应:2A(g)+B(g)xC(g) ΔH=Q kJ·mol-1,保持甲、乙两容器温度不变且相同,两容器中有关A的量随时间的变化如图:
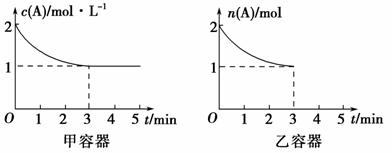
(1)根据上述图像判断,x________3(填“>”“=”或“<”)。写出该反应的平衡常数表达式:K=________,已知温度升高时,K值减小,则Q________0(填“>”“=”或“<”)。
(2)用B物质表示从0~3 min内乙容器中反应的平均速率v(B)=________。(结果保留三位小数)
(3)能说明甲容器中反应达到平衡状态的是________(填编号)。
a.2n(A)=n(B)=x·n(C)
b.c(A)、c(B)、c(C)保持一个定值
c.x·v逆(B)=v正(C)
d.甲容器中气体的密度保持不变
(4)甲、乙两容器中反应达到平衡时所耗时间相同,原因可能是__________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
如图是298 K时N2与H2反应过程中能量变化的曲线图。下列叙述正确的是 ( )。
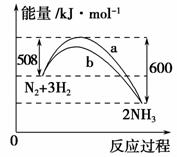
A.该反应的热化学方程式为N2+3H22NH3 ΔH=-92 kJ·mol-1
B.a曲线是加入催化剂时的能量变化曲线
C.加入催化剂,该化学反应的反应热发生改变
D.温度、体积一定,1 mol N2和3 mol H2反应后放出的热量为Q1 kJ,若2 mol N2和6 mol H2反应后放出的热量为Q2 kJ,则184>Q2>2Q1
查看答案和解析>>
科目:高中化学 来源: 题型:
已知反应:①101 kPa时,2C(s)+O2(g)===2CO(g)
ΔH=-221 kJ·mol-1
②稀溶液中,H+(aq)+OH-(aq)===H2O(l)
ΔH=-57.3 kJ·mol-1
下列结论正确的是 ( )。
A.碳的燃烧热的数值大于110.5 kJ·mol-1
B.①的反应热为221 kJ·mol-1
C.浓硫酸与稀NaOH溶液反应的中和热为-57.3 kJ·mol-1
D.稀硫酸与稀Ba(OH)2溶液反应生成1 mol水,放出57.3 kJ热量
查看答案和解析>>
科目:高中化学 来源: 题型:
燃料电池具有能量转化率高、无污染等特点,如图为MgNaClO燃料电池的结构示意图。下列说法正确的是 ( )。
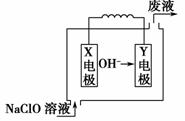
A.镁作Y电极
B.电池工作时,Na+向负极移动
C.废液的pH大于 NaClO 溶液的pH
D.X 电极上发生的反应为ClO- + 2H2O - 4e-===ClO + 4H+
+ 4H+
查看答案和解析>>
科目:高中化学 来源: 题型:
设NA为阿伏加德罗常数的值。下列说法正确的是( )
A.常温下,0.05 mol·L-1 Fe2(SO4)3溶液中含Fe3+数目为0.1NA
B.标准状况下,22.4 L甲苯中含C—H数目为8NA
C.常温常压下,3.2 g O2和O3混合物中,氧原子的数目为0.2NA
D.0.1 mol Na2O2与足量CO2反应时,转移的电子数目为0.2NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com