
下列关于有关物质的叙述正确的是 ( )
①酸性氧化物肯定是非金属氧化物
②不能跟酸反应的氧化物一定能跟碱反应
③碱性氧化物肯定是金属氧化物
④分散系一定是混合物
⑤浊液均可用过滤的方法分离
A.①③ B.③④ C.②④ D.④⑤
 天天向上口算本系列答案
天天向上口算本系列答案科目:高中化学 来源:2014年高考化学苏教版总复习 10-2 物质的检验、分离和提纯练习卷(解析版) 题型:选择题
取少量无机盐溶液,对其中的离子进行检验。下列判断正确的是( )
A.加入盐酸,产生白色沉淀,则试样中一定有Ag+
B.加入盐酸,产生能使澄清石灰水变浑浊的无色气体,则试样中一定有CO32-
C.加入NaOH溶液微热,产生能使湿润的红色石蕊试纸变蓝的气体,则试样中一定有NH4+
D.加入BaCl2溶液,产生白色沉淀,再加入稀硝酸,沉淀不溶解,则试样中一定有SO42-
查看答案和解析>>
科目:高中化学 来源:2014年高考化学苏教版总复习 1-2 物质的量、物质的聚集状态练习卷(解析版) 题型:实验题
测定1 mol氧气在标准状况下所占体积的实验操作步骤如下:
①按下图装配实验装置。
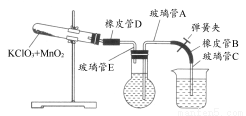
②洗净试管然后充分干燥。
③向500 mL烧瓶里装满水,向500 mL烧杯里加入少量水,把连接烧瓶和烧杯的玻璃管A、橡皮管B和玻璃管C中也装满水,中间不要留下气泡,然后用弹簧夹把橡皮管B夹紧。
④称得试管的质量为14.45 g,往试管里加入KClO3和MnO2的混合物,再称其质量为15.95 g。
⑤打开弹簧夹,把烧杯举起使烧瓶和烧杯中的水面一致,再关闭弹簧夹,然后把烧杯中的水倒掉。
⑥打开弹簧夹,加热试管的混合物到不再产生气体,即水不再流向烧杯时为止。
⑦反应完毕后把装置放置冷却到室温。
⑧调节烧杯的高度使烧瓶和烧杯中的水面一致,然后再关闭弹簧夹。
⑨用500 mL量筒测量烧杯里水的体积为285.0 mL,把它换算为标准状况下氧气的体积为279.7 mL。
⑩再称量冷却后试管的质量为15.55 g。
(1)在操作⑦中,装置冷却时,玻璃管C的出口,一直要在烧杯的水中,不能离开水面,其理由是 。
(2)简述操作⑧的必要性,即为什么要调节烧杯的高度,使烧瓶和烧杯中的水面一致? 。
(3)标准状况下,1 mol氧气所占的体积(保留小数后两位)为 L;混合物中MnO2的质量分数为 。
查看答案和解析>>
科目:高中化学 来源:2014年高考化学苏教版总复习 1-1 物质的分类、转化及分散系练习卷(解析版) 题型:填空题
在如下图所示的有关物质转化关系中,各物质均是我们中学化学所学的物质。C为一种黑色粉末,D为一种气体。
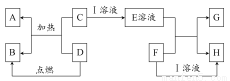
请根据框图中物质的转化关系及相关信息,用化学式填写下列空白:
(1)若F为可溶性碱,G为蓝色沉淀,则A为 ;D可能为 。
(2)若G为蓝色沉淀,H为难溶性盐,则I为 。
(3)若G、H都属于盐,且G为蓝色溶液,则I可能为 ;F可能为 。
查看答案和解析>>
科目:高中化学 来源:2014年高考化学苏教版总复习 1-1 物质的分类、转化及分散系练习卷(解析版) 题型:选择题
我国科学家在世界上第一次为一种名为“钴酞箐”的分子(直径为1.3×10-9m)恢复了磁性。“钴酞箐”分子的结构和性质与人体内的血红素和植物的叶绿素非常相似。下列关于“钴酞箐”分子的说法中正确的是 ( )
A.它的分子直径比Na+小
B.它的分子既能透过滤纸,也能透过半透膜
C.在水中形成的分散系能产生丁达尔效应
D.在水中所形成的分散系属悬浊液
查看答案和解析>>
科目:高中化学 来源:2014年高考化学苏教版一轮复习3-3铁、铜的获取及应用练习卷(解析版) 题型:选择题
向一定量的Cu、Fe2O3的混合物中加入300 mL 1 mol·L-1的盐酸,恰好使混合物完全溶解,所得溶液中不含Fe3+。若用过量的CO在高温下还原相同质量的原混合物,固体减少的质量为 ( )。
A.6.4 g B.4.8 g C.2.4 g D.1.6 g
查看答案和解析>>
科目:高中化学 来源:2014年高考化学苏教版一轮复习3-2从铝土矿到铝合金练习卷(解析版) 题型:填空题
2013年1月26日15时整,中国国产大型军用运输机运-20成功降落。标志着运-20首飞圆满成功。请回答下列问题:
Ⅰ.运-20根据结构和性能要求不同,使用的材料也不同,你认为下列材料中用于运-20制造,合理的是 (填序号)。
A.利用纯铝制造运-20发动机
B.用镁铝合金制造运-20座椅
C.用氧化铝制造运-20电器线路的导线
D.用普通钢制造运-20灭火器的外壳
Ⅱ.制造铝合金所需的铝从铝土矿中提取,已知铝土矿的主要成分为氧化铝(含有Fe2O3、SiO2杂质),SiO2不与盐酸反应但能溶解在NaOH溶液中生成可溶性Na2SiO3。工业上经过下列工艺可以冶炼金属铝:
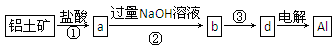
(1)①②中除加试剂外,还需要进行的操作是 。
(2)写出步骤②反应的化学方程式: 。
(3)③中需要通人过量的二氧化碳,写出该过程中含铝化合物发生反应的离子方程式: 。
(4)一种新型镁铝合金的化学式为Mg17Al12,科学家发现它具有储氢性能,是一种潜在的储氢材料,可在氩气保护下,将一定比例的Mg、Al单质在一定温度下熔炼获得。该合金在一定条件下完全吸氢的反应方程式为Mg17Al12+17H2=17MgH2+12Al,得到的混合物Y(17MgH2+12Al)在一定条件下能释放出氢气。
①制备镁铝合金(Mg17Al12)时通人氩气的目的是 。
②在5.0 mol·L-1盐酸中,混合物Y能完全释放出H2。1 mol Mg17A112完全吸氢后得到的混合物Y与上述盐酸完全反应,消耗盐酸的体积为 L。
查看答案和解析>>
科目:高中化学 来源:2014年高考化学苏教版一轮复习3-1钠、镁及其化合物练习卷(解析版) 题型:选择题
物质的量为0.10 mol的镁条在只含有CO2和O2混合气体的容器中燃烧(产物不含碳酸镁),反应后容器内固体物质的质量不可能为 ( )。
A.3.2 g B.4.0 g C.4.2 g D.4.6 g
查看答案和解析>>
科目:高中化学 来源:2014年高考化学苏教版一轮复习1-2-2溶液的配制及误差分析练习卷(解析版) 题型:填空题
在标准状况下,将224 L HCl气体溶于635 mL水中,所得盐酸的密度为1.18 g·cm-3。试计算:
(1)所得盐酸的质量分数和物质的量浓度分别是 、 。
(2)取出这种盐酸100 mL,稀释至1.18 L,所得稀盐酸的物质的量浓度是 。
(3)在40.0 mL 0.065 mol·L-1 Na2CO3溶液中,逐渐加入(2)所稀释的稀盐酸,边加边振荡。若使反应不产生CO2气体,加入稀盐酸的体积最多不超过 mL。
(4)将不纯的NaOH样品1 g(样品含少量Na2CO3和水),放入50 mL 2 mol·L-1的盐酸中,充分反应后,溶液呈酸性,中和多余的酸又用去40 mL 1 mol·L-1的NaOH溶液。蒸发中和后的溶液,最终得到 克固体。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com