
���� ��1�����������ڷ�Ӧ�е�Ԫ�ػ��ϼ۱仯���
��2����������ʵ���Ϊ$\frac{8.96L}{22.4L/mol}$=0.4mol�����Nԭ���غ��֪���μӷ�Ӧ����������ʵ���Ϊ2n[Cu��NO3��2]+n�����壩������ԭ����������ʵ�����������һ�������Ͷ������������ʵ����ĺͣ�����ϵ��ӡ�ԭ���غ������������NO��NO2��
��� �⣺��1�����ݷ���ʽCu+HNO3��Cu��NO3��2+NO��+NO2��+H2O ��֪�������ڷ�Ӧ�в��ֵ�Ԫ�ػ��ϼ۽��ͱ���Ϊ�����ԣ����ֻ��ϼ۲��䣬����Ϊ���ԣ�
�ʴ�Ϊ�������Ժ����ԣ�
��2����������ʵ���Ϊ$\frac{8.96L}{22.4L/mol}$=0.4mol�����Nԭ���غ��֪���μӷ�Ӧ����������ʵ���Ϊ2n[Cu��NO3��2]+n�����壩=0.3mol��2+0.4mol=1mol������ԭ����������ʵ���Ϊ��$\frac{8.96L}{22.4L/mol}$=0.4mol��
����������NO��NO2�����ʵ����ֱ�Ϊx��y������ԭ�Ӹ����غ㡢��ʧ�����غ�ɵã�
x+y=0.4
3x+y=0.3��2��
���x=0.1��y=0.3��
���Բ����Ļ��������NO��NO2�����Ϊ0.1mol��0.3mol=1��3��
�ʴ�Ϊ��0.4��1��1��3��
���� ���⿼������������ʼ��й�������ԭ��Ӧ�ļ��㣬���շ����Ļ�ѧ��Ӧ����ʧ�����غ㡢ԭ�Ӹ����غ�Ϊ���Ĺؼ������ط�������������Ŀ��飬��Ŀ�ѶȲ���



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �����ԣ�S��Cl2 | B�� | �����ԣ�K��Na | ||
| C�� | ���ȶ��ԣ�NaHCO3��Na2CO3 | D�� | ���ԣ�HClO4��H2SO4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | һ������ϩ | B�� | �����м��� | ||
| C�� | ���������� | D�� | һ���Ǽ������ϩ�Ļ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���ԣ���ˮ��Һ����HSCN��H2CO3��HCN | B�� | ��ԭ�ԣ�������Һ����Fe��OH��2��I-��KIO3 | ||
| C�� | ���ȶ��ԣ�NaCl��NaClO4��NaClO | D�� | �����ԣ�������Һ����I2��FeCl3��Co��OH��3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
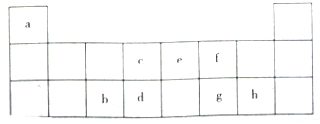 ��ñ���Ԫ�����ڱ��Ķ����ڲ��֣�������ĸ�ֱ��ʾһ��Ԫ�أ���ش��������⣺
��ñ���Ԫ�����ڱ��Ķ����ڲ��֣�������ĸ�ֱ��ʾһ��Ԫ�أ���ش��������⣺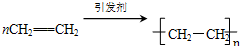 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 144.0 g CuSO4 | B�� | 144.0 g CuSO4•5H2O | ||
| C�� | 225.0 g CuSO4•5H2O | D�� | 250.0 g CuSO4•5H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 1��10-8mol/L | B�� | 1��10-6mol/L | C�� | 2��10-8mol/L | D�� | 1��10-7mol/L |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ijУ����С���ͬѧ����ɿα��Ҵ���������ȩ��ʵ��Ľ���ʵ�鷽������ͼ������������ʵ�������˳���Ѵ��ң���
ijУ����С���ͬѧ����ɿα��Ҵ���������ȩ��ʵ��Ľ���ʵ�鷽������ͼ������������ʵ�������˳���Ѵ��ң����鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com