
| A. | 肯定不能确定该物质的最简式 | B. | 肯定能确定该物质的最简式 | ||
| C. | 肯定不能确定该物质的分子式 | D. | 肯定不能确定该物质的结构式 |
分析 根据有机物燃烧生成的水和二氧化碳的物质的质量,可计算出水和二氧化碳的物质的量,根据C元素、H元素守恒可计算有机物中C、H元素的物质的量和质量,有机物的质量减去碳氢元素质量和得氧元素的质量,算出碳氢氧原子个数比得出最简式,以此解答该题.
解答 解:根据有机物燃烧生成的水和二氧化碳的物质的质量,可计算出水和二氧化碳的物质的量,根据C元素、H元素守恒可计算有机物中C、H元素的物质的量和质量,有机物的质量减去碳氢元素质量和得氧元素的质量,算出碳氢氧原子个数比得出最简式,故A错误,B正确;
若计算出的最简式中碳已达饱和可知分子式,若计算出的最简式中碳没饱和,则不能确定分子式,需要相对分子质量才能确定,故C错误,
根据质量变化只能确定分子组成,不能确定结构,故D错误.
故选B.
点评 本题考查有机物的分子式的计算,为高频考点,侧重于学生分析、实验和计算能力的考查,注意把握有机物的组成特点,从质量守恒的计算分析,难度中等.


科目:高中化学 来源: 题型:实验题
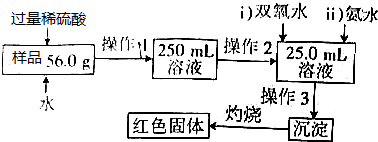
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Ca(OH)2 | B. | NaOH | C. | NaHCO3 | D. | Na2CO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①>②>③>④>⑤ | B. | ②>①>⑤>④>③ | C. | ③>④>⑤>①>② | D. | ⑤>④>③>②>① |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
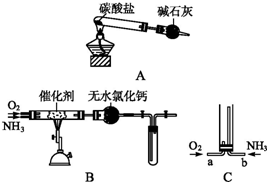
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaHS在水中的电离方程式为:NaHS═Na++H++S2- | |
| B. | 已知某温度下Ksp(CH3COOAg)=2.8×10-3,此温度下浓度均为0.1 mol•L-1的AgNO3溶液和CH3COONa溶液等体积混合一定能产生CH3COOAg沉淀 | |
| C. | 0.1mol/L CH3COOH溶液与0.05mol/L NaOH溶液等体积混合,所得溶液中:2c(H+)+c(CH3COOH)=c(CH3COO-)+2c(OH-) | |
| D. | 0.2mol/LNH3•H2O溶液与0.1mol/L盐酸等体积混合后,溶液显碱性,则:c(Cl-)>c(NH4+)>c(H+)>c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
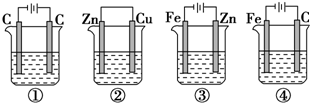
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com