
分析 金属氧化物是金属元素和氧元素组成的氧化物;
非金属氧化物是非金属元素和氧元素组成的氧化物;
酸是水溶液中电离出的阳离子全部是氢离子的化合物;酸分为强酸和弱酸;含有氧元素的酸称为含氧酸,不含氧元素的酸称为无氧酸;
碱是水溶液中电离出的阴离子全部是氢氧根离子的化合物;
盐是金属阳离子和酸根阴离子构成的化合物,铵盐例外;
根据盐中的阳离子可以将盐分为钠盐、钾盐、镁盐,根据阴离子可以将盐分为碳酸盐、硫酸盐、硝酸盐等,碱式盐是能电离出氢氧根离子的盐,
解答 解:②⑨水溶液中电离出的阳离子全部是氢离子,属于酸,其中⑨属于含氧酸;②属于无氧酸;③⑥水溶液中电离出的阴离子全部是氢氧根离子,属于碱; ⑤⑦⑧是金属阳离子(铵根离子)和酸根阴离子构成的化合物,属于盐,其中的⑤是能电离出氢氧根离子的盐,属于碱式盐,其中的⑧是能电离出镁离子的盐,属于镁盐,其中的⑤⑦是能电离出碳酸根离子的盐,属于碳酸盐,④⑩是金属元素和氧元素组成的氧化物,属于金属氧化物,①是非金属元素和氧元素组成的氧化物,属于非金属氧化物,②盐酸⑨硫酸能完全电离,电离出的阳离子全部是氢离子,属于强酸;NH4HCO3是能电离出铵根离子和酸根阴离子构成的化合物,属于铵盐,
故答案为:②⑨;⑨;②;③⑥;⑤⑦⑧;⑤;⑧;⑤⑦;④⑩;①;②⑨;⑦.
点评 本题考查了物质的分类,题目难度不大,注意掌握好概念、物质的分类依据是解题的关键,难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 对二甲苯的一氯代物有三种 | |
| B. | 对二甲苯的所有原子可能在同一平面内 | |
| C. | 对二甲苯能使溴水和酸性高锰酸钾因发生化学反应而褪色 | |
| D. | 在一定条件下,对二甲苯能发生氧化反应、还原反应、取代反应、加成反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
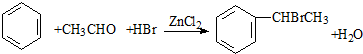 (卤烷基化反应)
(卤烷基化反应)
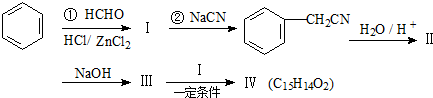
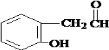 ,
,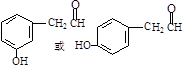 .
.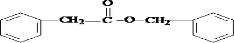 .
.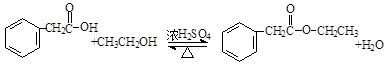 .
.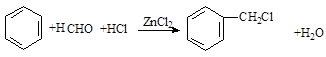 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 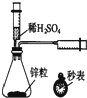 测定一定时间内生成H2的反应速率 | B. | 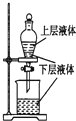 提取海带中的碘 | ||
| C. |  检验火柴燃烧产生的SO2 | D. | 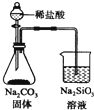 证明非金属性:Cl>C>Si |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 金刚石比石墨稳定性好 | |
| B. | 石墨和金刚石的转化是物理变化 | |
| C. | C(s、石墨)=C(s、金刚石)△H=+1.9 kJ•mol-1 | |
| D. | 断裂1 mol石墨中的化学键吸收的能量比断裂1 mol金刚石中的化学键吸收的能量小1.9 kJ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 普通的食醋中含3%~5%(质量分数)的乙酸 | |
| B. | 醋酸是一种弱酸,其酸性比碳酸更弱 | |
| C. | 可以用醋除去烧开水的壶内壁的水垢 | |
| D. | 在一定条件下,乙酸能与乙醇发生酯化反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
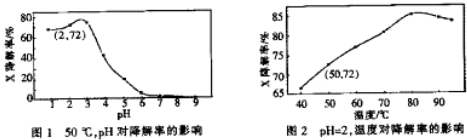
| A. | 温度为50℃,pH在3~6之间,X降解率随pH增大而减小 | |
| B. | pH=2,温度在40~80℃,X降解率温度升高而增大 | |
| C. | 无需再进行后续实验,就可以判断最佳反应条件是:pH=3、温度为80℃ | |
| D. | pH=2,温度为50℃,10min内v(X)=1.44×10-4 mol•L-1 min-1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com