
”¾ĢāÄæ”æĄūÓĆ·ĻŹ“æĢŅŗ(ŗ¬FeCl2”¢CuCl2¼°FeCl3)Öʱø¼īŠŌŹ“æĢŅŗ[Cu(NH3)4Cl2ČÜŅŗŗĶFeCl36H2OµÄÖ÷ŅŖ²½Öč£ŗÓĆH2O2Ńõ»Æ·ĻŹ“æĢŅŗ£¬Öʱø°±Ęų£¬Öʱø¼īŠŌŹ“æĢŅŗ[CuCl2+4NH3=Cu(NH3)4Cl2]”¢¹ĢŅŗ·ÖĄė£¬ÓĆŃĪĖįČܽā³Įµķ²¢ÖʱøFeCl36H2O”£ĻĀĮŠÓŠ¹ŲŹµŃéĖµ·ØÕżČ·µÄŹĒ£Ø £©
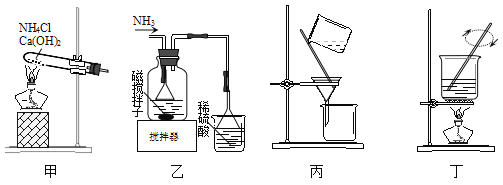
A. ÓĆH2O2Ńõ»Æ·ĻŹ“æĢŅŗµÄĄė×Ó·½³ĢŹ½ĪŖ£ŗ2H++2Fe2++H2O2=2Fe3++2H2O
B. ÓĆ×°ÖĆ¼×æÉŅŌÖʱøCu(NH3)4Cl2²¢³ĮĢś
C. ÓĆ×°ÖĆŅŅæÉŅŌ·ÖĄėCu(NH3)4Cl2ČÜŅŗŗĶFe(OH)3
D. ÓĆ×°Öƶ”ÓÉFeCl3ČÜŅŗÖʱøFeCl36H2OŠčŅŖ¾Õō·¢ÅØĖõ”¢ĄäČ“½į¾§”¢¹żĀĖĻ“µÓµČ²½Öč
”¾“š°ø”æB
”¾½āĪö”æ
ÓĆH2O2Ńõ»Æ·ĻŹ“æĢŅŗ£¬Ź¹ŃĒĢśĄė×ÓÉś³ÉĢśĄė×Ó£¬ÓĆ¼××°ÖĆÖʱø°±Ęų£¬Éś³ÉµÄ°±ĘųĶØČėŅŅ×°ÖĆ£¬Öʱø¼īŠŌŹ“æĢŅŗ[CuCl2+4NH3=Cu(NH3)4Cl2]£¬ÓƱū×°ÖĆ¹żĀĖ·ÖĄė£¬ÓĆŃĪĖįČܽāĒāŃõ»ÆĢś³Įµķ£¬½«ČÜŅŗŌŚÕō·¢ĆóÖŠ½ųŠŠÕō·¢£¬ĒŅÓ¦ĶØČėĀČ»ÆĒā·ĄÖ¹ĢśĄė×ÓĖ®½ā£¬ŅŌ“ļµ½ÖʱøFeCl36H2OµÄÄæµÄ£¬ŅŌ“Ė½ā“šøĆĢā”£
A.H2O2¾ßÓŠĒæµÄŃõ»ÆŠŌ£¬æÉÓĆH2O2Ńõ»Æ·ĻŹ“æĢŅŗÖŠµÄFe2+£¬·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ£ŗ2H++2Fe2++H2O2=2Fe3++2H2O£¬AÕżČ·£»
B.°±ĘųŅ×ČÜÓŚĖ®£¬×¢Ņā·ĄÖ¹µ¹Īü£¬ĖłŅŌŅŖŃ”ÓĆŅŅ×°ÖĆ£¬°±ĘųÓėČÜŅŗ·“Ӧɜ³ÉCu (NH3)4Cl2ŗĶĒāŃõ»ÆĢś£¬B“ķĪó£»
C.ÓĆ×°ÖƱūæÉŅŌ·ÖĄėæÉČÜŠŌCu(NH3)4Cl2ČÜŅŗŗĶÄŃČÜŠŌµÄ¹ĢĢ¬Fe(OH)3£¬C“ķĪó£»
D.ÓÉFeCl3ČÜŅŗÖʱøFeCl36H2OŠčŅŖŌŚÕō·¢ĆóÖŠÕōøÉ£¬²»ÄÜŌŁÉÕ±ÖŠ½ųŠŠ£¬D“ķĪó£»
¹ŹŗĻĄķŃ”ĻīŹĒA”£



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”潫 4 mol A ĘųĢåŗĶ 2 mol B ĘųĢåŌŚ 2 L µÄ¶ØČŻČŻĘ÷ÖŠ»ģŗĻ²¢ŌŚŅ»¶ØĢõ¼žĻĀ·¢ÉśČēĻĀ·“Ó¦ 2A£Øg£©£«B£Øg£©![]() 2C£Øg£© ”÷H<0 £¬¾ 2 s£ØĆė£©ŗó²āµĆ C µÄÅضČĪŖ 0. 6 mol”¤L-1 £¬ĻÖÓŠĻĀĮŠ¼øÖÖĖµ·Ø£ŗ
2C£Øg£© ”÷H<0 £¬¾ 2 s£ØĆė£©ŗó²āµĆ C µÄÅضČĪŖ 0. 6 mol”¤L-1 £¬ĻÖÓŠĻĀĮŠ¼øÖÖĖµ·Ø£ŗ
¢Ł ÓĆĪļÖŹ A ±ķŹ¾µÄ·“Ó¦µÄĘ½¾łĖŁĀŹĪŖ 0.3 mol”¤L-1s-1
¢Ś “ļµ½Ę½ŗāדĢ¬Ź±£¬ÉżøßĪĀ¶Č£¬ŌņøĆ»ÆŃ§Ę½ŗāĻņ×óŅĘ¶Æ£¬Ķ¬Ź±»ÆŃ§Ę½ŗā³£ŹżKŅ²¼õŠ”
¢Ū 2 s Ź±ĪļÖŹ A µÄ×Ŗ»ÆĀŹĪŖ70£„
¢Ü “ļµ½Ę½ŗāדĢ¬Ź±£¬Ōö¼ÓAĪļÖŹµÄĮ棬AŗĶB×Ŗ»ÆĀŹ¶¼Ģįøß
¢Żµ±ø÷ĪļÖŹÅضČĀś×ćc(A)=2c(B)= c(C)Ź±£¬øĆ·“Ó¦“ļµ½ĮĖĘ½ŗāדĢ¬
ĘäÖŠÕżČ·µÄŹĒ£Ø £©
A. ¢Ł¢Ū B. ¢Ł¢Ś C. ¢Ś¢Ū D. ¢Ū¢Ü
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ»ÆŗĻĪļGŹĒŗĻ³ÉijÖÖĻų“Ņ©µÄÖŠ¼äĢ壬GµÄŗĻ³ÉĀ·ĻßČēĶ¼£¬Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ

ŅŃÖŖ£ŗI£®»ÆŗĻĪļAµÄŗĖ“Ź²ÕńĒāĘ×ÓŠ4×éĪüŹÕ·å”£
¢ņ£®Ķس£ĒéæöĻĀ£¬ŌŚĶ¬Ņ»øöĢ¼Ō×ÓÉĻĮ¬ÓŠĮ½øöōĒ»ł²»ĪČ¶Ø£¬Ņ×ĶŃĖ®ŠĪ³ÉōŹ»ł”£
¢ó£®Č©ÄÜ·¢ÉśōĒČ©ĖõŗĻ·“Ó¦£¬ŌŁĶŃĖ®Éś³É²»±„ŗĶČ©£ŗ

¢ō£®
(1)AµÄ½į¹¹¼ņŹ½ŹĒ________£¬Ćū³ĘŹĒ________£¬1mol AĶźČ«Č¼ÉÕĻūŗÄŃõĘųµÄĪļÖŹµÄĮæĪŖ________mol”£
(2)BÉś³ÉCµÄ»Æѧ·½³ĢŹ½ŹĒ________________________________”£
(3)CµÄ·Ö×ÓŹ½ĪŖ________”£
(4)EÉś³ÉFµÄ·“Ó¦ĄąŠĶŹĒ________________”£
(5)GÖŠŗ¬Ńõ¹ŁÄÜĶŵÄĆū³ĘŹĒ________________”£
(6)·ūŗĻĻĀĮŠĢõ¼žµÄBµÄĶ¬·ÖŅģ¹¹Ģå¹²ÓŠ________ÖÖ”£
¢ŁÄÜÓėĀČ»ÆĢśČÜŅŗ·¢ÉśĻŌÉ«·“Ó¦
¢Ś1H”ŖNMRĘ×ĻŌŹ¾·Ö×ÓÖŠ±½»·ÉĻÓŠ2ÖÖ²»Ķ¬»Æѧ»·¾³µÄĒāŌ×Ó
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŌŚŗōĪüĆę¾ßŗĶĒ±Ė®Ķ§ÖŠæÉÓĆ¹żŃõ»ÆÄĘ×÷ĪŖ¹©Ńõ¼Į”£ĒėŃ”ŌńŹŹµ±µÄ»ÆѧŹŌ¼ĮŗĶŹµŃéÓĆĘ·£¬ÓĆĻĀĶ¼ÖŠµÄŹµŃé×°ÖĆ½ųŠŠŹµŃ飬֤Ć÷¹żŃõ»ÆÄĘæÉ×÷¹©Ńõ¼Į”£

£Ø1£©×°ÖĆAŹĒCO2ĘųĢåµÄ·¢Éś×°ÖĆ£¬ĒėŠ“³öŅĒĘ÷aµÄĆū³Ę__________”£
£Ø2£©BÖŠŹ¢±„ŗĶNaHCO3ČÜŅŗ£¬Ęä×÷ÓĆŹĒ___________”£
£Ø3£©Š“³öCÖŠ¹żŃõ»ÆÄĘÓė¶žŃõ»ÆĢ¼·“Ó¦µÄ»Æѧ·½³ĢŹ½____________________”£
£Ø4£©DÖŠŹ¢·ÅµÄŹŌ¼ĮæÉŅŌŹĒ__________£ØĢīŠņŗÅ£©”£
¢Ł ÅØH2SO4 ¢Ś NaOHČÜŅŗ ¢Ū CaCl2ČÜŅŗ ¢Ü Ca(OH)2ČÜŅŗ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠÓŠ¹ŲÓŠ»śĪļ½į¹¹ŗĶŠŌÖŹµÄĖµ·ØÕżČ·µÄŹĒ£Ø””””£©
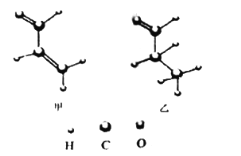
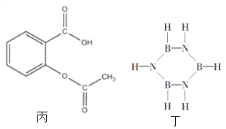
A. ¼×ÖŠĖłÓŠŌ×ÓæÉÄÜ“¦ÓŚĶ¬Ņ»Ę½Ćę
B. ŅŅµÄŅ»ĀČ“śĪļÓŠ4ÖÖ
C. ±ūŅ»¶ØĢõ¼žĻĀÄÜ·¢ÉśµÄ·“Ó¦ĄąŠĶÓŠČ”“ś£¬¼Ó³É£¬Ńõ»Æ£¬ĻūČ„·“Ó¦
D. ¶”Óė±½»„ĪŖµČµē×ÓĢ壬æÉÓɱ½µÄ½į¹¹ŗĶŠŌÖŹĶĘ²ā¶”µÄ½į¹¹ÓėŠŌÖŹ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĄ×ŵąŗŹĒÖĪĮĘĀżŠŌŠÄ½ŹĶ“Ź×Ń”ŠĀŅ©”£Ą×ŵąŗŗĻ³ÉĀ·ĻßČēĻĀ£ŗ

£Ø1£©Ą×ŵąŗÖŠŗ¬Ńõ¹ŁÄÜĶÅ£¬³żõ£°·¼ü£Ø-NHCO-£©Ķā£¬ĮķĮ½ÖÖ¹ŁÄÜĶÅĆū³Ę£ŗ___”¢____”£
£Ø2£©Š“³öĀś×ćĻĀĮŠĢõ¼žAµÄĶ¬·ÖŅģ¹¹ĢåµÄŹżÄæ_____”£¢ŁÄÜÓėFeCl3ČÜŅŗ·¢ÉśĻŌÉ«·“Ó¦£»¢Ś1moløĆ·Ö×ÓæÉÓė2molNaOH·“Ó¦”£
£Ø3£©“ÓĄ×ŵąŗŗĻ³ÉĀ·ĻߵƵ½ĘōŹ¾£¬æÉÓĆ¼ä¶ž¼×±½”¢ClCH2COCl”¢(C2H5)NH£ØĪŽ»śŹŌ¼ĮČĪÓĆ£©ŗĻ³ÉŃĪĖįĄū¶ąæØŅņ£¬ĒėŌŚŗįĻßÉĻ²¹³ä·“Ó¦Īļ£¬ŌŚ·½æņÄŚ²¹³äÉś³ÉĪļ”£_____”¢_____”¢_____”¢_____”¢_____”¢_____”£

ŃĪĖįĄū¶ąæØŅņ
ŅŃÖŖ£ŗ![]()

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æH2ŹĒŅ»ÖÖÖŲŅŖµÄĒå½ąÄÜŌ“”£
(1)2018ÄźĪŅ¹śÄ³æĘŃŠĶÅ¶ÓĄūÓĆĶøŃõĤ£¬Ņ»²½¼“»ńµĆŗĻ³É°±ŌĮĻŗĶŗĻ³ÉŅŗĢ¬Č¼ĮĻµÄŌĮĻ”£Ę乤×÷ŌĄķČēĶ¼ĖłŹ¾£ØæÕĘųÖŠN2ÓėO2µÄĪļÖŹµÄĮæÖ®±Č°“4£ŗ1¼Ę£©”£¹¤×÷¹ż³ĢÖŠ£¬Ä¤I²ąĖłµĆ![]() =3£¬ŌņĤI²ąµÄµē¼«·½³ĢŹ½ĪŖ________________________”£
=3£¬ŌņĤI²ąµÄµē¼«·½³ĢŹ½ĪŖ________________________”£

(2)ŅŃÖŖ: CO2(g)+3H2(g)=CH3OH(g)+H2O(g) ¦¤H2=-49.0kJ/mol£¬
CO(g)+H2O(g)=CO2(g)+H2(g) ¦¤H3= -41.1 kJ/mol£¬H2»¹ŌCO·“Ó¦ŗĻ³É¼×“¼µÄČČ»Æѧ·½³ĢŹ½ĪŖ£ŗCO(g)+2H2(g)![]() CH3OH(g)¦¤H1£¬Ōņ¦¤H1=_____________ kJ/mol£¬øĆ·“Ó¦×Ō·¢½ųŠŠµÄĢõ¼žĪŖ_________”£
CH3OH(g)¦¤H1£¬Ōņ¦¤H1=_____________ kJ/mol£¬øĆ·“Ó¦×Ō·¢½ųŠŠµÄĢõ¼žĪŖ_________”£
A.øßĪĀ B.µĶĪĀ C.ČĪŗĪĪĀ¶ČĢõ¼žĻĀ
(3)ŗćĪĀŗćŃ¹ĻĀ£¬ŌŚČŻ»żæɱäµÄĆܱÕČŻĘ÷ÖŠ¼ÓČė1mol COŗĶ2.2 mol H2£¬·¢Éś·“Ó¦ CO(g)+2H2(g)![]() CH3OH(g)£¬ŹµŃé²āµĆĘ½ŗāŹ±COµÄ×Ŗ»ÆĀŹĖęĪĀ¶Č”¢Ń¹ĒæµÄ±ä»ÆČēĶ¼ĖłŹ¾”£
CH3OH(g)£¬ŹµŃé²āµĆĘ½ŗāŹ±COµÄ×Ŗ»ÆĀŹĖęĪĀ¶Č”¢Ń¹ĒæµÄ±ä»ÆČēĶ¼ĖłŹ¾”£

P1_______P2£¬ÅŠ¶ĻµÄĄķÓÉŹĒ____________________________”£
(4)Čō·“Ó¦CO(g)+2H2(g)![]() CH3OH(g)ŌŚĪĀ¶Č²»±äĒŅĢå»żŗć¶ØĪŖ1LµÄĆܱÕČŻĘ÷ÖŠ·¢Éś£¬·“Ó¦¹ż³ĢÖŠø÷ĪļÖŹµÄĪļÖŹµÄĮæĖꏱ¼ä±ä»Æ¼ūĻĀ±ķĖłŹ¾£ŗ
CH3OH(g)ŌŚĪĀ¶Č²»±äĒŅĢå»żŗć¶ØĪŖ1LµÄĆܱÕČŻĘ÷ÖŠ·¢Éś£¬·“Ó¦¹ż³ĢÖŠø÷ĪļÖŹµÄĪļÖŹµÄĮæĖꏱ¼ä±ä»Æ¼ūĻĀ±ķĖłŹ¾£ŗ
Ź±¼ä/min | 0 | 5 | 10 | 15 |
H2 | 4 | 2 | ||
CO | 2 | 1 | ||
CH3OH(g) | 0 | 0.7 |
¢ŁĻĀĮŠø÷ĻīÄÜ×÷ĪŖÅŠ¶ĻøĆ·“Ó¦“ļµ½Ę½ŗā±źÖ¾µÄŹĒ_____(Ģī×ÖÄø)£»
A.ČŻĘ÷ÄŚŃ¹Ēæ±£³Ö²»±ä B.2vÕż(H2)=vÄę(CH3OH)
C.»ģŗĻĘųĢåµÄĻą¶Ō·Ö×ÓÖŹĮæ±£³Ö²»±ä D.»ģŗĻĘųĢåµÄĆܶȱ£³Ö²»±ä
¢ŚČōĘšŹ¼Ń¹ĒæĪŖP0 kPa£¬ŌņŌŚøĆĪĀ¶ČĻĀ·“Ó¦µÄĘ½ŗā³£ŹżKp=__________(kPa)-2”££ØÓĆĘ½ŗā·ÖŃ¹“śĢęĘ½ŗāÅØ¶Č¼ĘĖć£¬·ÖŃ¹=×ÜŃ¹”ĮĪļÖŹµÄĮæ·ÖŹż£©”£
¢Ū·“Ó¦ĖŁĀŹČōÓƵ„Ī»Ź±¼äÄŚ·ÖŃ¹µÄ±ä»Æ±ķŹ¾£¬Ōņ10minÄŚH2µÄ·“Ó¦ĖŁĀŹv(H2)= _______Pa/min”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”湤Ņµµē½ā±„ŗĶŹ³ŃĪĖ®Ä£Äā×°ÖĆµÄ½į¹¹ČēĶ¼ĖłŹ¾£ŗ


£Ø1£©Š“³öµē½ā±„ŗĶŹ³ŃĪĖ®µÄ»Æѧ·½³ĢŹ½____£¬øĆ¹¤Ņµ³Ę___¹¤Ņµ”£
£Ø2£©Źµ¼ŹÉś²śÖŠŹ¹ÓƵÄŃĪĶłĶłŗ¬ÓŠŅ»Š©ŌÓÖŹ£¬ŌŚµē½āŹ³ŃĪĖ®Ö®Ē°£¬ŠčŅŖĢį“æŹ³ŃĪĖ®”£ĪŖĮĖ³żČ„“ÖŃĪÖŠµÄCa2+”¢Mg2+”¢SO42£¼°ÄąÉ³£¬æɽ«“ÖŃĪČÜÓŚĖ®£¬Č»ŗó½ųŠŠĻĀĮŠĪåĻī²Ł×÷£¬¢Ł¹żĀĖ ¢Ś¼Ó¹żĮæµÄNaOHČÜŅŗ ¢Ū¼ÓŹŹĮæµÄŃĪĖį ¢Ü¼Ó¹żĮæµÄNa2CO3ČÜŅŗ ¢Ż¼Ó¹żĮæµÄBaCl2ČÜŅŗ£¬²Ł×÷ÕżČ·µÄĖ³ŠņŹĒ____£ØŃ”Ģī×ÖÄø£©
a£®¢Ł¢Ü¢Ś¢Ż¢Ū b£®¢Ż¢Ś¢Ü¢Ł¢Ū c£®¢Ś¢Ż¢Ü¢Ł¢Ū d£®¢Ż¢Ś¢Ü¢Ū¢Ł
£Ø3£©ŌŚøĆ×°ÖĆÖŠŠ“³ö×°NaOHČÜŅŗŹŌ¹ÜÖŠĖł·¢ÉśµÄ»Æѧ·“Ó¦·½³ĢŹ½_____”£
£Ø4£©¹¤ŅµÉĻÓĆ____£ØŠ“ĪļÖŹĆū³Ę£©ŗĶµē½ā²śĪļ____·“Ó¦æÉÖʵĆĘÆ·Ū¾«£¬ ĘÆ·Ū¾«³ØæŚ·ÅÖĆÓŚæÕĘųÖŠŅ׏§Š§£¬ŌŅņŹĒ£ØÓĆ»Æѧ·½³ĢŹ½±ķŹ¾£©___”¢____”£
£Ø5£©¹¤ŅµÉĻÓĆĮ½ÖÖµē½ā²śĪļŌŚČēĶ¼ŗĻ³ÉĖžÖŠŗĻ³ÉĀČ»ÆĒā£¬A“¦ĶØČė___£¬B“¦ĶØČė___£¬ŗó½«ĀČ»ÆĒāČÜÓŚĖ®ÖŠ¼“æɵƵ½ŃĪĖį£¬ĘäµēĄė·½³ĢŹ½ĪŖ___”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠ¹ŲÓŚČ¼ĮĻ³ä·ÖČ¼ÉÕµÄĖµ·Ø£¬²»ÕżČ·µÄŹĒ ( )
A. æÕĘųĮæŌ½¶ąŌ½ŗĆB. Ó¦ĶØČėŹŹĮææÕĘų
C. ¹ĢĢåČ¼ĮĻČ¼ÉÕĒ°ŅŖ·ŪĖéD. ŅŗĢåČ¼ĮĻČ¼ÉÕŹ±æÉŅŌŅŌĪķדÅē³ö
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com