
| A�� | ���ʵ���������;�� �ǰ���ҩ��������ϸ���ϳɺ���--���Ʒ��ס���Ĥ�ס���·��Ⱦ����������Ⱦ ��������к�-----θ�����IJ��˷��ú��������Ƶ�ҩ�� | |
| B�� | ���������� ���ơ���ɫ��Ⱦ��--���ٺͿ���ʹ������������Ʒ ��ֹˮ����Ⱦ--�ᳫʹ������ϴ�·� | |
| C�� | ������ȫ��ʶ�� ���üپ��ж�--�ɼ״����� ʳ�ü����ж�--�������������� | |
| D�� | �����е�һЩ������ ��ȥ�·��ϵ�����--��������ϴ�� ʹúȼ�ո���--������ú������Ӵ���� |
���� A���ǰ���ҩ��������ϸ���ϳɺ���������ƾ���ǿ��ʴ�ԣ�
B����ɫ������Ʒ���𡰰�ɫ��Ⱦ��������ϴ�·ۻ���Ⱦˮ��
C���״����������ƶ������к���
D���������������ͣ������ȼ���������ĽӴ�������Դٽ�ȼ�գ����Ծݴ˽��
��� �⣺A���ǰ���ҩ��������ϸ���ϳɺ��ᣬ�����ƶ���ϸ������ĸ�Ⱦ����������кͷ�Ӧ��ԭ������֪��θ�����IJ��˿��Է��ú�����������ҩ����Dz������������ƣ��������ƾ���ǿ��ʴ�ԣ���A����
B����ɫ������Ʒ���𡰰�ɫ��Ⱦ�������ٺͿ���ʹ������������Ʒ�����Կ��ơ���ɫ��Ⱦ��������ϴ�·ۻ���Ⱦˮ���ᳫʹ������ϴ�·ۣ����Է�ֹˮ����Ⱦ����B��ȷ��
C���״������������ж���ʳ�ü����ж�����������������ģ���C��ȷ��
D���������ͳ�ȥ�·��ϵ����ۣ��������Ӵ����Խ��ȼ��Խ���ң���������ú������ĽӴ��������ʹúȼ�ո�������D��ȷ��
��ѡA��
���� ������Ҫ�������ʵ����ʺ���;���ѶȲ������ʾ��ж������ʣ����ʱӦ���������ʵ���;�������ʵ��������ʾ����ģ�


 ��ѧʵ����ϵ�д�
��ѧʵ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
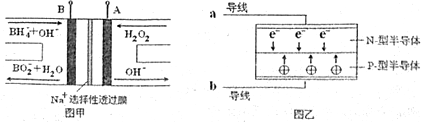
| A�� | ���A�����ĵ缫��ӦʽΪ��H2O2+2e-=2OH- | |
| B�� | ��طŵ�����У�Na+�Ӹ��������������ƶ� | |
| C�� | ÿ��1mol NaBH4�μӷ�Ӧת�Ƶ�����Ϊ4NA | |
| D�� | ҪʹLED����������������⣬ͼ���еĵ���aӦ��ͼ���е�B������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

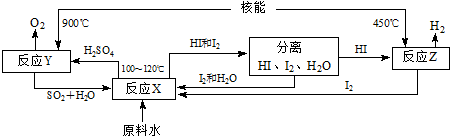
 ����Ӧ����������Ӧ��ȡ����Ӧ��
����Ӧ����������Ӧ��ȡ����Ӧ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 2.3�˽������ڸ�������б�������������ʱʧȥ�ĵ�����ĿΪ0.1NA | |
| B�� | 18��ˮ������������ĿΪNA | |
| C�� | �ڳ��³�ѹ�£�11.2�����������ķ�����ĿΪ0.5NA | |
| D�� | 32�˳���������ԭ����ĿΪNA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com