
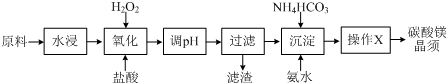
| ���� | ��ʼ���� | ������ȫ |
| Fe��OH��3 | 2.7 | 3.7 |
| Fe��OH��2 | 7.6 | 9.6 |
| Mg��OH��2 | 9.9 | 11.1 |
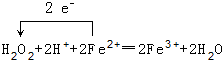 ��
������ ԭ��ˮ������������⣬��������������Ϊ�����ӣ��ٵ���pH��ʹ������ת��Ϊ������������ȥ�����˺���Һ�а�ˮ��̼����淋õ��������ٹ��ˡ�ϴ�ӡ���ɵõ�̼��þ���룮
��1���������̷�����Ӧ��H2O2+2H++2Fe2+�T2Fe3++2H2O��
��2��������pH��Ŀ����ʹFe3+���������������������������ȥ���Ҿ�������Mg2+ת��Ϊ������
��3��̼��þ�������ḽ�������ӵȣ���������������Һ�������ϴ��Һ���Ƿ����������ж��Ƿ�ϴ�Ӹɾ���
��4��ͨ������������Ӧ��Cl2-+2Fe2+�T2Fe3++2Cl-��������Ũ�ȱ仯��������Һ����������Ũ�ȣ�
������NaOH��Һ�õ��ij���ϴ�ӡ����գ����յõ�Fe2O3������Feԭ���غ����n��Fe3+��������������Һ�е�Fe3+��Ũ�ȣ�
��� �⣺ԭ��ˮ������������⣬��������������Ϊ�����ӣ��ٵ���pH��ʹ������ת��Ϊ������������ȥ�����˺���Һ�а�ˮ��̼����淋õ��������ٹ��ˡ�ϴ�ӡ���ɵõ�̼��þ���룮
��1���������̷�����Ӧ��H2O2+2H++2Fe2+�T2Fe3++2H2O���õ����ű������ת�Ƶķ������ĿΪ��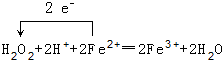 ��
��
�ʴ�Ϊ��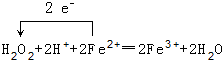 ��
��
��2��������pH��Ŀ����ʹFe3+����������������������������ȥ���Ҿ�������Mg2+ת��Ϊ���������ݸ���������������ɵ�pH�������ȫ��pH����֪Ӧ����pH��3.7��9.9֮�䣬��������Ҫ�ɷ�ΪFe��OH��3��
�ʴ�Ϊ��3.7��9.9֮�䣻Fe��OH��3��
��3��̼��þ�������ḽ�������ӵȣ�ȡ���һ��ϴ��Һ�����������ữ���ټ�����������Һ��û�а�ɫ�������ɣ�˵��ϴ�Ӹɾ���
�ʴ�Ϊ��ȡ���һ��ϴ��Һ�����������ữ���ټ�����������Һ��û�а�ɫ�������ɣ�˵��ϴ�Ӹɾ���
��4��ͨ������������Ӧ��Cl2-+2Fe2+�T2Fe3++2Cl-�����ݷ���ʽ��֪��������Ũ�ȱ仯��������Һ����������Ũ�ȣ�����Һ��c��Fe2+��=��c��Cl-��=0.460mol/L-0.455mol/L=0.005mol/L��
������NaOH��Һ�õ��ij���ϴ�ӡ����գ����յõ�MgO��Fe2O3���������ʵ����ֱ�Ϊxmol��ymol�����ݵ���غ���2x+6y=0.0460mol������������40x+160y=0.96������x=0.04mol��y=0.001mol�����Ը���Feԭ���غ�n��Fe3+��=0.001mol��2-0.005mol/L��0.1L=0.0015mol������Һ�е�Fe3+��Ũ��Ϊ0.015mol/L��
��ˮ������Һ��Fe2+��Ũ��Ϊ0.005mol/L��Fe3+�����ʵ���Ũ��Ϊ0.015mol/L��
���� ���⿼��ѧ���Թ������̵����⡢������ԭ��Ӧ���������Ŀ���ѡ��������ȣ����������ԭ���ǽ���Ĺؼ����Ƕ�ѧ���ۺ������Ŀ��飬��Ҫѧ���߱���ʵ�Ļ��������������������Ŀ�Ѷ��еȣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | NA��OH- | B�� | 3NA������ | C�� | 2NAԭ�� | D�� | 10NA������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
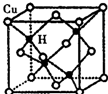 ͭ�ǵ�����������Ҫ�Ĺ���Ԫ��֮һ���䵥�ʼ���������й㷺��;��CuH�ľ���ṹ��ͼ��ʾ����CuH���ܶ�Ϊd g•cm-3�������ӵ�������ֵΪNA����þ����ı߳�Ϊ$\root{3}{\frac{260}{d{N}_{A}}}$cm���ú�d��NA��ʽ�ӱ�ʾ����
ͭ�ǵ�����������Ҫ�Ĺ���Ԫ��֮һ���䵥�ʼ���������й㷺��;��CuH�ľ���ṹ��ͼ��ʾ����CuH���ܶ�Ϊd g•cm-3�������ӵ�������ֵΪNA����þ����ı߳�Ϊ$\root{3}{\frac{260}{d{N}_{A}}}$cm���ú�d��NA��ʽ�ӱ�ʾ�����鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �Ҵ�������ˮ | B�� | ��ϩ��ʹ����KMnO4��Һ��ɫ | ||
| C�� | ��������Ա�̼���� | D�� | ��������ȡ��ˮ�еĵⵥ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��֪0.1 mol•L-1�Ĵ�����Һ�д��ڵ���ƽ�⣺CH3COOH?CH3COO-+H+���������ռ���Һ��ʹ��Һ��c��H+��/c��CH3COOH��ֵ���� | |
| B�� | 25��ʱ����ˮ�м�����������CH3COONa��ˮ�ĵ���ƽ�⣺H2O?H++OH-�����ƶ���c��H+������ | |
| C�� | ȡc��H+��=0.01mol/L������ʹ����100mL���ֱ�ϡ��2�����ٷֱ���� 0.03gп�ۣ�����ͬ�����³�ַ�Ӧ��������п��Ӧ�����ʴ� | |
| D�� | �����£���pH=11��Ba��OH��2��Һ��ˮϡ��10������Һ��pH=12 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
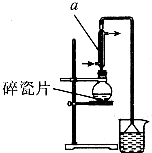 ������±�ᷴӦ���Ʊ�±��������Ҫ������ʵ�����Ʊ�1һ�嶡��ķ�Ӧ��ʵ��װ�����£�
������±�ᷴӦ���Ʊ�±��������Ҫ������ʵ�����Ʊ�1һ�嶡��ķ�Ӧ��ʵ��װ�����£�| �۵�/�� | �е�/�� | �ܶ�/g•cm-3 | |
| ������ | -89.53 | 117.25 | 0.81 |
| 1-�嶡�� | -112.4 | 101.6 | 1.28 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �����������£�SO2����100%��ת��ΪSO3 | |
| B�� | ʹ�ô�����Ϊ�˼ӿ췴Ӧ���ʣ��������Ч�� | |
| C�� | �ﵽƽ��ʱ��SO2��SO3��Ũ�ȱ��ֲ��� | |
| D�� | Ϊ�����SO2��ת���ʣ������ʵ����O2��Ũ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
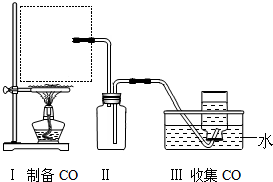
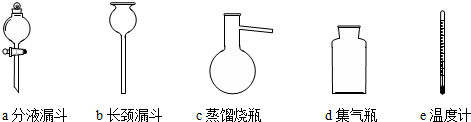

�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com