
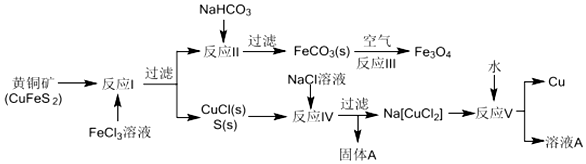
分析 根据流程:黄铜矿CuFeS2与FeCl3发生反应Ⅰ:CuFeS2+3FeCl3=CuCl↓+4FeCl2+2S↓,过滤,
滤液为氯化亚铁,与NaHCO3发生反应Ⅱ生成FeCO3,过滤,向FeCO3中通入空气生成四氧化三铁,
滤渣为S、CuCl,与NaCl溶液发生反应Ⅳ:CuCl+NaCl=Na[CuCl2],S不溶,过滤得到Na[CuCl2]溶液,固体为S,向滤液中加入水,Cu+ 在反应V中发生自身氧化还原反应,歧化为Cu2+和Cu,溶液A含有CuCl2、NaCl,据此分析可得.
解答 解:(1)黄铜矿CuFeS2中铁元素显+2价,S元素显-2价,故铜元素显+2;65gFeC13的物质的量为$\frac{65g}{162.5g/mol}$=0.4mol,三价铁还原为二价铁得电子0.4mol,CuFeS2中硫元素化合价由-2价升高到0价,共升高4价,硫元素被氧化,失去0.4mol电子时CuFeS2为0.1mol;
故答案为:+2;0.1;
(2)沉淀的颗粒较大,静止后容易沉降至容器底部,常用倾析法分离.沉淀呈胶状或絮状,静止后不容易沉降,不能采取倾析法分离;
故答案为:AB;
(3)己知FeCO3的Ksp=3.0×10-11,NaHCO3饱和溶液(其中CO32-平衡浓度为1.2×10-3mol/L)可产生FeCO3沉淀时的最小Fe2+浓度是$\frac{3.0×1{0}^{-11}}{1.2×1{0}^{-3}}$mol/L=2.5×10-8mol/L;
故答案为:2.5×10-8mol/L;
(4)高温氧化锻烧法来制备磁性氧化铁,化学方程式为:6FeCO3+O2$\frac{\underline{\;高温\;}}{\;}$2Fe2O3+6CO2;
故答案为:6FeCO3+O2$\frac{\underline{\;高温\;}}{\;}$2Fe2O3+6CO2;
(5)滤渣为S、CuCl,与NaCl溶液发生反应Ⅳ:CuCl+NaCl=Na[CuCl2],S不溶,过滤得到Na[CuCl2]溶液,固体为S;
故答案为:硫;
(6)潮湿的FeCO3固体若不及时灼烧处理会在空气中逐渐变红,二价铁被氧化为三价铁并水解生成红褐色的氢氧化铁,化学方程式为:6FeCO3+O2+6H2O═4Fe(OH)3+4CO2;
故答案为:6FeCO3+O2+6H2O═4Fe(OH)3+4CO2;
(7)反应Ⅳ使用氯化钠溶液,反应Ⅴ生成的溶液A含有CuCl2、NaCl,氯化钠可循环使用;
故答案为:氯化钠.
点评 本题以实际化工生产“黄铜矿的综合利用”为背景,考查了元素化合物知识,离子方程式和化学方程式的书写,题目更注重考查学生利用化学原理来解决实际问题的能力.


 同步轻松练习系列答案
同步轻松练习系列答案 课课通课程标准思维方法与能力训练系列答案
课课通课程标准思维方法与能力训练系列答案科目:高中化学 来源: 题型:选择题
| A. | 芒硝晶体(Na2SO4•10H2O)白天在阳光下曝晒后失水、溶解吸热,夜里重新结晶放热,实现了太阳能转化为化学能继而转化为热能 | |
| B. | 将植物的秸秆、枝叶、杂草和人畜粪便加入沼气发酵池中,在富氧条件下,经过缓慢、复杂、充分的氧化反应最终生成沼气,从而有效利用生物质能 | |
| C. | 生活、生成中大量应用氢能源,首先要解决由水制备氢气的能耗、氢气的储存和运输等问题 | |
| D. | 垃圾焚烧处理厂把大量生活垃圾中的生物质能转化为热能、电能,减轻了垃圾给城市造成的压力,改善了城市的环境,增强了市民的环保意识 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 试剂 | 成分 | 价格/(元•吨-1) |
| 漂液 | 含25.2% NaClO | 450 |
| 双氧水 | 含30% H2O2 | 2400 |
| 浓硝酸 | 含98% HNO3 | 1500 |
| 氢氧化物 | 开始沉淀的pH | 沉淀完全的pH |
| Fe(OH)2 | 7.6 | 9.6 |
| Fe(OH)3 | 2.7 | 3.7 |
| Cu(OH)2 | 4.0 | 6.5 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向含有FeI2的溶液中通入适量氯气,当有1mo1Fe2+被氧化时,该反应转移电子数目为3NA | |
| B. | 40gCuO和Cu2S混合物中所含铜原子的数目不等于0.5NA | |
| C. | 含0.1mo1NH4HSO4的溶液中,阳离子数目略小于0.2NA | |
| D. | C3H8分子中的2个H原子分别被1个-NH2和一个-OH取代,1mol此有机物所含共用电子对数目为13NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 物质 | FeS | MnS | HgS |
| 溶度积 | 5.0×l0-18 | 4.6×l0-14 | 2.2×l0-54 |
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Mn(OH)2 |
| 开始沉淀的pH | 2.7 | 7.6 | 8.3 |
| 完全沉淀的pH | 3.7 | 9.7 | 9.8 |
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | I2、Br2、Cl2 | B. | Na+、K+、Cs+ | C. | Cl-、Br-、I- | D. | Al3+、Mg2+、Na+ |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
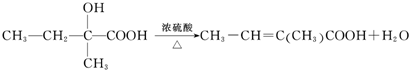 .
.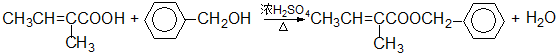 .
.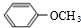 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com