
| A. | 间二甲苯的二氯代物有5种 | |
| B. | 二氯甲烷有2种同分异构体 | |
| C. | 丙烯分子中所有的原子有可能在同一平面上 | |
| D. | 用-C4H9取代苯环上的1个氢原子,最多可得4种同分异构体 |
分析 A.先确定一个氯原子的位置再确定另一个氯原子的位置;
B.二氯代物的同分异构体等于一氯代物中氢原子的种类;
C.根据乙烯的平面结构以及甲烷的四面体结构;
D.根据-C4H9异构体数目分析.
解答 解:A.一个氯原子在其中的一个甲基上,另一个氯原子的位置有5种,苯环上有4种,甲基上一种;两个氯原子也可以在同一个甲基上,故A错误;
B.一氯甲烷中只有1种氢原子,所以二氯甲烷只有一种结构,故B错误;
C.CH2=CHCH3中存在甲基,具有甲烷的结构,所以原子不可能处于同一平面内,故C错误;
D.若苯中氢原子被-C4H9取代苯环上的一个H原子,丁基有4种,则得到4种异构体,故D正确;
故选D.
点评 本题考查了同分异构体的判断及常见有机物的结构,中等难度,注意等效氢的判断.


科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | c(NH4+)>c(Cl-),c(OH-)>c(H+) | B. | c(Cl-)>c(NH4+),c(OH-)>c(H+) | ||
| C. | c(Cl-)>c(NH4+),c(H+)>c(OH-) | D. | c(NH4+)=c(Cl-),c(OH-)=c(H+) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 逆反应速率增大更大,平衡向逆反应方向移动 | |
| B. | 正反应速率增大更大,平衡向正反应方向移动 | |
| C. | 正反应速率减小,逆反应速率增大,平衡向逆反应方向移动 | |
| D. | 正反应速率增大,逆反应速率减小,平衡向正反应方向移动 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分子内共价键越强,分子越稳定,其熔沸点也越高 | |
| B. | C、H、O、N四种元素组成的化合物一定是离子化合物 | |
| C. | HF分子间存在着氢键,所以HF比HCl稳定 | |
| D. | 由原子构成的晶体可能是原子晶体,也可能是分子晶体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 物质发生化学反应时不一定都伴随着能量变化 | |
| B. | 伴有能量变化的变化都是化学变化 | |
| C. | 在一个确定的化学反应关系中,反应物的总能量总是高于生成物的总能量 | |
| D. | 在一个确定的化学反应关系中,反应物的总能量与生成物的总能量一定不同 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
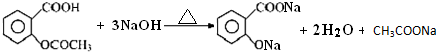
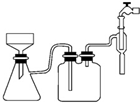 阿司匹林口服时,具有解热镇痛作用,是一种常用的治疗感冒的药物,也可用于抗风湿,促进痛风患者尿酸的排泄.近年来还发现阿司匹林能抑制血小板凝聚,可防止血栓的生成;它的有效成分是乙酰水杨酸(
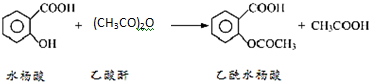
阿司匹林口服时,具有解热镇痛作用,是一种常用的治疗感冒的药物,也可用于抗风湿,促进痛风患者尿酸的排泄.近年来还发现阿司匹林能抑制血小板凝聚,可防止血栓的生成;它的有效成分是乙酰水杨酸(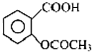 ).
).
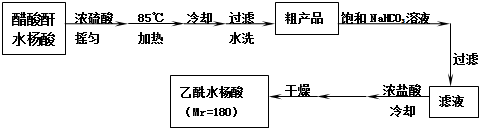
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
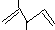 名称:2,3-二甲基-1,5-戊二烯 ②乙烯的实验式;CH2
名称:2,3-二甲基-1,5-戊二烯 ②乙烯的实验式;CH2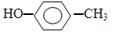
| A. | 2个 | B. | 3个 | C. | 4个 | D. | 5个 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com