
在体积为2 L的密闭容器中,进行如下化学反应:
CO2(g)+H2(g) CO(g)+H2O(g) △H=Q,化学平衡常数K与温度T的关系如下表:
CO(g)+H2O(g) △H=Q,化学平衡常数K与温度T的关系如下表:
| T/℃ | 700 | 800 | 850 | 1 000 | 1 200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
回答下列问题:
(1)Q____0(填 “>”、“<”),升高温度,化学平衡向________(填“正反应”或“逆反应”)方向移动。
(2)若某温度下,平衡浓度符合下列关系:c(CO2)·c(H2)=c(CO)·c(H2O),此时的温度为__________;在此温度下,若该容器中含有1mol CO2、3mol H2、2mol CO、2mol H2O,则此时反应所处的状态为____________(填“向正反应方向进行中”、“向逆反应方向进行中”或“平衡状态”),此温度平衡时CO2的浓度为___________ mol·L-1;在此温度下,若该容器中含有1.5mol CO2、3.5mol H2、1.5mol CO、1.5mol H2O达到平衡时CO2的浓度为___________ mol·L-1。
 手拉手全优练考卷系列答案
手拉手全优练考卷系列答案科目:高中化学 来源: 题型:
下列叙述正确的是( )
A.高温下二氧化硅与碳酸钠反应放出二氧化碳,说明硅酸(H2SiO3)的酸性比碳酸强
B.陶瓷、玻璃、水泥容器都能贮存氢氟酸
C.石灰抹墙、水泥砌墙的硬化过程原理相同
D.玻璃熔炉中出来的气体的主要成分是二氧化碳
查看答案和解析>>
科目:高中化学 来源: 题型:
下图所示的是一些常见的单质、化合物之间的转化关系图,有些反应中的部分物质和反应条件被略去。常温常压下,A是红棕色金属氧化物,B、D和L都是生产生活中常见的金属单质,B元素是地壳中含量最多的金属元素,F和J为常见的非金属元素的气体单质,且F呈无色、J呈黄绿色,L单质呈紫红色,E和M都是典型的两性化合物;C是氯碱工业的主要产品之一,俗名烧碱;C与K在溶液中反应时有红褐色沉淀生成。
(1)A的化学式为 ▲ 。
(2)H的电子式为 ▲ 。
(3)反应①的化学方程式为 ▲ 。
(4)反应②的离子方程式为 ▲ 。
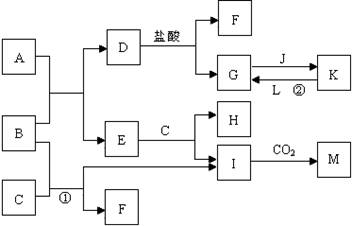
查看答案和解析>>
科目:高中化学 来源: 题型:
在一定条件下发生反应:2A(g)+2B(g)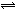 xC(g)+2D(g),在2L密闭容器中,把4molA和2molB混合,2min后达到平衡时生成1.6molC,又测得反应速率VD=0.2mol/(L·min),下列说法正确的是:
xC(g)+2D(g),在2L密闭容器中,把4molA和2molB混合,2min后达到平衡时生成1.6molC,又测得反应速率VD=0.2mol/(L·min),下列说法正确的是:
A.A和B的转化率均是20%; B.x = 4;
C.平衡时A的物质的量为2.8mol; D.平衡时气体压强比原来减小。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述不正确的是
A.根据某元素原子的质子数和中子数,可以确定该元素的相对原子质量
B.CaCl2、MgCl2晶体都容易潮解,它们潮解的实质是晶体表面吸水形成溶液
C.根据金属活动性顺序表,可以推断冶炼金属时可能的方法
D.根据酸、碱、盐的溶解性表,可以判断某些溶液中的复分解反应能否进行
查看答案和解析>>
科目:高中化学 来源: 题型:
下列依据热化学方程式得出的结论正确的是
A.已知:C(石墨,s)==C(金刚石,s) 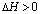 ,则金刚石比石墨稳定
,则金刚石比石墨稳定
B.已知:2H2(g)+O2(g)==2H2O(g)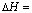 -483.6kJ·mol-1,则氢气的燃烧热为241.8kJ·mol-1
-483.6kJ·mol-1,则氢气的燃烧热为241.8kJ·mol-1
C. 已知:500℃、30MPa下,N2(g)+3H2(g)  2NH3 (g)
2NH3 (g) 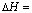 -38.6kJ·mol-1;将1.5molH2和过量的N2在此条件下充分反应,放出热量19.3kJ
-38.6kJ·mol-1;将1.5molH2和过量的N2在此条件下充分反应,放出热量19.3kJ
D. 已知: H2(g)+F2(g)== 2HF(g) 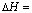 -270kJ·mol-1,则相同条件下,2molHF气体的能量小于1mol氢气和1mol氟气的能量之和
-270kJ·mol-1,则相同条件下,2molHF气体的能量小于1mol氢气和1mol氟气的能量之和
查看答案和解析>>
科目:高中化学 来源: 题型:
为探究氯水中含有的部分粒子及某些粒子的性质,某化学兴趣小组做了如下实验:
(1)观察氯水颜色,发现氯水呈黄绿色,说明氯水中含有的粒子是________;
(2)向氯水中滴入碳酸钠溶液,有气体生成,说明氯水中含有的粒子是________;
(3)在盛有氯水的试管中放入的有色布条退色,说明氯水中含有的粒子是________;
(4)写出氯气与水反应的化学方程式:_____________________________________;
(5)写出氯气与金属铁反应的化学方程式:_________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法中不正确的是( )
A.HF稳定性比HCl强 B.Mg失电子能力比Ca弱
C.NaCl与NH4Cl含有的化学键类型相同 D.等物质的量的C2H6和H202含电子数相同
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com