
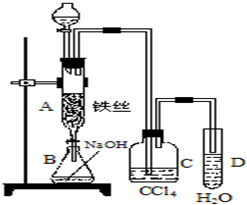
 ij��ѧ����С������ͼװ����ȡ�屽�������Һ©���м��뱽��Һ�壬�ٽ����Һ�������뷴Ӧ��A��A�¶˻����رգ��У�
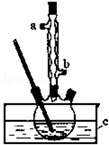
ij��ѧ����С������ͼװ����ȡ�屽�������Һ©���м��뱽��Һ�壬�ٽ����Һ�������뷴Ӧ��A��A�¶˻����رգ��У����� �����巴Ӧ�����廯�������廯���������£������巢��ȡ����Ӧ�����屽��HBr��Cװ�����ڳ�ȥ�壬D����HBr��Ϊ����HBr���ɼ�����������Һ����Ӧ������������������巴Ӧ���ɳ�ȥ�屽�е��壮
��1������Һ�����廯���������·���ȡ����Ӧ�����屽���廯�䣬�÷�Ӧ�Ƿ��ȷ�Ӧ�ҷ�Ӧ�������ӷ���
��2���嵥�������������Ʒ�Ӧ���屽���ܣ�
��3��CCl4 ���ܽ��岻���ܽ��廯�⣻
��4���������Һ�巢������ȡ����Ӧ������HBr���ɣ�����������Ǽӳɷ�Ӧ������HBr���ɣ������廯���˵������ȡ����Ӧ�������廯��ɼ�����Һ�е������ӻ���鷴Ӧ����Һ������ԣ�
��� �⣺��1���ڴ����������£������ϵ���ԭ�ӱ���ԭ����ȡ���������屽��ͬʱ���廯�����ɣ�������ӦΪC6H6+Br2$\stackrel{Fe}{��}$C6H5Br+HBr���÷�Ӧ�ų�����������ʹ��ӦҺ�У���ʹ��ӷ�����HBr�����л������������ʺ���ɫ��
�ʴ�Ϊ����ӦҺ�У��к���ɫ�������A������
��2���嵥����������������Һ��Ӧ���屽���ܣ����������������Һ���Գ�ȥ�屽�е��嵥�ʣ�����Br2+2NaOH�TNaBr+NaBrO+H2O��
�ʴ�Ϊ����ȥ�����屽�е��壻Br2+2NaOH�TNaBr+NaBrO+H2O��
��3��CCl4 ���ܽ��岻���ܽ��廯�⣬�������Ȼ�̼��ȥ�廯���е��壬�������ʵ������
�ʴ�Ϊ����ȥ�廯�������е���������
��4���������Һ�巢������ȡ����Ӧ������HBr���ɣ�����������Ǽӳɷ�Ӧ������HBr���ɣ�Ҳ����˵�����Ҫ֤������Һ�巢������ȡ����Ӧ�������Ǽӳɷ�Ӧ��ֻ���������HBr���ɣ������Թ�D�м���AgNO3��Һ������������ɫ����������֤������ȡ����Ӧ������H+�ķ���������ʯ����Һ�����������ȡ����Ӧ�������ӷ����廯�������е����������廯��ļ����и������ã���ˣ��ڼ����廯��ǰ�����ȥ����������Ҳ����C��ʢ�ŵ�CCl4�����ã�
�ʴ�Ϊ��ʯ����Һ����죮
���� ���⿼�鱽��ȡ����Ӧ����ʽ��ʵ�������Լ�����HBr�ļ��飬Ϊ��Ƶ���㣬������ѧ���ķ�����ʵ�������Ŀ��飬��Ŀ�Ѷ��еȣ�ע�����ձ���ȡ����Ӧԭ������ȷ��Ӧ�IJ��PHBr�Ļ�ѧ���ʽ��н��⣮



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 18gˮ���е�ԭ����ΪNA | |
| B�� | 4g�����Ʊ�ɸ�����ʱʧȥ�ĵ�����Ϊ0.1NA | |
| C�� | 1molO2����������1mol��ԭ�ӵ����� | |
| D�� | 24gO2��24gO3������ԭ����Ŀ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
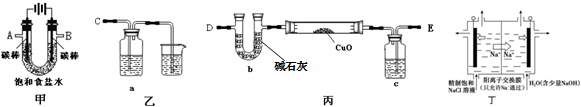
| ��� | A��Һ | B��Һ |
| �� | 2mL 0.2mol/L H2C2O4��Һ | 4mL 0.01mol/L KMnO4��Һ |
| �� | 2mL 0.1mol/L H2C2O4��Һ | 4mL 0.01mol/L KMnO4��Һ |
| �� | 2mL 0.2mol/L H2C2O4��Һ | 4mL 0.01mol/L KMnO4��Һ������MnSO4 |
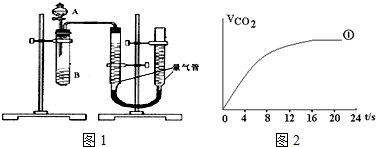
| ʵ���� | 1 | 2 | 3 | 4 |
| ˮ/mL | 10 | 5 | 0 | X |
| 0.5mol/L H2C2O4/mL | 5 | 10 | 10 | 5 |
| 0.2mol/L KMnO4/mL | 5 | 5 | 10 | 10 |
| ʱ��/s | 40 | 20 | 10 | --- |
| ʱ��/s | 0 | 5 | 10 | 15 | 20 | 25 | 30 |
| �¶�/�� | 25 | 26 | 26 | 26 | 26.5 | 27 | 27 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����

| A�� | ������Ҫ��Ӧ���Ȼ�ѧ����ʽ��S��s��+O2��g���TSO2��g����H=-297kJ•mol-1 | |
| B�� | ������Ҫ��Ӧ�Ļ�ѧ����ʽ��2SO2+O2$?_{��}^{����}$2SO3 | |
| C�� | ����ʹ�ô��������ѧ��Ӧ���ʺ�ƽ��ת���� | |
| D�� | ��������a ����ֱ���ŷŵ������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
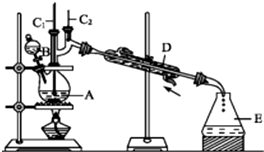
 �����ѣ�CH3CH2CH2CH2OCH2CH2CH2CH3����һ�ֻ���ԭ�ϣ�������Ϊ��ɫҺ�壬������ˮ���е�Ϊ142.4�棬�ܶȱ�ˮС��ijʵ��С����������װ�úϳ������ѣ�����װ�þ���ȥ������������Ҫ��ӦΪ��2C3CH2CH2CH2OH$��_{135��}^{ŨH_{2}SO_{4}}$CH3CH2CH2CH2OCH2CH2CH2CH3+H2O
�����ѣ�CH3CH2CH2CH2OCH2CH2CH2CH3����һ�ֻ���ԭ�ϣ�������Ϊ��ɫҺ�壬������ˮ���е�Ϊ142.4�棬�ܶȱ�ˮС��ijʵ��С����������װ�úϳ������ѣ�����װ�þ���ȥ������������Ҫ��ӦΪ��2C3CH2CH2CH2OH$��_{135��}^{ŨH_{2}SO_{4}}$CH3CH2CH2CH2OCH2CH2CH2CH3+H2O�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
 ����ȩ��һ�ֻ���ԭ�ϣ�
����ȩ��һ�ֻ���ԭ�ϣ�| �е�/�� | �ܶ�/��g•cm-3�� | ˮ���ܽ��� | |
| ������ | 117.2 | 0.810 9 | �� |
| ����ȩ | 75.7 | 0.801 7 | �� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com