
| �� | �� | �� | �� | ||
| �ܱ��������/L | 2 | 2 | 2 | 1 | |
| ��ʼ���ʵ��� | n��SO2��/mol | 0.4 | 0.8 | 0.8 | 0.4 |
| n��O2��/mol | 0.24 | 0.24 | 0.48 | 0.24 | |
| SO2��ƽ��ת����/% | 80 | a1 | a2 | a3 | |
| A�� | ���¶��£��÷�Ӧ��ƽ�ⳣ��KΪ400 | |
| B�� | SO2��ƽ��ת���ʣ�a1��a2=a3 | |
| C�� | �ﵽƽ��ʱ���������е�����Ӧ���ʱ��������еĴ� | |
| D�� | �ﵽƽ��ʱ����������c�� SO3��������������c�� SO3�������� |
���� A.2SO2+O2?2SO3��
��ʼ 0.2 0.12 0
ת�� 0.16 0.08 0.16
ƽ�� 0.04 0.04 0.16
KΪ������Ũ����֮���뷴Ӧ��Ũ����֮���ıȣ�
B���ҡ�����ȣ���������Ũ�ȴ��������Ũ����ͬ��
C�����������Ũ����ͬ��
D���ס�����ȣ�����Ũ��Ϊ��2����������ѹǿƽ�������ƶ���
��� �⣺A.2SO2+O2?2SO3��
��ʼ 0.2 0.12 0
ת�� 0.16 0.08 0.16
ƽ�� 0.04 0.04 0.16
K=$\frac{0.1{6}^{2}}{0.04��0.0{4}^{2}}$=400����A��ȷ��
B���ҡ�����ȣ���������Ũ�ȴ��������Ũ����ͬ����SO2��ƽ��ת���ʣ�a1��a2=a3����B����
C�����������Ũ����ͬ���¶���ͬ����ﵽƽ��ʱ���������е�����Ӧ���ʵ����������еģ���C����
D���ס�����ȣ�����Ũ��Ϊ��2����������ѹǿƽ�������ƶ�����ﵽƽ��ʱ����������c�� SO3��������������c�� SO3������������D��ȷ��
��ѡAD��
���� ���⿼�黯ѧƽ��ļ��㣬Ϊ��Ƶ���㣬����ƽ�����η���K�ļ��㡢ƽ���ƶ�Ϊ���Ĺؼ������ط�����Ӧ�������Ŀ��飬ע��ѡ��DΪ�����ѵ㣬��Ŀ�ѶȲ���


 53���ò�ϵ�д�
53���ò�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
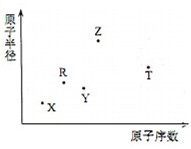 ����������Ԫ��X��Y��Z��R��T��ԭ�Ӱ뾶��ԭ��������ϵ��ͼ��ʾ��Rԭ�������������ǵ��Ӳ�����2����Y��Z���γ�Z2Y��Z2Y2�����ӻ����Z��T�γɵĻ�����Z2T�������ƶϴ�����ǣ�������
����������Ԫ��X��Y��Z��R��T��ԭ�Ӱ뾶��ԭ��������ϵ��ͼ��ʾ��Rԭ�������������ǵ��Ӳ�����2����Y��Z���γ�Z2Y��Z2Y2�����ӻ����Z��T�γɵĻ�����Z2T�������ƶϴ�����ǣ�������| A�� | �γɵļ����Ӱ뾶�Ĵ�С˳��ΪT��Y��Z | |
| B�� | Z2Y��Z2Y2�����еĻ�ѧ��������ͬ | |
| C�� | 0.005mol•L-1T������������Ӧˮ�����ˮ��ҺpH����2 | |
| D�� | Z2T��ˮ��Һ�Լ��ԣ���ˮ�ĵ����дٽ����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
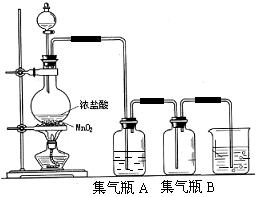 ʵ�������������������������з�����ȡ�ģ�4HCl��Ũ��+MnO2$\frac{\underline{\;\;��\;\;}}{\;}$Cl2��+MnCl2+2H2O
ʵ�������������������������з�����ȡ�ģ�4HCl��Ũ��+MnO2$\frac{\underline{\;\;��\;\;}}{\;}$Cl2��+MnCl2+2H2O�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 �ϲ��뺣�����ƣ���һ�ָ��������ĺ���ֲ���Ʒ�ϲ��ᱡ�ɴࡢ�Ⱥ������ױ����ճɻң���ʱ��ת��Ϊ�⻯�����Σ������ڵⵥ�ʵ���ȡ��
�ϲ��뺣�����ƣ���һ�ָ��������ĺ���ֲ���Ʒ�ϲ��ᱡ�ɴࡢ�Ⱥ������ױ����ճɻң���ʱ��ת��Ϊ�⻯�����Σ������ڵⵥ�ʵ���ȡ��| �Ҵ� | ���Ȼ�̼ | �⣨���壩 | |
| �ܶ�/g•cm-3 | 0.7893 | 1.595 | 4.94 |
| �е�/�� | 78.5 | 76.8 | 184.35 |
 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
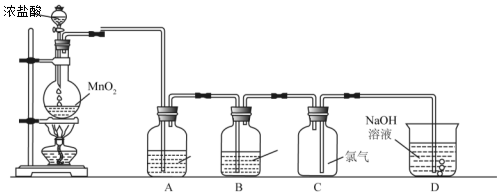
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
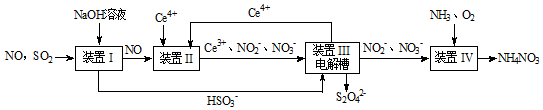
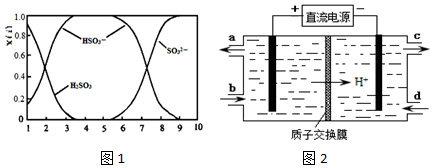
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 2������������4��-�ȴ��� | B�� | 3������������5��-�ȴ��� | ||
| C�� | 3������������9��-�ȴ��� | D�� | 4������������4��-�ȴ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
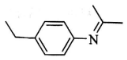 ���й㷺Ӧ�ã��ϳ�G��һ��·����ͼ��1H-NMR����ʾC�ṹ��ֻ��һ�ֻ������⣬�Ҳ��ܷ���������Ӧ��D�����ΪC8H10��
���й㷺Ӧ�ã��ϳ�G��һ��·����ͼ��1H-NMR����ʾC�ṹ��ֻ��һ�ֻ������⣬�Ҳ��ܷ���������Ӧ��D�����ΪC8H10��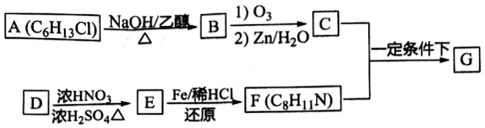
 $��_{��Zn/H_{2}O}^{��O_{3}}$R1CHO+
$��_{��Zn/H_{2}O}^{��O_{3}}$R1CHO+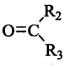
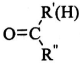 $\stackrel{һ������}{��}$
$\stackrel{һ������}{��}$ +H2O
+H2O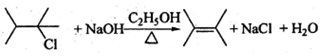 ��
�� ��
��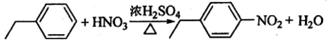 ��
��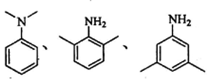 ��
��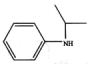 ���ĺϳ�·�ߣ�����ͼ��ʾ�����Լ���ѡ��
���ĺϳ�·�ߣ�����ͼ��ʾ�����Լ���ѡ��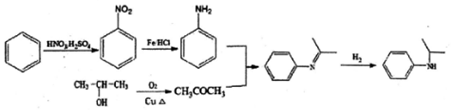 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| ���� | �����Լ� | ����� | װ�ã��ɼ��ȣ� | |
| A | O2 | ����غͶ������� | ��ˮ�Ȼ��� | 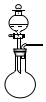 |
| B | NH3 | Ũ��ˮ����ʯ�� | ��ʯ�� | |
| C | H2 | ϡ�����п�� | Ũ���� | |
| D | SO2 | Ũ������������� | ��ʯ�� |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com