
| H2��g�� | N2��g�� | NH3��g�� | |
| 1mol�����еĻ�ѧ���γ�ʱҪ�ͷų�������/kJ | 436 | 946 | a |
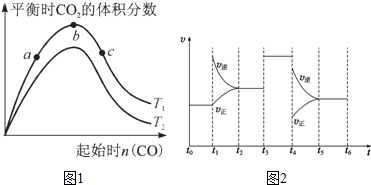
| A�� | 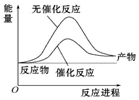 ��ͼ�ɱ�ʾ�ϳɰ������е������仯 | |
| B�� | a����ֵΪ391 | |
| C�� | Q1����ֵΪ92 | |
| D�� | ��ͬ�����£���Ӧ����Ϊ2 mol N2��6 mol H2���ų�����Q2��2Q1 |
���� A����Ӧ���ȣ���Ӧ���������������
B���ݡ�H=��Ӧ����ܺ�-��������ܺͼ��㣻
C���ϳɰ��ǿ��淴Ӧ��
D���ϳɰ�������Ӧ�����������С�ķ�Ӧ��1L�����У���Ӧ��Խ�෴Ӧ��ת����Խ�ߣ�
��� �⣺A����Ӧ�Ƿ��ȷ�Ӧ����Ӧ�����������������A����
B����H=��Ӧ����ܺ�-��������ܺͣ���-92KJ/mol=946KJ/mol+3��436KJ/mol-6aKJ/mol��a=360KJ/mol����B����
C���ϳɰ��ǿ��淴Ӧ��1molN2��3molH2������ȫת������C����
D���ϳɰ�������Ӧ�����������С�ķ�Ӧ��1L�����У���Ӧ��Խ�෴Ӧ��ת����Խ�ߣ�������ͬ�����£���Ӧ����Ϊ2molN2��6molH2���ų�����Q2��2Q1����D��ȷ��
��ѡ��D��
���� ���⿼���˷��ȷ�Ӧ��ͼ�����ü������㷴Ӧ�ȡ����淴Ӧ�ķ�Ӧ�ȵȵȣ���Ŀ�ѶȲ���



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��Һ������Һ | B�� | ��Һ��������ȡ | C�� | ����������ȡ | D�� | ����Һ����ȡ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ������������ | B�� | ��������Ƽ� | C�� | ���顢ҡͷ�� | D�� | ����ù�ء���Ŷ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �����ʯ��ˮ��ͨ������������̼��OH-+CO2�THCO3- | |
| B�� | ������Ͷ��ˮ�з�����Ӧ��O2-+H2O�T2OH- | |
| C�� | ��������Һ�м���ͭ�ۣ�Ag++Cu�TCu2++Ag | |
| D�� | ����������ϡ�����У�2Fe+6H+�T2Fe3++3H2�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 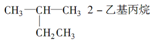 | B�� | CH3CH2CH2CH2OH 1-���� | ||
| C�� | 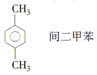 | D�� |  |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
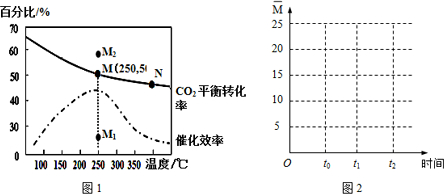
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com