
| A��X��Y�γɵĻ������п��ܺ���˫�� |
| B��X���ʺ�Z�����ڰ����ܾ��ҷ�Ӧ |
C��WԪ����ZԪ���γɵĻ������õ���ʽ��ʾ�γɹ���Ϊ��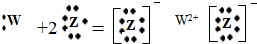 |
| D��XZ�ķе�����Zͬ�������X�Ļ���������� |
 ��ѡ����Ca�ĵ���ʽ��д����C����
��ѡ����Ca�ĵ���ʽ��д����C����

 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
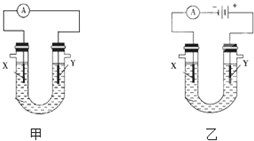
| A�������¶ȣ�������ɫ�����˷�ӦΪ���ȷ�Ӧ |
| B������ѹ�����������ƽ�������ƶ������������ɫ��dz |
| C������ѹ������������������Сһ�룬ѹǿ����С��ԭ�������� |
| D�����º���ʱ�����������������壬ѹǿ����ƽ�������ƶ�������������ɫ��dz |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����״���£�22.4L��H2O�к��еķ�����ΪNA |
| B�����³�ѹ�£�48g O3��O2��������к���ԭ����Ϊ3NA |
| C��12g Mg������ϡ���ᷴӦת�Ƶĵ�����Ϊ2NA |
| D��1L 1mol?L-1Na2CO3��Һ�к��е���������ΪNA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��1 | B��2 | C��3 | D��4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ѡ�� | ʵ����� | ���� | ���� |
| A | ��ij��Һ�м������� | ������ɫ���� | ��Һ��һ������CO32- |
| B | ����Fe��OH��2¶���ڿ�����һ��ʱ�� | ��ɫ����Ѹ�ٱ�Ϊ����ɫ�����ձ�Ϊ���ɫ | ˵��Fe��OH��2�ױ�������Fe��OH��3 |
| C | ��CuSO4��Һ�м���KI��Һ���ټ��뱽���� | �ϲ���Ϻ�ɫ���²��а�ɫ�������� | ͭ���ӿ������������ӣ���ɫ��������ΪCuI |
| D | ��ij��ɫ��Һ�еμ������ữ��BaCl2��Һ | ������ɫ���� | ��Һ��һ������SO42- |
| A��A | B��B | C��C | D��D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��78g������̼̼˫������ĿΪ3NA |
| B�����³�ѹ�£�22.4L������̼���е�ԭ������Ϊ3NA |
| C��1mol Fe������ϡHNO3��Ӧ��ת��3NA������ |
| D��1L 1mol?L-1��NaClO��Һ�к���ClO-����ĿΪNA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ���� | �����ᣨHCN�� | ̼�ᣨH2CO3�� | ����ᣨHF�� |
| ����ƽ�ⳣ��Kֵ | 6.2��10-10��K�� | 4.2��10-7��K1�� 5.6��10-11��K2�� |
6.61��10-4��K�� |
| A����������Һ��ͨ�����CO2 F-+H2O+CO2=HF+HCO3- |
| B��Na2CO3��Һ��2C��Na+��=C��CO32-��+C��HCO3-��+C��H2CO3�� |
| C���к͵��������pH�������ᣨHCN��������ᣨHF������NaOH����ǰ�ߴ��ں��� |
| D����Ũ�ȵ�NaCN��NaF��Һ��PHֵǰ��С�ں��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| �� |
| ���� |
| ʵ���� | �¶�/�� | ��ʼ��/mol | ƽ����/mol | �ﵽƽ������ʱ��/min | ||
| SO2 | O2 | SO2 | O2 | |||
| 1 | T1 | 4 | 2 | x | 0.8 | 6 |
| 2 | T2 | 4 | 2 | 0.4 | y | 9 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com