

分析 (1)非氧化还原反应即无元素化合价变化的反应;
(2)在反应①中,N2H4做还原剂,CuO做氧化剂,根据氧化剂与还原剂的物质的量之比为4:1,据此分析X;
(3)根据化学方程式来分析;
(4)温度高时氢氧化铜分解,且气体溶解度随温度升高而降低;
(5)在整个转化过程中满足铜元素的守恒.
解答 解:1)非氧化还原反应即无元素化合价变化的反应,反应②中铜元素、氮元素和氢元素以及氧元素的化合价均没有变化,故为非氧化还原反应,故答案为:②;
(2)在反应①中,N2H4做还原剂,CuO做氧化剂,则X为氧化产物,设X中氮元素为a价,则根据氧化剂与还原剂的物质的量之比为4:1有:4×(2-1)=1×2×(a-2+2),可解得a=0,即X为氮气,故答案为:N2;
(3)转化②中的离子方程式为:Cu2O+4NH3•H2O=2Cu(NH3)2++2OH-+3H2O,故溶液中氢氧根的物质的量增大,故答案为:增大;
(4)温度高时氢氧化铜分解,且气体溶解度随温度升高而降低,从而促进反应向正反应方向进行,
故答案为:氢氧化铜分解、降低联氨溶解度使其从溶液中逸出;
(5)在整个转化过程中满足铜元素的守恒,故若①中参加反应的CuO物质的量为0.4mol,按图示转化过程进行后,④中生成的CuO物质的量也等于0.4mol,故答案为:0.4mol.
点评 本题考查氧化还原反应、化学方程式计算等知识点,为高频考点,明确计量数与物质的量变化量关系是解(3)题关键,题目难度中等.


科目:高中化学 来源: 题型:选择题
 最近索尼公司演示了一种电池,可以采用碎纸运行,产生的废弃物就是水.该电池的电解质溶液中混合了水和酶,酶分解纸张会产生氢离子,氢离子与空气结合产生水,从而形成电流.其结构示意图如图所示,关于该电池的叙述正确的是( )
最近索尼公司演示了一种电池,可以采用碎纸运行,产生的废弃物就是水.该电池的电解质溶液中混合了水和酶,酶分解纸张会产生氢离子,氢离子与空气结合产生水,从而形成电流.其结构示意图如图所示,关于该电池的叙述正确的是( )| A. | 该电池属于燃料电池 | |
| B. | 该电池可在高温下使用 | |
| C. | a为该电池的负极 | |
| D. | b极附近的电极反应为:(C6H10O5)π+7nH2O+24ne-=6nCO2+24nH+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. |  用图装置除去Cl2中混有的少量HCl | |
| B. | 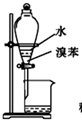 用图装置分离水和溴苯的混合物 | |
| C. |  用图装置制备并收集NO气体 | |
| D. |  用图装置蒸干AlCl3饱和溶液制备AlCl3晶体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 明矾可用作净水剂 | B. | 食醋可用于清除暖水瓶中的水垢 | ||
| C. | 氢氧化钠可用来治疗胃酸过多 | D. | 过氧化钠可用作潜艇里氧气来源 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 反应总体向左进行 | |
| B. | 反应达到平衡时,H2的物质的量分数<50% | |
| C. | 反应向某方向进行一段时间后K<57.0 | |
| D. | 反应达到平衡时,H2的转化率为75% |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③ | B. | ②①③ | C. | ③②① | D. | ③①② |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Cu(OH)2+2HNO3═Cu(NO3)2+2H2O | B. | Ba(OH)2+2HCl═BaCl2+2H2O | ||
| C. | 2NaOH+H2SO4═Na2SO4+2H2O | D. | KOH+HCl═KCl+H2O |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com