


科目:高中化学 来源: 题型:
| 砝码质量/g | 50 | 20 | 20 | 10 | 5 |
| 称量(取用砝码过程) |

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Zn+H2SO4═ZnSO4+H2↑ | ||||
B、2KClO3
| ||||
C、S+O2
| ||||
D、CH4+2O2
|
查看答案和解析>>
科目:高中化学 来源: 题型:
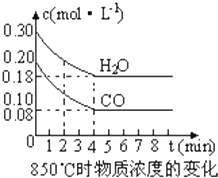 (1)化学平衡常数K表示可逆反应的进行程度,K值越大,表示
(1)化学平衡常数K表示可逆反应的进行程度,K值越大,表示| 时间(min) | CO | H2O | CO2 | H2 |
| 0 | 0.200 | 0.300 | 0 | 0 |
| 2 | 0.138 | 0.238 | 0.062 | 0.062 |
| 3 | c1 | c2 | c3 | c3 |
| 4 | c1 | c2 | c3 | c3 |
| 5 | 0.116 | 0.216 | 0.084 | |
| 6 | 0.096 | 0.266 | 0.104 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、NaHC03的电离:NaHC03?Na++H++C032- |
| B、HS-的水解:HS-+H20?H30++S2- |
| C、氢氧燃料电池在碱性介质中的负极反应式:02+2H20+4e-═40H- |
| D、用饱和Na2C03溶液处理重晶石:BaS04+C032-?BaC03+S042- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、使甲基橙呈红色的溶液:NH4+、Na+、Al02-、HC03- | ||
| B、c(NH3?H2O)=1.Omol?L-1的溶液:K+、Al3+、S042-、Cl- | ||
| C、由水电离的c(H+)=10-12mol?L-1的溶液:K+、Ba2+、Cl-、Br- | ||
D、在
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、c(NO3-)=1mol?L-1的溶液中:NH4+、Ba2+、Fe2+、Br- |
| B、水电离出c(OH-)=10-10mol?L-1的溶液:HCO3-、K+、Na+、Cl- |
| C、在pH=2的溶液中:NH4+、K+、ClO-、Cl- |
| D、c(Fe3+)=0.1mol?L-1的溶液中:K+、ClO-、SO42-、SCN- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、只有①②④ | B、①②③④ |
| C、只有①③④ | D、只有①②③ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com