
|
在溴水中加入或通入下列物质: ①镁粉 ②SO2 ③H2S ④活性炭 ⑤AgNO3溶液 ⑥NaHCO3溶液 ⑦NH3 ⑧KI能使溶液褪色的是 | |
| [ ] | |
A. |
全部 |
B. |
④⑧ |
C. |
除⑧外 |
D. |
②③④⑤ |
科目:高中化学 来源: 题型:
- 3 |
- 3 |
- 3 |
- 3 |

- 3 |
- 3 |
- 3 |
- 3 |
- 3 |
- 3 |
- 3 |
- 3 |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解

| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解


查看答案和解析>>
科目:高中化学 来源: 题型:
(2011?宝鸡一模)下表中实验操作能达到实验目的或得出正确结论的是( )
|
查看答案和解析>>
科目:高中化学 来源: 题型:

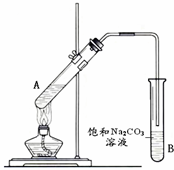
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com