
元素R的最高价含氧酸的化学式为H nRO2 n-2 ,则在气态氢化物中R元素的化合价为( )
A、12-3n B、3n-12 C、3n-10 D、6-3n
科目:高中化学 来源: 题型:
电炉加热时用纯O2氧化管内样品,根据产物的质量确定有机物的组成.下列装置是用燃烧法确定有机物分子式常用的装置。

(1)产生的O2按从左到右的流向,所选装置各导管的正确连接顺序是g→ → →h→i→ → → → 。
(2) 燃烧管中CuO的作用是______________________。
(3)若实验中所取样品只含C、H、O三种元素中的两种或三种,准确称取3.24 g 样品,经充分反应后,A管质量增加9.24g,B管质量增加2.16 g,则该样品的实验式为________。
(4)要确定该物质的分子式,还要知道该物质的_____________。经测定其蒸气密度为4.82g/L(已换算为标准状况下),则其分子式为________。
(5) 经红外光谱分析知该化合物的分子中存在1个苯环,苯环上只有1个支链,且支链中有1个甲基。试写出该有机物的结构简式 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列离子方程式不正确的是 ( )
A.溴乙烷在氢氧化钠水溶液中的反应:CH3CH2Br + OH-  CH3CH2OH +Br -
CH3CH2OH +Br -
B.醋酸溶液与氢氧化铜反应:2CH3COOH + Cu(OH)2 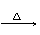 Cu2+ + 2CH3COO-+ 2H2O
Cu2+ + 2CH3COO-+ 2H2O
C.苯酚钠溶液中通入少量二氧化碳:2C6H5O-+ CO2 + H2O  2C6H5OH + CO32-
2C6H5OH + CO32-
D.甲醛溶液与足量的银氨溶液共热
HCHO+4[Ag(NH3)2]++4OH- 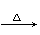 CO32-+2NH4+ +4Ag↓+6NH3+2H2O
CO32-+2NH4+ +4Ag↓+6NH3+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
桂醛在食品、医药、化工等方面都有应用。肉桂酸甲酯是常用于调制具有草莓、葡萄、樱桃、香子兰等香味的食用香精.
(1)肉桂醛由C、H、O三种元素组成,质谱分析肉桂醛分子的相对分子质量为132,其分子中碳元素的质量分数为81.8%,肉桂醛的分子式是 。
肉桂醛是苯的一取代物,核磁共振氢谱显示,苯环侧链上有三种不同化学环境的
氢原子,其结构简式是 。(不考虑顺反异构与对映异构)
(2)已知:
I.醛与醛能发生反应,原理如下:
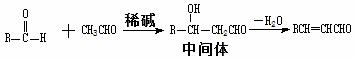
II.合成肉桂醛的工业流程如下图所示,其中甲为某种烃。

①甲的结构简式是 。
②丙和丁生成肉桂的化学方程式是 。
(3)肉桂醛能被银氨溶液氧化,再经酸化得到肉桂酸,写出肉桂酸甲酯的结构简式 。
(4)现用芳香烃A 为原料合成肉桂酸甲酯H的路线如下,测出A的核磁共振氢谱谱图有6个峰,其面积之比为1︰2︰2︰2︰1︰2。:

①化合物F中的官能团有 (填名称)。
②B→C的反应类型是 ,F→G的反应类型是 ,
③书写化学方程式
F→I
G→H
④G的同分异构体中,属于酯类目苯环上只有一个取代基的同分异构体有 种。
其结构简式分别是
查看答案和解析>>
科目:高中化学 来源: 题型:
人们应用原电池原理制作了多种电池,以满足不同的需要。以下每小题中的电池广泛使用于日常生活、生产和科学技术等方面,请根据题中提供的信息,填写空格。
(1)蓄电池在放电时起原电池作用,在充电时起电解池的作用。铅蓄电池在放电时发生的电池反应式为:Pb+PbO2+2H2SO4=2PbSO4+2H2O。
负极反应式为________________ 。 正极反应式为________________ 。
(2)铁、铜、铝是生活中使用广泛的金属,FeCl3溶液常用于腐蚀印刷电路铜板,其反应过程的离子方程式为________________ ,若将此反应设计成原电池,则负极所用电极材料为________________,正极反应式为________________。
(3)将铝片和铜片用导线相连,一组插入浓硝酸中,一组插入烧碱溶液中,分别形成了原电池,在这两个原电池中,负极分别为________________。
A.铝片、铜片 B.铜片、铝片 C.铝片、铝片 D.铜片、铜片
写出插入烧碱溶液中形成原电池的负极反应式:________________。
(4)燃料电池是一种高效、环境友好的供电装置,如图是甲烷燃料电池原理示意图,回答下列问题:

①电池的负极是__________(填“a”或“b”),该极的电极反应式是:________________。
②电池工作一段时间后电解质溶液的pH_________(填“增大”、“减小”或“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列对有机物结构或性质的描述中错误的是( )
A.一定条件下,Cl2可在甲苯的苯环或侧链上发生取代反应
B.乙烷和丙烯的物质的量共1mol,完成燃烧生成3molH2O
C.用核磁共振氢谱鉴别1—丙醇和2—丙醇
D.间二溴苯仅有一种空间结构可证明苯分子中不存在单双键交替的结构
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是
A.同温同压下,H2 (g)+Cl2(g)= 2HCl(g)在光照和点燃条件下的△H相同
B.任何酸与碱发生中和反应生成1 mol H2O的过程中,能量变化均相同
C.已知:①2H2(g) +O2(g) =2H2O(g) △H=-a kJ·mol-1,②2H2(g)+O2 (g)= 2H2O(1) △H=-b kJ·mol-1,则a>b
D.已知:①C(s,石墨)+O2 (g)=CO2(g) △H=- 393.5kJ·mol-1,②C(s,金刚石)+O2(g)=CO2 (g) △H=- 395.0 kJ·mol-1,则C(s,石墨)=C(s,金刚石) △H= -1.5 kJ·mol-1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com