
【题目】下列有关说法正确的是
A.反应![]() 在任何条件下都不会自发进行
在任何条件下都不会自发进行
B.溶液![]() 加水稀释后,溶液中
加水稀释后,溶液中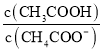 的值减小
的值减小
C.温度升高,反应物的活化分子数增多,主要因素是分子的运动加快,反应速率加快
D.![]() 液中加入少量
液中加入少量![]() 固体,
固体,![]() 水解程度减小,溶液的pH减小
水解程度减小,溶液的pH减小
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】PNA是一种具有良好的热稳定性、耐腐蚀性和抗水性的高分子化合物,常用作增塑剂,其合成路线如下图所示:
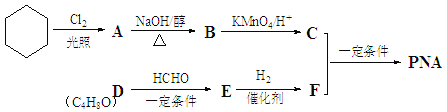
已知:
① R1CH=CHR2![]() R1COOH + R2COOH (R1、R2代表烃基)
R1COOH + R2COOH (R1、R2代表烃基)
②
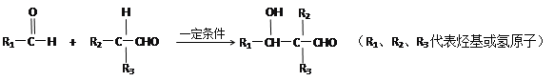
请回答:
(1)A分子中只有一个氯原子,A→B的化学方程式是 。
(2)C含有的官能团名称是 。
(3)D能发生银镜反应,且分子中有支链, D的结构简式是 。
(4)E→F的反应类型是 。
(5)E的结构简式是 。
(6)C与F在一定条件下生成增塑剂PNA的反应的化学方程式是: 。
(7)香豆素是一种重要的香料,与C具有相同的相对分子质量;14.6 g香豆素完全燃烧
生成39.6 g CO2和5.4 g H2O。
①香豆素的分子式是 。
②写出所有符合下列条件的香豆素的同分异构体的结构简式 。
a. 分子中含有![]() 基团
基团
b. 分子中除一个苯环外,无其他环状结构
c. 苯环上的氢原子被氯原子取代,得到两种一氯代物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“84”消毒液(工业利用Cl2与NaOH反应制得)可用于消毒和漂白,下列实验现象的分析不正确的是
实验操作 |
|
|
|
实验现象 | 混合后溶液的pH=9.9,短时间内未褪色,一段时间后蓝色褪去。 | 混合后溶液pH=5.0,蓝色迅速褪去,无气体产生。 | 混合后溶液pH=3.2,蓝色迅速褪去,并产生大量气体,使湿润的淀粉碘化钾试纸变蓝。 |
A.对比实验①和②,②中蓝色迅速褪去的原因是发生了反应ClO+H+═HClO
B.实验③中产生的气体是Cl2,由HClO分解得到:2HClO═Cl2↑+H2O
C.对比实验②和③,溶液的pH可能会影响ClO的氧化性或Cl的还原性
D.加酸可以提高“84”消毒液的漂白效果,但需要调控合适的pH才能安全使用
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质间反应的产物中一定不存在同分异构体的是
A. CH3-CH=CH2与HBr B. ![]() 与NaOH乙醇溶液共热
与NaOH乙醇溶液共热
C. CH3CH3与Cl2 D.  与NaHCO3溶液
与NaHCO3溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于 所具有性质说法不正确的是
所具有性质说法不正确的是
A.该有机物加入FeCl3溶液,显紫色
B.通常条件下,1mol该有机物与饱和溴水反应最多消耗2molBr2
C.通常条件下,1mol该有机物最多可与1molNaOH溶液反应
D.1mol该有机物最多可与4molH2反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定条件下,对于密闭容器中进行的反应:X(g) + Y(g)![]() 2Z(g),下列说法能充分说明该反应已达到化学平衡状态的是 ( )
2Z(g),下列说法能充分说明该反应已达到化学平衡状态的是 ( )
A.X、Y、Z的浓度相等B.正、逆反应速率均等于零
C.X、Y、Z在容器中共存D.X、Y、Z的浓度均不再改变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有平衡体系:CO(g)+2H2(g)![]() CH3OH(g) ΔH<0,为了增加甲醇的产量,应采取的压强措施是
CH3OH(g) ΔH<0,为了增加甲醇的产量,应采取的压强措施是
A.高温、高压B.适宜温度、高压、催化剂
C.低温、低压D.高温、高压、催化剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能量是一个世界性的话题,如何充分利用能量、开发新能源,为人类服务是广大科技工作者不懈努力的目标。
(1)如图所示,组成一个原电池:
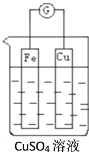
Cu电极是___(填“正”或“负”)极,其电极反应式为___;电子由___极流出。
(2)利用(1)图中的电极和电解液,在增加电源后可以实现电能转化为化学能,Fe接入电源负极,Cu接入电源正极,电解过程电极质量增加的是___(填“Fe”或“Cu”),Fe的腐蚀速度比正常在空气中的腐蚀速度___(填“快”或“慢”),溶液中c(Cu2+)___(填“增大”、“减小”或“不变”)。
(3)利用氢气与氧气的燃烧反应2H2(g)+O2(g)=2H2O(l) ΔH=-571.6kJ·mol-1,作为燃料电池的反应原理,可以提高能量的利用率,填充H2的电极是____(填“正”或“负”)极;当有11.2L(折算成标准状况下的体积)H2反应,会放出___kJ热量;如果2H2(g)+O2(g)=2H2O(g) ΔH=-a kJ·mol-1,则a___571.6(填“>”、“<”或“=”)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列热化学方程式中,正确的是( )
A.甲烷的燃烧热为 890.3 kJmolˉ1,则甲烷燃烧的热化学方程式可表示为:CH4(g)+2O2(g)=CO2(g)+2H2O(g);△H=+890.3 kJmolˉ1
B.稀盐酸和稀氢氧化钠溶液混合, 其热化学方程式为:H++OH-=H2O; △H =-57.3 kJmolˉ1
C.已知 H2 燃烧热为 142.9kJmolˉ1 ,则氢气燃烧的热化学方程式为:2H2(g)+O2(g)=2H2O(1);△H =-285.8 kJmolˉ1
D.500℃、30MPa 下,将 0.5mol N2 和 1.5molH2 置于密闭的容器中充分反应生成 NH3(g),放热 19.3kJ,其热化学方程式为:N2(g) + 3H2(g) ![]() 2NH3(g) ;△H=-38.6kJ· mol-1
2NH3(g) ;△H=-38.6kJ· mol-1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com