
科目:高中化学 来源:2015-2016学年贵州凯里一中高一下期中理科化学试卷(解析版) 题型:选择题
如图是氢氧燃料电池构造示意图。关于该电池的说法不正确的是( )
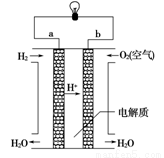
A.a极是负极
B.供电时的总反应为2H2+O2==2H2O
C.电子由b通过灯泡流向a
D.氢氧燃料电池是环保电池
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山西省高二5月月考理科化学试卷(解析版) 题型:选择题
关于同分异构体的下列说法中正确的是 ( )
A.结构不同,性质相异,化学式相同的物质互称同分异构体
B.同分异构体现象是导致有机物数目众多的重要原因之一
C.同分异构体现象只存在于有机化合物中
D.同分异构体现象只存在于无机化合物中
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山西大学附中高一下期中化学试卷(解析版) 题型:选择题
某主族元素R的最高正价与最低负化合价的代数和为4,由此可以判断
A.R气态氢化物化学式为H2R
B.R一定是Ⅵ族元素
C.R的气态氢化物比同周期其他元素气态氢化物稳定
D.R一定是第四周期元素
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山西大学附中高一下期中化学试卷(解析版) 题型:选择题
对于在一密闭容器中进行如下反应:C(s)+O2(g)=CO2(g)下列说法错误的是
A.将木炭粉碎成粉末状可以加快化学反应速率
B.升高温度可以加快化学反应速率
C.增加压强可以加快化学反应速率
D.增加木炭的物质的量可以加快化学反应速率
查看答案和解析>>
科目:高中化学 来源:2015-2016学年青海师大附二中高一下期中化学试卷(解析版) 题型:计算题
Fe3+具有较强的氧化性,可以将Cu氧化为Cu2+,即: 2Fe3+ + Cu = 2Fe2+ + Cu2+,请将该反应设计成原电池:①画出原电池的装置图;②标出正、负极和电解质溶液;③并写出电极反应式。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年青海师大附二中高一下期中化学试卷(解析版) 题型:选择题
原电池的电极名称不仅与电极材料的性质有关,也与电解质溶液有关。下列说法中正确的是
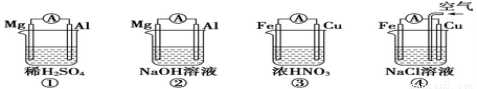
A.①②中Mg作负极,③④中Fe作负极
B.②中Mg作正极,电极反应式为:2H2O+2e-= 2OH-+H2↑
C.③中Fe作负极,电极反应式为Fe-2e-= Fe2+
D.④中Cu作正极,电极反应式为2H++2e-= H2↑
查看答案和解析>>
科目:高中化学 来源:2015-2016学年青海师大附二中高二下期中化学试卷(解析版) 题型:填空题
研究硫元素及其化合物的性质具有重要意义。
(1)①硫离子的结构示意图为 。
②加热时,硫元素的最高价氧化物对应水化物的浓溶液与木炭反应的化学方程式为 。
(2)25℃,在0.10mol·L-1H2S溶液中,通入HCl气体或加入NaOH固体以调节溶液pH,溶液pH与c(S2-)关系如图(忽略溶液体积的变化、H2S的挥发)。
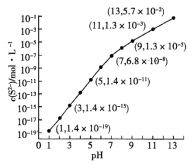
①pH=13时,溶液中的c(H2S)+c(HS-)= mol·L-1。
②某溶液含0.020 mol·L-1Mn2+、0.10 mol·L-1H2S,当溶液pH= 时,Mn2+开始沉淀。[已知:Ksp(MnS)=2.8×10-13]
(3)25℃,两种酸的电离平衡常数如下表。

①HSO3-的电离平衡常数表达式K= 。
②0.10 mol·L-1Na2SO3溶液中离子浓度由大到小的顺序为 。
③H2SO3溶液和NaHCO3溶液反应的主要离子方程式为 。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江苏省高二下期中化学试卷(解析版) 题型:填空题
已知:2NO2(g) N2O4(g) △ H<0。在恒温恒容条件下,将一定量NO2和N2O4的混合气体通入容积为2L的密闭容器中,反应过程中各物质的物质的量浓度c随时间t的变化关系如下图所示。
N2O4(g) △ H<0。在恒温恒容条件下,将一定量NO2和N2O4的混合气体通入容积为2L的密闭容器中,反应过程中各物质的物质的量浓度c随时间t的变化关系如下图所示。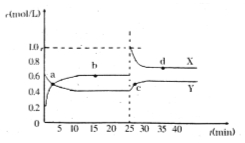
(1)a、b、c、d四个点中,化学反应处于平衡状态的是 点。
(2)b点平衡常数的表达式为 。
(3)b、d两点所表示的反应体系中,气体颜色由深的是 (填字母)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com