
| A. | 标准状况下,同体积的气体A和气体B的质量比m:n | |
| B. | 25℃,101KPa时,1Kg气体A与1Kg气体B的分子数比为n:m | |
| C. | 同温同压下,气体A与气体B密度比为n:m | |
| D. | 标准状况下,等质量的A与B的体积比为n:m |
分析 在同温同压下,气体摩尔体积相等,mg A气体与ng B气体的分子数相等,说明二者的物质的量相等,根据n=$\frac{m}{M}$知,A、B的摩尔质量之比=其质量之比=m:n,结合m=$\frac{V}{{V}_{m}}$M、N=$\frac{m}{M}$NA、ρ=$\frac{M}{{V}_{m}}$、V=$\frac{m}{M}$Vm进行计算和判断.
解答 解:在同温同压下,气体摩尔体积相等,mg A气体与ng B气体的分子数相等,说明二者的物质的量相等,根据n=$\frac{m}{M}$知,A、B的摩尔质量之比=其质量之比=m:n,
A.相同条件下,根据m=$\frac{V}{{V}_{m}}$M可知,气体体积相等时,气体的质量与摩尔质量成正比,所以A、B的质量之比=m:n,故A正确;
B.根据N=$\frac{m}{M}$NA可知,相同质量时气体分子数之比等于摩尔质量反比=n:m,故B正确;
C.根据ρ=$\frac{M}{{V}_{m}}$可知,气体摩尔体积相等时,气体的密度之比等于其摩尔质量之比=m:n,故C错误;
D.根据V=$\frac{m}{M}$Vm可知,相同条件下,质量相等时气体体积之比等于摩尔质量反比=n:m,故D正确;
故选C.
点评 本题考查阿伏伽德罗定律及其推论,题目难度中等,试题侧重考查公式灵活运用,明确物质的量公式中各个物理量的关系是解本题关键,试题培养了学生的分析能力及化学计算能力.


科目:高中化学 来源: 题型:选择题
| A. | 将碘水倒入分液漏斗,加适量乙醇,振荡后静置,可将碘萃取到乙醇中 | |
| B. | 某气体能使湿润的红色石蕊试纸变蓝,该气体水溶液一定显碱性 | |
| C. | 某无色溶液加Ba(NO3)2溶液,再加入稀盐酸,沉淀不溶解,则原溶液中一定有SO42- | |
| D. | 加入稀盐酸产生无色无味气体,将气体通入澄清石灰水中溶液变浑浊,一定有CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用加热、蒸发的方法除去粗盐中的CaCl2、MgCl2等杂质 | |
| B. | 用过滤的方法除去NaCl溶液中含有的少量淀粉胶体 | |
| C. | 用溶解、过滤的方法提纯含有少量BaSO4的BaCO3 | |
| D. | 用丁达尔现象区分溶液与胶体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 光照新制的氯水时,溶液黄绿色变浅 | |
| B. | 高温高压有利于N2和H2转化为NH3:N2(g)+3H2(g)?2NH3(g);△H<0) | |
| C. | 打开汽水瓶时,有大量气泡逸出 | |
| D. | 氨水应密闭保存于低温处 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 过滤 萃取 分液 | B. | 萃取 分液 蒸馏 | C. | 分液 蒸馏 萃取 | D. | 萃取 蒸馏 分液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温常压下,18.0 g NH4+中所含的质子数为10 NA | |
| B. | 室温下,8 g甲烷含有共价键数为2NA | |
| C. | 常温下,2.7 g铝片投入足量的浓硫酸中,铝失去的电子数为0.3NA | |
| D. | 常温下,1 mol/L 的 Na2SO4溶液中含有Na+个数为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 试剂 | 乙醚 | 乙醇 | 乙酸 | 乙酸乙酯 |
| 沸点/℃ | 34.7 | 78.5 | 118 | 77.1 |
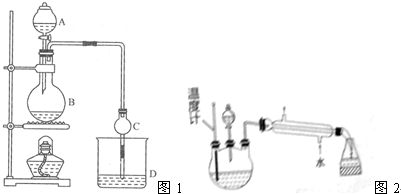
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
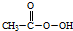 (过氧乙酸)+H2O
(过氧乙酸)+H2O查看答案和解析>>
科目:高中化学 来源: 题型:解答题
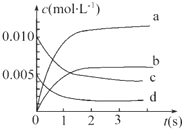 在2L密闭容器内,800℃时反应2NO(g)+O2(g)═2NO2(g)体系中,n(NO)随时间的变化如表:
在2L密闭容器内,800℃时反应2NO(g)+O2(g)═2NO2(g)体系中,n(NO)随时间的变化如表:| 时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)(mol) | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com