
| A. | 还原性:S2-<Cl-<F- | B. | 稳定性:HF>HCl>H2S | ||
| C. | 碱性:KOH<NaOH<Al(OH)3 | D. | 还原性:K>Na>Mg |
分析 A.非金属性越强,阴离子的还原性越弱;
B.元素的非金属性越强,对应的氢化物越稳定;
C.金属性越强,对应的最高价氧化物的碱性越强;
D.元素的金属性越强,对应的反之的还原性越强.
解答 解:A.非金属性S<Cl<F,非金属性越强,阴离子的还原性越弱,应为S2->Cl->F-,故A错误;
B.非金属性S<Cl<F,元素的非金属性越强,对应的氢化物越稳定,故B正确;
C.金属性K>Na>Al,金属性越强,对应的最高价氧化物的碱性越强,故C错误;
D.金属性K>Na>Mg,元素的金属性越强,对应的反之的还原性越强,故D正确.
故选AC.
点评 本题考查学生元素周期律的应用知识,为高频考点,侧重于学生的分析能力的考查,可以根据周期表中同周期和同主族元素性质的递变规律回答,难度不大.


科目:高中化学 来源: 题型:解答题
| 配 料 | 氯化钠、碘酸钾 |
| 含碘量 | (20mg~40mg)/1kg |
| 保质期 | 18个月 |
| 食用方法 | 勿长时间炖炒 |
| 贮藏指南 | 避热、防潮 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
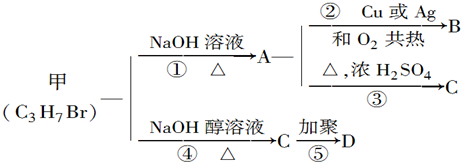
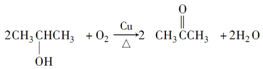

 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加入少量碳酸钠粉末 | B. | 加入少量硫酸铜溶液 | ||
| C. | 加入适量NaCl溶液 | D. | 加热 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 含有NA个氢原子的氢气在标准状况下的体积约为22.4L | |
| B. | 25℃,1.01×105 Pa,64g SO2中含有的原子数为3NA | |
| C. | 2.3g金属钠变为钠离子失去电子数为0.05NA | |
| D. | 标准状况下,11.2LH2O 含有的分子数为0.5NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 实验事实 | 理论解释 |
| A | N原子的第一电离能大于O原子 | N原子2p能级半充满 |
| B | CO2为直线形分子 | CO2分子中C=O之间的夹角为120° |
| C | 金刚石的熔点低于石墨 | 金刚石是原子晶体,石墨是原子晶体 |
| D | HF的沸点高于HCl | HF的相对分子质量小于HCl |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com