
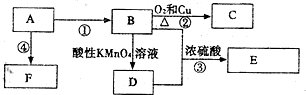
分析 A是来自石油的重要有机化工原料,F是一种高聚物,可制成食品包装材料,则A为乙烯,烯发生加聚反应生成F为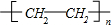 ,乙烯与水发生加成反应生成B为乙醇,乙醇发生催化氧化生成C为乙醛,乙醇被酸性高锰酸钾氧化生成D为乙酸,乙酸与乙醇发生酯化反应生成E为乙酸乙酯,据此解答.
,乙烯与水发生加成反应生成B为乙醇,乙醇发生催化氧化生成C为乙醛,乙醇被酸性高锰酸钾氧化生成D为乙酸,乙酸与乙醇发生酯化反应生成E为乙酸乙酯,据此解答.
解答 解:A是来自石油的重要有机化工原料,F是一种高聚物,可制成食品包装材料,则A为乙烯,烯发生加聚反应生成F为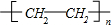 ,乙烯与水发生加成反应生成B为乙醇,乙醇发生催化氧化生成C为乙醛,乙醇被酸性高锰酸钾氧化生成D为乙酸,乙酸与乙醇发生酯化反应生成E为乙酸乙酯.
,乙烯与水发生加成反应生成B为乙醇,乙醇发生催化氧化生成C为乙醛,乙醇被酸性高锰酸钾氧化生成D为乙酸,乙酸与乙醇发生酯化反应生成E为乙酸乙酯.
(1)A为乙烯,含有碳碳双键,其结构简式为CH2=CH2,故答案为:CH2=CH2;
(2)D为乙酸,分子中的官能团是:羧基,故答案为:羧基;
(3)反应②是乙醇氧化生成乙醛,反应方程式为:2CH3CH2OH+O2$→_{△}^{Cu}$2CH3CHO+2H2O,故答案为:2CH3CH2OH+O2$→_{△}^{Cu}$2CH3CHO+2H2O.
点评 本题考查有机物推断,涉及烯烃、醇、醛、羧酸的性质与转化,比较基础,注意对基础知识的理解掌握.


 考前必练系列答案
考前必练系列答案科目:高中化学 来源: 题型:选择题
| A. | pH=3的醋酸溶液稀释100倍后,溶液的pH=5 | |
| B. | pH=2的盐酸与等体积0.01 mol?L-1醋酸钠混合溶液后,溶液中c(Cl-)=c(CH3COO-) | |
| C. | 氨水中通入过量CO2后,溶液中c(H+)+c(NH4+)=c(OH-)+c(HCO3-) | |
| D. | 0.1mol AgCl和0.1mol AgI混合后加入1L水中,所得溶液中c(Cl-)>c(I-) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 实验序号 | 1 | 2 | 3 | 4 |
| 消耗NaOH溶液的体积(mL) | 20.05 | 20.00 | 18.80 | 19.95 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 (R、R′、R〞表示氢、烷基或芳基)合成五元环有机化合物J 的路线如下:
(R、R′、R〞表示氢、烷基或芳基)合成五元环有机化合物J 的路线如下:
 ,它的分子子中有3种不同类型的官能团,它是J的同分异构体;
,它的分子子中有3种不同类型的官能团,它是J的同分异构体; ;
; +H2O;E的核磁共振氢谱中应该具有6组峰.
+H2O;E的核磁共振氢谱中应该具有6组峰. .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.| 碳酸盐 | MgCO3 | CaCO3 | BaCO3 | SrCO3 |
| 热分解温度/℃ | 402 | 900 | 1172 | 1360 |
| 阳离子半径/pm | 66 | 99 | 112 | 135 |
 是比C60约早20年合成出的一种对称型烃类分子,而现如今已合成出一种立方烷与C60的复合型分子晶体,该晶体的晶胞结构如图所示,立方烷分子填充在原C60晶体的分子间空隙中.则该复合型分子晶体的组成用二者的分子式可表示为C8H8.C60
是比C60约早20年合成出的一种对称型烃类分子,而现如今已合成出一种立方烷与C60的复合型分子晶体,该晶体的晶胞结构如图所示,立方烷分子填充在原C60晶体的分子间空隙中.则该复合型分子晶体的组成用二者的分子式可表示为C8H8.C60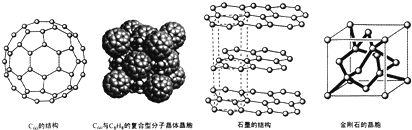
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 元素代号 | X | Y | Z | W | Q |
| 原子半径(nm) | 0.073 | 0.077 | 0.099 | 0.102 | 0.118 |
| 主要化合价 | -2 | +4、-4 | -1 | +6、-2 | +3 |
| A. | 单质沸点:W>Q>Z | |
| B. | X、Y、W三种元素两两之间均能以共价键形成AB2型的化合物 | |
| C. | Z的含氧酸的酸性一定大于W的含氧酸的酸性 | |
| D. | W与Q形成的常见化合物可以稳定存在于水溶液中 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Ca(HCO3)2溶液中加入少量NaOH溶液:Ca2++2HCO3-+2OH-═CaCO3↓+CO32-+H2O | |
| B. | 向次氯酸钙溶液通入SO2:Ca2++2C1O-+H2O+SO2═CaSO3↓+2HC1O | |
| C. | 氢氧化钙溶液气碳酸氢镁溶液反应:Ca2++OH-+HCO3 -═CaCO3↓+H2O | |
| D. | 硫酸亚铁的酸性溶液中加入H2O2溶液:Fe 2++H2O2+2H+═Fe 3++2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 将某有机物与溴的四氯化碳 溶液混合 | 溶液褪色 | 该有机物中必定含有 碳碳双键 |
| B | 向亚硫酸钠溶液中滴加硝酸 钡和稀硝酸 | 产生白色沉淀 | 亚硫酸钠溶液己变质 |
| C | 向酸性高锰酸钾溶液中滴加 双氧水 | 紫色褪去,产生气泡 | H202具有还原性 |
| D | 向油脂皂化反应后的溶液中 滴入酚酞 | 溶液不变红 | 油脂己经完全皂化 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
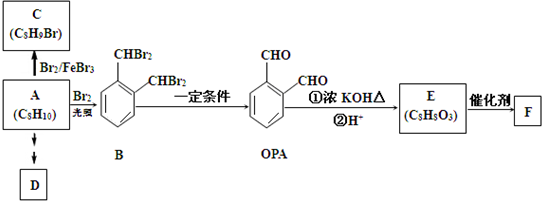

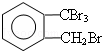 ;
; ;
; .
.
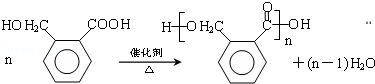 .
.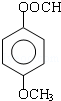 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com