
设NA表示阿伏加德罗常数的值。下列说法正确的是( )
A.一定条件下,0.2 mol SO2与足量O2充分反应,生成SO3分子数为0.2NA
B.0.1 mol —NH2(氨基)中含有的电子数为0.7NA
C.3.4 g H2O2中含有的共用电子对数为0.1NA
D.常温常压下,16 g O2和O3混合气体含有的氧原子数为NA
 举一反三期末百分冲刺卷系列答案
举一反三期末百分冲刺卷系列答案科目:高中化学 来源: 题型:
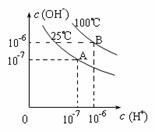
在不同温度下,水达到电离平衡时c(H+)与
c(OH—)的关系如右图所示,下列说法中正确的是
A、100℃时,pH=12的NaOH溶液和pH=2的H2SO4溶液恰好中和,
所得溶液的pH等于7
B、25℃时,0.2 mol/L Ba(OH)2溶液和0.2 mol/L HCl溶液等体积混合,
所得溶液的pH等于7
C、25℃时, 0.2 mol/L NaOH溶液与0.2 mol/L乙酸溶液恰好中和,所得溶液的pH等于7
D、25℃时,pH=12的氨水和pH=2的H2SO4溶液等体积混合,所得溶液pH大于7
查看答案和解析>>
科目:高中化学 来源: 题型:

观察1s轨道电子云示意图,判断下列说法正确的是( )
A.一个小黑点表示1个自由运动的电子
B.1s轨道的电子云形状为圆形的面
C.电子在1s轨道上运动像地球围绕太阳旋转
D.1s轨道电子云中点的疏密表示电子在某一位置出现机会的多少
查看答案和解析>>
科目:高中化学 来源: 题型:
普通泡沫灭火器的铁筒里装着一只小玻璃筒,玻璃筒内盛装硫酸铝溶液,铁筒里盛装碳酸氢钠饱和溶液。使用时,倒置灭水器,两种药液相混合就会喷出含二氧化碳的白色泡沫。
(1)产生此现象的化学方程式是
________________________________________________________________________
________________________________________________________________________。
不能把硫酸铝溶液装在铁筒里的主要原因是
________________________________________________________________________
________________________________________________________________________
________________________________________________________________________。
一般不用碳酸钠代替碳酸氢钠,是因为
________________________________________________________________________
________________________________________________________________________
________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下面的问题中,与盐类水解有关的是( )
①为保存FeCl3溶液,要在溶液中加入少量盐酸;
②实验室盛放Na2CO3、Na2SiO3等溶液的试剂瓶应用橡胶塞;
③在NH4Cl或AlCl3溶液中加入镁条会产生气泡;
④长期使用硫酸铵,土壤酸性增强。
A.只有①④ B.只有②③ C.只有③④ D.全部
查看答案和解析>>
科目:高中化学 来源: 题型:
用NA表示阿伏加德罗常数的值。下列叙述正确的是( )
A.在H2O2+Cl2===2HCl+O2反应中,每生成32 g氧气,则转移4NA个电子
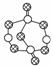
B.17.4 g某硫化磷(如图)中含P—S键数目为0.6NA
C.1 mol含8个碳原子的某烃分子,最多形成7 mol碳碳单键
D.标准状况下,22.4 L SO2与O2混合气体,含有2NA个氧原子
查看答案和解析>>
科目:高中化学 来源: 题型:
在一密闭容器中加入A和B,各物质的物质的量浓度随着反
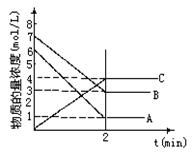
 应的进行,如右图所示。下列说法不正确的是
应的进行,如右图所示。下列说法不正确的是
A.该反应的化学方程式为5A+4B 4C
B.2min时,该反应达到平衡,此时A、B、C的浓度
比为5:4:4
C.用B的浓度变化表示2min内的速率为
2mol/(L·min)
D.2min前,正反应速率逐渐减小,逆反应速率逐渐增大
查看答案和解析>>
科目:高中化学 来源: 题型:
盖斯定律在生产和科学研究中有很重要的意义。有些反应的反应热虽然无法直接测得,但可通过间接的方法测定。现根据下列3个热化学反应方程式:
①Fe2O3(s)+3CO(g)== 2Fe(s)+3CO2(g) △H= ―24.8kJ/mol
②3Fe2O3(s)+ CO(g)==2Fe3O4(s)+ CO2(g) △H= ―47.2kJ/mol
③Fe3O4(s)+CO(g)==3FeO(s)+ CO2(g) △H= +640.5kJ/mol
写出CO气体还原FeO固体得到Fe固体和CO2气体的热化学反应方程式:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com