
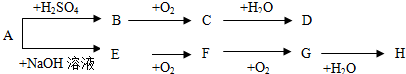
分析 B是能使品红溶液褪色的气体,B是SO2,E是碱性气体,E和氧气反应生成F,F和氧气反应生成G,G是红棕色气体,则G是NO2,E是NH3,F是NO,H为HNO3.A为正盐,与H2SO4反应生成SO2,那么A中含有SO32-,且与NaOH反应生成NH3,则A是(NH4)2SO3,B是SO2,C是SO3,D是H2SO4.
解答 解:B是能使品红溶液褪色的气体,B是SO2,E是碱性气体,E和氧气反应生成F,F和氧气反应生成G,G是红棕色气体,则G是NO2,E是NH3,F是NO,H为HNO3.A为正盐,与H2SO4反应生成SO2,那么A中含有SO32-,且与NaOH反应生成NH3,则A是(NH4)2SO3,B是SO2,C是SO3,D是H2SO4.
(1)由上述分析可知,B是SO2,D是H2SO4,E是NH3,F是NO,
故答案为:SO2;H2SO4;NH3;NO;
(2)铵根离子的检验,主要是用铵盐和碱反应生成氨气,氨气呈碱性,能使石蕊的红色石蕊试纸变红,检验方案为:取少量溶液于试管中,向其中加入加入浓NaOH溶液并加热,若产生能使湿润的红色石蕊试纸变蓝的气体,则证明有NH4+,否则没有,
故答案为:取少量溶液于试管中,向其中加入加入浓NaOH溶液并加热,若产生能使湿润的红色石蕊试纸变蓝的气体,则证明有NH4+,否则没有.
点评 本题考查无机物推断,物质的颜色、性质是推断突破口,注意掌握中学常见连续反应,熟练掌握元素化合物知识及常见离子检验.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:填空题
 ②Na2O2
②Na2O2 ③N2
③N2 ④H2O
④H2O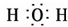 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②④③①⑤ | B. | ②③①④⑤ | C. | ②④③⑤① | D. | ②⑤③①④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 福尔马林可用作食品的保鲜剂 | |
| B. | “血液透析”利用了胶体的性质 | |
| C. | 气象环境报告中的“PM2.5”是对一种新分子的描述 | |
| D. | 氢氧化钠可作胃酸的中和剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:推断题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③④ | B. | ①③④ | C. | ③④ | D. | ①②③ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
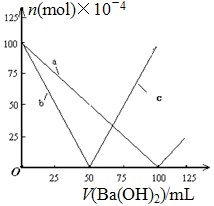 烧杯中盛有 100mL 0.1mol/L 的 NaHSO4溶液,向其中逐滴滴加 0.1mol/L 的 Ba(OH)2溶液,烧杯中某些物质(或微粒)的物质的量的变化曲线如图.下列说法正确的是( )
烧杯中盛有 100mL 0.1mol/L 的 NaHSO4溶液,向其中逐滴滴加 0.1mol/L 的 Ba(OH)2溶液,烧杯中某些物质(或微粒)的物质的量的变化曲线如图.下列说法正确的是( )| A. | 曲线 a 表示 Ba2+的物质的量的变化 | |
| B. | 曲线 c 表示 OH-的物质的量的变化 | |
| C. | 加入 Ba(OH)2溶液 50mL 时反应的离子方程式为:Ba2++OH-+H++SO42-═BaSO4↓+H2O | |
| D. | 加入 Ba(OH)2溶液大于 50mL 后,反应的离子方程式为:OH-+H+═H2O |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com