

分析 铬铁矿的主要成分可表示为FeO•Cr2O3,还含有SiO2、Al2O3等杂质,将铬铁矿和氢氧化钠、空气混合焙烧,发生反应得到Na2CrO4、NaAlO2、NaOH、Na2SiO3、NaFeO2,然后水浸、过滤得到滤渣1和浸出液,浸出液中溶质是Na2CrO4、NaAlO2、NaOH、Na2SiO3,根据信息①知,滤渣1为Fe(OH)3,在浸出液中加入试剂a调整人员PH,试剂a应为酸,依据流程中分离出的物质可知,加入酸为硫酸,溶液中偏铝酸钠、Na2SiO3、NaOH与硫酸溶液生成硅酸沉淀和氢氧化铝沉淀,然后过滤得到滤液和滤渣2,滤渣2是H2SiO3、Al(OH)3,滤液中含有Na2CrO4、和Na2SO4,加入硫酸继续调节溶液的pH,根据信息②知,溶质变为Na2Cr2O7,将混合溶液蒸发浓缩、冷却结晶得到Na2Cr2O7晶体,和滤液为Na2SO4,
(1)根据发生的反应确定固体产物成分;FeO•Cr2O3和氧气发生氧化还原反应;
(2)结合题给信息确定滤渣成分,浸出液的成分除Na2CrO4、NaOH外,还含有NaAlO2、NaOH、Na2SiO3,NaFeO2在水溶液中强烈水解生成对应的氢氧化物,所以滤渣1为Fe(OH)3;
(3)上述分析可知试剂A为硫酸;
(4)酸性过强,产品Na2Cr2O7晶体中可能含有铝离子,偏铝酸钠和适量硫酸反应生成氢氧化铝沉淀,氢氧化铝会溶解于氢氧化铝生成铝离子.
解答 解:(1)通过以上分析知,“焙烧”后的固体产物成分除Na2CrO4、NaFeO2外,还有NaAlO2、Na2SiO3,铬元素化合价+3价,铁元素化合价为+2价,被氧气氧化生成铬酸钠和NaFeO2,铬元素化合价变化为+6价,铁元素化合价变化为+3价,电子转移总数为34,据此电子守恒和原子守恒配平书写得到焙烧过程中发生的氧化还原反应为4FeO•Cr2O3+7O2+10Na2CO3$\frac{\underline{\;高温\;}}{\;}$8Na2CrO4+4NaFeO2+10CO2,4FeO•Cr2O3反应电子转移28,每熔化1mol FeO•Cr2O3,转移的电子数为$\frac{28}{4}$mol×6.02×1023=4.214×1024,
故答案为:4FeO•Cr2O3+7O2+10Na2CO3$\frac{\underline{\;高温\;}}{\;}$8Na2CrO4+4NaFeO2+10CO2;4.214×1024;
(2)浸出液中溶质是Na2CrO4、NaAlO2、NaOH、Na2SiO3,浸出液的成分除Na2CrO4、NaOH外,还含有NaAlO2、Na2SiO3,NaFeO2在水溶液中强烈水解生成对应的氢氧化物,所以滤渣1为Fe(OH)3,
故答案为:NaAlO2、Na2SiO3;Fe(OH)3;
(3)由分析可知,流程最后分离得到硫酸钠,加入的试剂a为硫酸,用来调节溶液PH,
故答案为:H2SO4 ;
(4)该流程中用了两步调节pH,若合并成一步调pH,酸性过强,产品Na2Cr2O7晶体中可能含有较多杂质,可能含有铝离子,偏铝酸钠和适量硫酸反应生成氢氧化铝沉淀,氢氧化铝会溶解于氢氧化铝生成铝离子,AlO2-+H++H2O=Al(OH)3,Al(OH)3+3H+=Al3++H2O,引入该杂质的原因用离子方程式说明为:AlO2-+4H+=Al3++2H2O或AlO2-+H++H2O=Al(OH)3,Al(OH)3+3H+=Al3++3H2O,
故答案为:AlO2-+4H+=Al3++2H2O或AlO2-+H++H2O=Al(OH)3,Al(OH)3+3H+=Al3++3H2O.
点评 本题考查了物质分离提纯的实验过程分析判断,主要是物质性质和试剂选择、试剂反应的产物分析应用,掌握基础是解题关键,题目难度中等.


 励耘书业暑假衔接宁波出版社系列答案
励耘书业暑假衔接宁波出版社系列答案科目:高中化学 来源: 题型:解答题
 已知A、B、C是中学化学的常见物质,它们在一定条件下有如图转化关系:
已知A、B、C是中学化学的常见物质,它们在一定条件下有如图转化关系:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Al2O3、NaHCO3均可与强酸、强碱反应,都为两性物质 | |
| B. | Na2O2、AlCl3在适当条件下均可导电,都为电解质 | |
| C. | CuCl2与FeCl3均可与Fe发生置换反应,都可充当氧化剂 | |
| D. | BaCO3、BaSO4、Ba(OH)2均难溶于水,所以均属于难溶电解质 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| TiCl4 | SiCl4 | |
| 熔点/℃ | -25.0 | -68.8 |
| 沸点/℃ | 136.4 | 57.6 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 实验是化学研究的一种重要手段,现有如图所示A~G七种仪器,请根据要求填空.
实验是化学研究的一种重要手段,现有如图所示A~G七种仪器,请根据要求填空.查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 和
和 E、CH3CH2CH2CH3和
E、CH3CH2CH2CH3和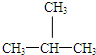
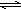 HCO3-+OH-
HCO3-+OH- 的系统命名为:3-甲基-4-乙基-庚烷
的系统命名为:3-甲基-4-乙基-庚烷 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 甲是一种可用于净水和膨化食品的盐,由A、B、C、D、E五种短周期元素组成.甲溶于水后可电离出三种离子,其中一种是由A、B形成的10电子阳离子.A元素原子核内质子数比E的少l,D、E同主族.某同学为探究甲的组成而进行如下实验:
甲是一种可用于净水和膨化食品的盐,由A、B、C、D、E五种短周期元素组成.甲溶于水后可电离出三种离子,其中一种是由A、B形成的10电子阳离子.A元素原子核内质子数比E的少l,D、E同主族.某同学为探究甲的组成而进行如下实验:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com