
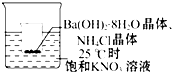
 °ŃŠ”ÉÕ±·ÅČė25”ęµÄŹ¢ÓŠ±„ŗĶĻõĖį¼ŲČÜŅŗµÄ“óÉÕ±ÖŠ£¬Š”ÉÕ±£ØŅѱ»Éč·Ø¹Ģ¶Ø£©ÖŠ·ÅÓŠ 25gŃŠ³É·ŪÄ©µÄĒāŃõ»Æ±µ¾§Ģå[Ba£ØOH£©2•8H2O]£¬ŌŁ¼ÓČėŌ¼12gµÄĀČ»Æļ§¾§Ģ壬²¢½Į°čŹ¹Ęä³ä·Ö·“Ó¦£®
°ŃŠ”ÉÕ±·ÅČė25”ęµÄŹ¢ÓŠ±„ŗĶĻõĖį¼ŲČÜŅŗµÄ“óÉÕ±ÖŠ£¬Š”ÉÕ±£ØŅѱ»Éč·Ø¹Ģ¶Ø£©ÖŠ·ÅÓŠ 25gŃŠ³É·ŪÄ©µÄĒāŃõ»Æ±µ¾§Ģå[Ba£ØOH£©2•8H2O]£¬ŌŁ¼ÓČėŌ¼12gµÄĀČ»Æļ§¾§Ģ壬²¢½Į°čŹ¹Ęä³ä·Ö·“Ó¦£®·ÖĪö Ba£ØOH£©2•8H2OŗĶNH4ClµÄ·“Ó¦ĪüČČ£¬¹ŹÄÜŹ¹±„ŗĶĻõĖį¼ŲČÜŅŗµÄĪĀ¶Č½µµĶ£¬¶ųĻõĖį¼ŲµÄČܽā¶ČĖę×ÅĪĀ¶ČµÄ½µµĶ¶ų¼õŠ”£¬¹Ź»įÓŠĻõĖį¼Ų¾§ĢåĪö³ö£¬¾Ż“Ė·ÖĪö£®
½ā“š ½ā£ŗBa£ØOH£©2•8H2OŗĶNH4ClµÄ·“Ó¦ĪüČČ£¬¹ŹÄÜŹ¹±„ŗĶĻõĖį¼ŲČÜŅŗµÄĪĀ¶Č½µµĶ£¬¶ųĻõĖį¼ŲµÄČܽā¶ČĖę×ÅĪĀ¶ČµÄ½µµĶ¶ų¼õŠ”£¬¹Ź»įÓŠĻõĖį¼Ų¾§ĢåĪö³ö£®
£Ø1£©ĻõĖį¼ŲµÄČܽā¶ČĖę×ÅĪĀ¶ČµÄ½µµĶ¶ų¼õŠ”£¬¹Ź±„ŗĶĻõĖį¼ŲČÜŅŗÖŠ»įÓŠ¾§ĢåĪö³ö£¬¹Ź“š°øĪŖ£ŗKNO3ČÜŅŗÖŠÓŠ¾§ĢåĪö³ö£»
£Ø2£©µ¼ÖĀÉĻŹöĻÖĻóµÄŌŅņŹĒBa£ØOH£©2•8H2OÓėNH4Cl¾§Ģå·“Ó¦ĪüČČ£¬Ź¹ČÜŅŗĪĀ¶Č½µµĶ£¬KNO3Čܽā¶Č¼õŠ”£¬µ¼ÖĀ¾§ĢåĪö³ö£¬¹Ź“š°øĪŖ£ŗBa£ØOH£©2•8H2OÓėNH4Cl¾§Ģå·“Ó¦ĪüČČ£¬Ź¹ČÜŅŗĪĀ¶Č½µµĶ£¬KNO3Čܽā¶Č¼õŠ”£¬µ¼ÖĀ¾§ĢåĪö³ö£»
£Ø3£©Ba£ØOH£©2•8H2OÓėNH4Cl¾§Ģå·“Ó¦ĪüČČ£¬¹Ź·“Ó¦ĪļµÄ×ÜÄÜĮæŠ”ÓŚÉś³ÉĪļµÄ×ÜÄÜĮ棬¹Ź“š°øĪŖ£ŗŠ”ÓŚ£»
£Ø4£©Ba£ØOH£©2•8H2OÓėNH4Cl¾§Ģå·“Ó¦ĪüČČ£¬¹ŹÄÜĮæ±ä»ÆÓėĒāŃõ»Æ±µŗĶĀČ»Æļ§·“Ó¦²»Ķ¬µÄ·“Ó¦¼“ĪŖ·ÅČČ·“Ó¦£¬ĒŅŅŖĒóŹĒČżøö²»Ķ¬ĄąŠĶµÄ·“Ó¦£¬ČēHCl+NaOH=NaCl+H2OĪŖ·ÅČČ·“Ó¦£¬ĪŖø“·Ö½ā·“Ó¦£» Zn+H2SO4=ZnSO4+H2”üĪŖ·ÅČČ·“Ó¦£¬ĒŅĪŖÖĆ»»·“Ó¦£»CH4+2O2$\stackrel{µćČ¼}{”ś}$CO2+2H2OĪŖ·ÅČČ·“Ó¦£¬ĪŖŃõ»Æ»¹Ō·“Ó¦£¬
¹Ź“š°øĪŖ£ŗHCl+NaOH=NaCl+H2O”¢Zn+H2SO4=ZnSO4+H2”ü”¢CH4+2O2$\stackrel{µćČ¼}{”ś}$CO2+2H2O£®
µćĘĄ ±¾Ģāæ¼²éĪüČČ·“Ó¦µÄĢ½¾æ£¬ĢāÄæÄŃ¶Č²»“󣬱¾Ģā×¢Ņā°ŃĪÕĀČ»Æļ§ŗĶĒāŃõ»Æ±µ·“Ó¦µÄŌĄķ£¬×¢Ņā“Ó·“Ó¦ĪļÓėÉś³ÉĪļ×ÜÄÜĮæµÄ¹ŲĻµ·ÖĪö£®


 ÓäæģµÄŗ®¼ŁÄĻ¾©³ö°ęÉēĻµĮŠ“š°ø
ÓäæģµÄŗ®¼ŁÄĻ¾©³ö°ęÉēĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ¢Ł¢Ü | B£® | ¢Ł¢Ś | C£® | ¢Ū¢Ü | D£® | ¢Ł¢Ū¢Ü |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
| ĪĀ¶Č/”ę | ĘšŹ¼Įæ/mol | Ę½ŗāĮæ/mol | “ļµ½Ę½ŗāĖł ŠčŹ±¼ä/min | ||
| H2O | CO | H2 | CO | ||
| 900 | 1.0 | 2.0 | 0.4 | 1.6 | 3.0 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
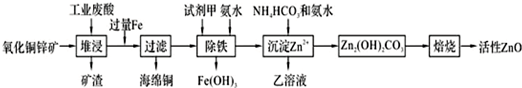
| Ąė×Ó | æŖŹ¼³ĮµķŹ±µÄpH | ĶźČ«³ĮµķŹ±µÄpH |
| Fe2+ | 6.34 | 9.7 |
| Fe3+ | 1.48 | 3.2 |
| Zn2+ | 6.2 | 8.0 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 150 mL | B£® | 200 mL | C£® | 250 mL | D£® | ĪŽ·ØČ·¶Ø |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
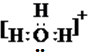 ŗĶ
ŗĶ £»
£»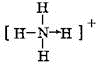 ŗĶO=C=O£®
ŗĶO=C=O£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Ćŗ¾“¦Ąķ±äĪŖĘųĢåČ¼ĮĻµÄ¹ż³ĢŹōÓŚĪļĄķ±ä»Æ | |
| B£® | µķ·Ū”¢ÓĶÖ¬ŗĶµ°°×ÖŹ¶¼ŹĒøß·Ö×Ó»ÆŗĻĪļ | |
| C£® | ŅŅĶéŗĶŅŅ“¼¾łÄÜ·¢ÉśČ”“ś·“Ó¦ | |
| D£® | ŅŅĖįŅŅõ„ŗĶÖ²ĪļÓĶ¾łæÉĖ®½āÉś³ÉŅŅ“¼ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ¢Ł¢Ś¢Ū¢Ż | B£® | ¢Ś¢Ū¢Ü¢Ž | C£® | ¢Ś¢Ū¢Ü¢Ż | D£® | ¢Ł¢Ū¢Ü¢Ż |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com