
将氯化铝溶液和氢氧化钠溶液等体积混合,得到的沉淀物中铝元素的质量与溶液中所含铝元素的质量相等,则原氯化铝溶液和氢氧化钠溶液的物质的量浓度之比可能是()
| A. | 1:3 | B. | 3:2 | C. | 1:4 | D. | 2:7 |
| 化学方程式的有关计算. | |
| 专题: | 计算题. |
| 分析: | 将氯化铝溶液和氢氧化钠溶液等体积混合,得到的沉淀物中含铝元素的质量与溶液中含铝元素的质量相等,沉淀为Al(OH)3,溶液中的铝可能为AlCl3或NaAlO2, 可分别发生:Al3++3OH﹣═Al(OH)3↓、Al(OH)3+OH﹣=AlO2﹣+2H2O,结合反应的离子方程式分为两种情况讨论计算. |
| 解答: | 解:设AlCl3和NaOH的浓度分别为c1和c2,相同体积为V, 若NaOH过量,生成NaAlO2,此时参加反应的AlCl3的物质的量是c1Vmol,NaOH是3c1Vmol,生成c1V mol 的Al(OH)3, 又因为得到的沉淀物中铝元素的质量和溶液中铝元素的质量相等,则说明第一步反应完后,生成的Al(OH)3有一半( 所以可求的NaOH的物质的量为:3c1V+0.5c1V=3.5c1V=c2V,所以c1:c2=2:7,D选项符合; 当氯化铝过量时,氢氧化钠不足,生成氢氧化铝白色沉淀发生反应:Al3++3OH﹣═Al(OH)3↓,设反应掉的铝离子物质的量为x,得到的沉淀物中铝元素的质量和溶液中铝元素的质量相等,则c1V﹣x=x,所以x=0.5c1V,消耗氢氧化钠3x,即1.5c1Vmol,所以1.5c1V=c2V,所以此时c1:c2=2:3,没有选项符合, 故选D. |
| 点评: | 本题考查了根据方程式进行计算,同时考查学生分析问题、解决问题能力,很多同学往往只考虑溶液中的铝元素为铝离子而漏掉为偏铝酸根离子而导致错误,为易错点,题目难度中等. |


科目:高中化学 来源: 题型:
关于工业合成氨的叙述中,错误的是( )
A.在动力、设备、材料允许的情况下,反应尽可能在高压下进行
B.温度越高越有利于工业合成氨
C.在工业合成氨中N2、H2的循环利用可提高其利用率,降低成本
D.及时从反应体系中分离出氨气有利于平衡向正反应方向移动
查看答案和解析>>
科目:高中化学 来源: 题型:
有关Al与NaOH溶液的反应的说法中,正确的是()
| A. | 铝是还原剂,其氧化产物是Al(OH)3 | |
| B. | NaOH是氧化剂,其还原产物是H2 | |
| C. | 铝是还原剂,H2O和NaOH都是氧化剂 | |
| D. | H2O是氧化剂,Al被氧化 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列除去杂质的方法不正确的是()
| A. | 镁粉中混有少量铝粉:加入过量烧碱溶液充分反应,过滤、洗涤、干燥 | |
| B. | 用过量氨水除去Fe3+溶液中的少量Al3+ | |
| C. | 用新制的生石灰,通过加热蒸馏,以除去乙醇中的少量水 | |
| D. | Al(OH)3中混有少量Mg(OH)2:加入足量烧碱溶液,充分反应,过滤,向滤液中通入过量CO2后过滤 |
查看答案和解析>>
科目:高中化学 来源: 题型:
将一定质量的镁、铝合金,投入100mL一定浓度的盐酸中,合金完全溶解.向所得溶液中滴加5mol/L NaOH溶液,生成的沉淀质量与加入NaOH溶液体积如图所示,由图中数据分析计算:
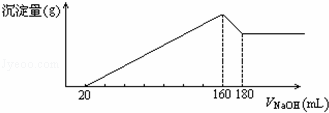
①原合金中镁的质量为g
②铝的质量为g
③盐酸的物质的量浓度为mol/L.
查看答案和解析>>
科目:高中化学 来源: 题型:
下列条件下的X溶液均能跟少量盐酸反应,其中反应速率最快的是
A.10℃ 20 mL 3mol/L的X溶液 B.20℃ 30 mL 2mol/L的X溶液
C.20℃ 10 mL 4mol/L的X溶液 D.10℃ 10 mL 2mol/L的X溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
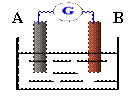
右图为某原电池装置:
(1)若A为Zn,B为石墨,电解质溶液 为稀硫酸,则A极的电极反应式为______________________________。
为稀硫酸,则A极的电极反应式为______________________________。
(2)若A为铜,B为铁,电解质溶液为Fe2(SO4)3溶液,则铜片为______极(填正或负);该极电极反应式为______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
一定条件下的反应:PCl5(g) PCl3(g)+Cl2(g)(正反应吸热)达到平衡后,下列情况使PCl5分解率降低的是
PCl3(g)+Cl2(g)(正反应吸热)达到平衡后,下列情况使PCl5分解率降低的是
A. 温度、体积不变,充入氩气 B. 体积不变,对体系加热
C. 温度、体积不变,充入氯气 D. 温度不变,增大容器体积
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com