
【题目】亚硝酰氯(NOCl,熔点:-64.5 ℃,沸点:-5.5 ℃)是一种黄色气体,遇水易反应,生成一种氯化物和两种氧化物。可用于合成清洁剂、触媒剂及中间体等。实验室可由氯气与一氧化氮在常温常压下合成。
(1)甲组的同学拟制备原料气NO和Cl2,制备装置如下图所示:
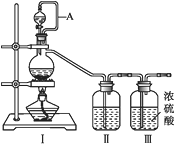
为制备纯净干燥的气体,下表中缺少的药品是:
装置Ⅰ | 装置Ⅱ | ||
烧瓶中 | 分液漏斗中 | ||
制备纯净Cl2 | MnO2 | ① | ② |
制备纯净NO | Cu | ③ | ④ |
②___________,③___________。
(2)乙组同学利用甲组制得的NO和Cl2制备NOCl,装置如图所示:

①装置连接顺序为a→___________________(按气流自左向右方向,用小写字母表示)。
②装置Ⅶ的作用为________________,若无该装置,Ⅸ中NOCl可能发生反应的化学方程式为_______________________________。
③乙组同学认为氢氧化钠溶液只能吸收氯气和NOCl,不能吸收NO,所以装置Ⅷ不能有效除去有毒气体。为解决这一问题,可将尾气与某种气体同时通入氢氧化钠溶液中,这种气体的化学式是__________。
(3)丙组同学查阅资料,查得王水是浓硝酸与浓盐酸的混酸,一定条件下混酸可生成亚硝酰氯和氯气,该反应的化学方程式为___________________。
(4)丁组同学用以下方法测定亚硝酰氯(NOCl)纯度
取Ⅸ中所得液体mg溶于水,配制成250mL溶液;取出25.00mL,以K2CrO4溶液为指示剂,用c mol/LAgNO3 标准溶液滴定至终点,消耗标准溶液的体积为b mL。(已知:Ag2CrO4为砖红色固体)
①亚硝酰氯(NOCl)的质量分数为_________(用代数式表示即可)。
②若滴定前,滴定管尖嘴有气泡,滴定后气泡消失,则所测亚硝酰氯的纯度_________(偏高、偏低、无影响)
【答案】饱和食盐水 稀硝酸 e→f(或f→e)→c→b→d 防止水蒸气进入装置Ⅸ 2NOCl+H2O=2HCl+NO+NO2 O2(或NO2) HNO3(浓)+3HCl(浓)=NOCl↑+Cl2↑+2H2O ![]() ×100% 偏高
×100% 偏高
【解析】
氯气与一氧化氮在常温常压下合成NOCl。根据实验室用浓盐酸与二氧化锰制备氯气,制得的氯气中混有氯化氢和水蒸气;用铜和稀硝酸反应制备NO,制得的NO中可能混有其他氮氧化合物,结合NOCl的性质,制得气体中的杂质需要除去,尾气中氯气、NO以及NOCl均不能排放到空气中,需要用氢氧化钠溶液吸收,据此分析解答。
(1)实验室制备氯气,一般用浓盐酸与二氧化锰加热制备,制得的氯气中混有氯化氢和水蒸气,故装置Ⅱ用饱和食盐水吸收氯化氢气体;
实验室制备NO,一般用铜和稀硝酸反应制备,制得的NO中可能混有其他氮氧化合物,NO不溶于水,故装置Ⅱ用水净化NO;故答案为:饱和食盐水;稀硝酸;
(2)①将氯气和NO干燥后在装置Ⅵ中发生反应,由于亚硝酰氯(NOCl,熔点:-64.5 ℃,沸点:-5.5 ℃)是一种黄色气体,遇水易反应,需要在冰盐中冷凝收集NOCl,氯气、NO以及NOCl均不能排放到空气中,需要用氢氧化钠溶液吸收,NOCl遇水易水解,故在收集装置和尾气处理装置之间需加一个干燥装置,因此装置连接顺序为a→e→f(或f→e)→c→b→d,故答案为:e→f(或f→e)→c→b→d;
②NOCl遇水易水解,故在收集装置和尾气处理装置之间需加一个装置 VII干燥装置防止水蒸气进入装置Ⅸ;若无该装置,Ⅸ中NOCl水解生成氯化氢、NO和NO2,反应的化学方程式为2NOCl+H2O=2HCl+NO+NO2,故答案为:防止水蒸气进入装置Ⅸ;2NOCl+H2O=2HCl+NO+NO2;
③乙组同学认为氢氧化钠溶液只能吸收氯气和NOCl,不能吸收NO,所以装置Ⅷ不能有效除去有毒气体。NO能够与氧气反应生成二氧化氮,二氧化氮能够被氢氧化钠溶液吸收,一氧化氮和二氧化氮的混合气体也能够被氢氧化钠溶液吸收,因此解决这一问题,可将尾气与氧气(或二氧化氮)同时通入氢氧化钠溶液中,故答案为:O2(或NO2);
(3)王水是浓硝酸与浓盐酸的混酸,一定条件下混酸可生成亚硝酰氯和氯气,反应的化学方程式为:HNO3(浓)+3HCl(浓)=NOCl↑+Cl2↑+2H2O,故答案为:HNO3(浓)+3HCl(浓)=NOCl↑+Cl2↑+2H2O;
(4)①亚硝酰氯(NOCl)遇水反应得到HCl,用AgNO3标准溶液滴定,生成白色沉淀,以K2CrO4溶液为指示剂,出现砖红色沉淀达到滴定终点,根据氯元素守恒: NOCl~HCl~AgNO3,则样品中n(NOCl)=cmol/L×b×10-3L×![]() = 10bc×10-3mol,亚硝酰氯(NOCl)的质量分数为
= 10bc×10-3mol,亚硝酰氯(NOCl)的质量分数为![]() ×100%=
×100%=![]() ×100%,故答案为:
×100%,故答案为:![]() ×100%;
×100%;
②若滴定前,滴定管尖嘴有气泡,滴定后气泡消失,导致消耗的标准溶液的体积偏大,则所测亚硝酰氯的纯度偏高,故答案为:偏高。


 小学学习好帮手系列答案
小学学习好帮手系列答案 小学同步三练核心密卷系列答案
小学同步三练核心密卷系列答案科目:高中化学 来源: 题型:
【题目】下列与金属腐蚀有关的说法正确的是( )

A. 图a中,插入海水中的铁棒,越靠近底端腐蚀越严重
B. 图b中,开关由M改置于N时,Cu-Zn合金的腐蚀速率减小
C. 图c中,接通开关时Zn腐蚀速率增大,Zn上放出气体的速率也增大
D. 图d中,钢铁轮船外壳连接一块金属A(铜块)可以减缓船体外壳腐蚀速度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知HA的酸性弱于HB的酸性。25℃时,用NaOH固体分别改变物质的量浓度均为0.1 molL-1的HA溶液和HB溶液的pH(溶液的体积变化忽略不计),溶液中A-、B-的 物质的量浓度的负对数与溶液的pH的变化悄况如图所示。
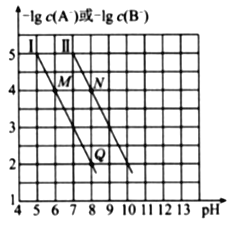
下列说法正确的是( )
A. 曲线Ⅰ表示溶液的pH与-lgc(A-)的变化关系
B. ![]()
C. 溶液中水的电离程度:M>N
D. N点对应的溶液中c(Na+)>Q点对应的溶液中c(Na+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示是一系列含硫化合物的转化关系(反应中生成的水已略去),其中说法正确的是

A.反应①说明SO2具有漂白性,反应②说明SO2具有酸性
B.反应②中生成物n(Na2SO3):n(NaHSO3)=1:1时,则反应物n(SO2):n(NaOH)=1:2
C.反应③④⑤均属于氧化还原反应
D.工业上可利用反应②和反应④回收SO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,下列关亍电解质的说法中正确的是
A. 中和等体积、等浓度的氨水和氢氧化钠溶液至pH等于7,前者消耗的盐酸多
B. 向NaHS 溶液中加入适量 KOH 后:c(Na+)=c(H2S)+c(HS-)+c(S2-)
C. 将amol·L-1的醋酸与0.01 mol·L-1的氢氧化钠溶液等体积混合,溶液中:c(Na+)=c(CH3COO-),醋酸的电离常数Ka=![]() (用含a的代数式表示)
(用含a的代数式表示)
D. 向NH4Cl溶液中加入少量等浓度的稀盐酸,则 的值减小
的值减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氟喹诺酮是人工合成的抗菌药,其中间体G的合成路线如下:
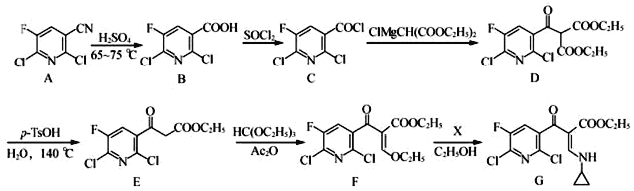
(1)G中的含氧官能团为_____和_____(填名称)。
(2)由C→D的反应类型是_____。
(3)化合物X(分子式为C3H7N)的结构简式为_____。
(4)E到F过程中的反应物HC(OC2H5)3中最多有_____个碳原子共面。
(5)B和乙醇反应的产物为H(C8H6FCl2NO2),写出该反应的化学方程式_______________ 。
写出满足下列条件的H的所有同分异构体的结构简式:_____________。
Ⅰ.是一种α﹣氨基酸;
Ⅱ.分子中有4种不同化学环境的氢,且分子中含有一个苯环。
(6)根据已有知识并结合相关信息,写出以 ![]() 和ClMgCH(COOC2H5)2为原料制备
和ClMgCH(COOC2H5)2为原料制备 的合成路线流程图(无机试剂任选,合成路线流程图示例见本题题干)_____________。
的合成路线流程图(无机试剂任选,合成路线流程图示例见本题题干)_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2019年是“国际化学元素周期表年”。1869年门捷列夫把当时已知的元素根据物理、化学性质进行排列,准确预留了甲、乙两种未知元素的位置,并预测了二者的相对原子质量,部分原始记录如下。下列说法不正确的是( )

A. 元素乙的原子序数为32
B. 原子半径比较:甲>乙>Si
C. 元素乙的简单气态氢化物的稳定性强于![]() 。
。
D. 推测乙可以用作半导体材料
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某溶液中含如下离子组中的几种![]()
![]()
![]()
![]() ,某同学欲探究该溶液的组成进行了如下实验:
,某同学欲探究该溶液的组成进行了如下实验:
Ⅰ.用铂丝醮取少量溶液,在火焰上灼烧,透过蓝色钴玻璃,观察到紫色火焰
Ⅱ.另取原溶液加入足量盐酸有无色气体生成,此时溶液颜色加深,但无沉淀生成
Ⅲ.取Ⅱ反应后溶液分别置于两支试管中,第一支试管中加入 BaCl2 溶液有白色沉淀生成, 再滴加 KSCN 溶液,上层清液变红,第二支试管加入 CCl4,充分振荡静置后溶液分层,下层为无色。
下列说法正确的是( )
A.原溶液中肯定不含 ![]()
B.原溶液中肯定含有 ![]()
C.步骤Ⅱ中无色气体是 NO 气体,无 CO2 气体产生
D.为确定是否含有 Cl-可取原溶液加入过量硝酸银溶液,观察是否产生白色沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某溶液中可能含有OH-、CO32-、A1O2-、SiO32-、SO42-、HCO3-、Na+、Fe3+、Mg2+、Al3+等离子。当向该溶液中逐滴加入一定物质的量浓度的盐酸溶液时,发现生成沉淀的物质的量随盐酸溶液的体积变化如下图所示。下列说法正确的是
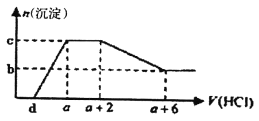
A. 原溶液中可能含有Na2SO4、可能不含有CO32-
B. 原溶液中一定含有的阴离子只有:OH-、A1O2-、CO32-
C. 原溶液中含CO32-与A1O2-的物质的量之比为3:4
D. a-d>3/4
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com