
����Ŀ����ͼ��ʾװ�ý���̽��ʵ�飬����֤����������ϩ��������ϩ���в������ԡ����¶�Ѹ�������ɹ۲쵽�Թ�����ˮ��ɫ����ƿ��Ũ�������Ҵ��Ļ��Һ���Ϊ�غ�ɫ��
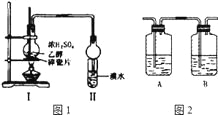
��1��д����ʵ����������ϩ�Ļ�ѧ����ʽ: _______
��2����ͬѧ��Ϊ:���ǵ��û��Һ�巴Ӧ�ĸ����ԣ���ˮ��ɫ��������֤����Ӧ������ϩ��������ϩ���в������ԣ���������ȷ���� ������ĸ��ţ�
A����ϩ����ˮ����ȡ����Ӧ B��ʹ��ˮ��ɫ�ķ�Ӧ,δ���Ǽӳɷ�Ӧ
C��ʹ��ˮ��ɫ������,δ������ϩ D��Ũ���������Ҵ�������ȩ,Ҳ��ʹ��ˮ��ɫ
��3����ͬѧ����ϸ�¹۲����Ϊ�Թ�����һ�����֤����Ӧ������ϩ���ɣ����������____________
��4����ͬѧ������ʵ��װ�ý����˸Ľ�����I��II֮��������ͼ2װ�ã���A�е��Լ�ӦΪ______________����������______________��B�е��Լ�Ϊ______________
��5����������ʵ�����ƿ�з�Һ����ȷ������ ������ĸ��ţ�
A����Һ��ȴ������ˮ����
B����Һ��ȴ����շ�Һ����
C����ˮ������ƿ��ϡ�ͺ����Һ�ף�
���𰸡���14�֣�
��1����![]()
��2����BC
��3����Һ������㣬�²�����״Һ��
��4����NaOH��Һ ����SO2Ʒ����Һ
��5����B
��������
���⣨1���Ҵ���Ũ����������¼��ȵ�170��������ȥ��Ӧ������ϩ����Ӧ�Ļ�ѧ����ʽΪCH3CH2OH![]() CH2=CH2��+H2O��
CH2=CH2��+H2O��
��2��A����ϩ����ˮ������ȡ����Ӧ��A�����B��ʹ��ˮ��ɫ�ķ�Ӧ��δ���Ǽӳɷ�Ӧ��B����ȷ�� C��Ũ���������ˮ�Ժ�ǿ�����ԣ��ܽ�C������CO2����Ũ����Ļ�ԭ�����Ƕ�������������Ҳ��ʹ��ˮ��ɫ����ʹ��ˮ��ɫ������,δ������ϩ����ȷ��D��Ũ�������л��ﷴӦ������ˮ�ԣ����������Ҵ�������ȩ,����ѡBC��
��3�������ϩ����ˮ�����ӳɷ�Ӧ����Ӧ����±������������±����������ˮ�����۲쵽Һ��ֲ㣬��״Һ�����²㣬֤������������ɣ�����Ӧ������ϩ���ɡ�
��4�����������������������NaOH��Һ��ȥ���ɣ�Ϊ�˼����Ƿ������B��Ӧ��ʢ��Ʒ����Һ������SO2�Ƿ����������A�е��Լ�ӦΪNaOH��Һ�������������ն�������B�е��Լ�ΪƷ����Һ��
��5��ʵ�����ƿ�з�Һ�к���Ũ���ᣬŨ�����ܶȴ���ˮ������ˮ���ȣ���Ũ������и�ʴ�ԣ������ȷ�Ĵ��������Ƿ�Һ��ȴ����շ�Һ���У���ѡB��


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������������У�����һ�����ʵ�������������ֲ�ͬ��
��MgO��Na2O��CO2��CuO
��HCl��H2O��H2SO4��HNO3
��NaOH��Na2CO3��KOH��Cu(OH)2
(1)��������������(�ѧʽ)��
A________��B________��C________��
(2)д������C������ϡ���ᷴӦ�����ӷ���ʽ��______________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ����( )
A.ij���ʲ��ǵ���ʾ��Ƿǵ����
B.̼��������ˮ�еĵ��뷽��ʽ��![]()
C.�ܵ����H+ �Ļ����ﶼ����
D.������ǿ����Һ�������ƶ���������Ŀ��һ���ȵ�����������Һ�������ƶ�����������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��(1)�ݿƼ��ձ����������Ͽ���ѧ�����Ŷӽ������ͱ������Ṳ�������״�ʵ��ϩ������Ч����ɫ�ϳɡ�ϩ�������仯������Ƴɸ��͡�ҽҩ��ũҩ�����ϣ��ϳ�ά����E��KI����Ȼ����ҩ����ɼ���ж����йؼ���ϩ�����ṹ����ϩ���Ľṹ��ʽΪCH2=CH-CH2OH����ش��������⣺
�ٻ�̬��ԭ�ӵļ۵����Ų�ʽΪ___________________��
��1 mol CH2=CH-CH2OH��____mol������ϩ����������̼ԭ�ӵ��ӻ�����Ϊ________��
�� Ni2+���γɶ��������ӣ���[Ni(NH3)6]2+��[Ni(CN)2]2�� ��[Ni(SCN)2]�� �ȣ���CN����Ϊ�ȵ�����ķ���Ϊ____________��
(2)��Ȳ���л��ϳɹ�ҵ��һ��ԭ�ϡ���ҵ������CaC2��ˮ��Ӧ������Ȳ��
��CaC2��C22����O22+��Ϊ�ȵ����壬O22+�ĵ���ʽ�ɱ�ʾΪ_____________�� lmol O22+�к��е�������ĿΪ_______________��
�ڽ���Ȳͨ��[Cu(NH3)2]Cl��Һ����Cu2C2����ɫ������Cu+��̬��������Ų�ʽΪ____________��
����Ȳ�������ᷴӦ�ɵñ�ϩ��(H2C=CH-C��N)����ϩ�������̼ԭ�ӹ���ӻ�������_______________�������д���ͬһֱ���ϵ�ԭ����Ŀ���Ϊ_______________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���Ȳ裬�Ժܶ�����˵��������һ����֣���Ҷ�к��������Ŀ����������������Ѫ�ܡ��̼����Ե����ã��������������Ի�����������ȷ¡��Ҵ�����ͪ���ȱ��ȣ�����ˮ��ʯ���ѡ����нᾧˮ�Ŀ���������ɫ��״�ᾧ��ζ�࣬��100��ʱʧȥ�ᾧˮ����ʼ������120��ʱ�����൱������178��ʱ�����ܿ졣�ṹʽ����,ʵ���ҿ�ͨ�����м����Ӳ�Ҷ����ȡ������

(1)������ķ���ʽΪ________________��
(2)����1�ݽ���Ҷ���õ��ܼ����Ϊ��_______��
A ˮ B �ƾ� C ʯ����
(3)�������к��������ŵ�����Ϊ______________
(4)1mol����������⣬���������_____________mol H2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���״���һ�ֿ�������Դ����CO2�Ʊ��״��Ĺ��̿����漰�ķ�Ӧ���£�
��Ӧ����CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) ��H1=��49.58 kJmol��1
CH3OH(g)+H2O(g) ��H1=��49.58 kJmol��1
��Ӧ����CO2(g)+H2(g)![]() CO(g)+H2O(g) ��H2
CO(g)+H2O(g) ��H2
��Ӧ����CO(g)+2H2(g)![]() CH3OH(g) ��H3=��90.77 kJmol��1
CH3OH(g) ��H3=��90.77 kJmol��1
�ش��������⣺
(1)��Ӧ��ġ�H2=_________������Ӧ����������ƽ�ⳣ���ֱ�ΪK1��K2��K3����K2=________(��K1��K3��ʾ)��
(2)��Ӧ���Է�����������___________(�����ϵ��¶��������ϸ��¶��������κ��¶���)��
(3)��һ��������2 L�����ܱ������г���3 mol H2��1.5 mol CO2����������Ӧ��ʵ���ò�ͬ��Ӧ�¶�����ϵ��CO2��ƽ��ת���ʵĹ�ϵ�����±���ʾ��
�¶�(��) | 500 | T |
CO2��ƽ��ת���� | 60�G | 40�G |
��T______500��(����>������<�� ����=��)��
���¶�Ϊ500��ʱ���÷�Ӧ10 minʱ�ﵽƽ�⡣��H2��ʾ�÷�Ӧ�ķ�Ӧ����v(H2)=______________�����¶��£���ӦI��ƽ�ⳣ��K=______________L2/mol2
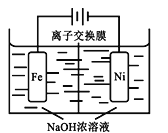
(4)��CO2�Ʊ��״�����Ҫ��������ҵ���õ�ⷨ��ȡNa2FeO4��ͬʱ���������Fe+2H2O+2OH![]() FeO42+3H2��������ԭ����ͼ��ʾ�����һ��ʱ���c(OH)���͵�������__________ (������������������������)�����ҷ����ĵ缫��ӦʽΪ��___________________________��
FeO42+3H2��������ԭ����ͼ��ʾ�����һ��ʱ���c(OH)���͵�������__________ (������������������������)�����ҷ����ĵ缫��ӦʽΪ��___________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������Na2CO3��NaHCO3��˵����ȷ���� ( )
A.��ˮ�е��ܽ��ԣ�NaHCO3��Na2CO3
B.������������ͬ��������Һ��Ӧ�ų�����Ŀ�����NaHCO3��Na2CO3
C.���ȶ��ԣ�NaHCO3��Na2CO3
D.�������Ĺ������������ᷴӦ�ų�CO2������Na2CO3��NaHCO3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����з��ӻ������У����幹����ƽ�������ε��ǣ� ��
A. CH4B. NH4+
C. NO3-D. CO2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪�ƻ�1 mol A��A����1 mol B��B����1 mol A��B��ʱ�ֱ���Ҫ����436 kJ��498 kJ��463 kJ����������Ӧ2A2+B2![]() 2A2B�������仯��ϵ��ͼ��ʾ������˵������������(����)��
2A2B�������仯��ϵ��ͼ��ʾ������˵������������(����)��
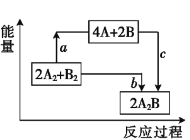
A. a=1370 kJB. b=482 kJ
C. �÷�Ӧ�����ȷ�ӦD. ��ϵ��A��Bԭ�������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com