
【题目】有机化学中的反应类型较多,请写出下列反应类型。
①苯与浓硝酸共热生成硝基苯__________
②乙醛和新制的银氨溶液反应__________
③乙烯使溴的四氯化碳溶液褪色________
④溴乙烷和氢氧化钠的乙醇溶液共热________
⑤由乙炔制备聚乙炔_______________
【答案】取代(硝化)反应 氧化反应(不能答银镜反应) 加成反应 消去反应 加聚反应
【解析】
根据有机物的官能团判断有机物的反应类型,苯可以发生取代反应,乙烯、乙炔含有不饱和键,可发生加成、加聚和氧化反应,乙醛可以发生氧化反应,溴乙烷和发生水解、消去反应,以此解答该题。
①苯与浓硝酸在浓硫酸、加热条件下发生取代反应生成硝基苯与水,反应方程式为:![]() ,该反应为取代反应,
,该反应为取代反应,
因此,本题正确答案是:取代反应;
②乙醛分子中含有官能团醛基,能够发生银镜反应,该反应为氧化反应,
因此,本题正确答案是:氧化反应;
③含有不饱和键的有机分子能发生加成反应,有机物分子中的不饱和键断裂,断键原子与其它原子或原子团相结合,生成新的化合物,乙烯含有碳碳双键,能和溴反应生成1,2-二溴乙烷,该反应为加成反应,
因此,本题正确答案是:加成反应;
④溴乙烷和氢氧化钠的乙醇溶液共热生成乙烯、溴化钠和水,该反应为消去反应,
因此,本题正确答案是:消去反应;
⑤乙炔发生加聚反应生成聚乙炔,该反应为加聚反应,
因此,本题正确答案是:加聚反应。


科目:高中化学 来源: 题型:
【题目】环己烷可制备1,4-环己二醇。下列七步有关反应(其中无机产物都已经略去)中,其中有两步属于取代反应,两步属于消去反应,三步属于加成反应(提示:⑤属于1,4-加成反应)
试回答:
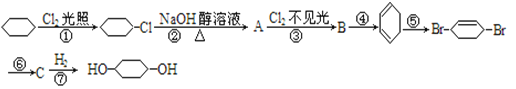
(1)写出下列化合物的结构简式:B__________,C________。
(2)反应________和________(填写序号)属于取代反应
(3)反应④所用的试剂和条件分别为:___________。
(4)写出下列反应的化学方程式:
①____________________________;④____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列三个化学反应的平衡常数(K1、K2、K3)与温度的关系分别如下表所示:
化学反应 | 平衡常数 | 温度 | |
973K | 1173K | ||
①Fe(s)+CO2(g) | K1 | 1.47 | 2.15 |
②Fe(s)+H2O(g) | K2 | 2.38 | 1.67 |
③CO(g)+H2O(g) | K3 | ? | ? |
则下列说法正确的是
A.△H1<0,△H2>0
B.反应①②③的反应热满足关系:△H2-△H1=△H3
C.反应①②③的平衡常数满足关系:K1·K2=K3
D.要使反应③在一定条件下建立的平衡向正反应方向移动,可采取升温措施
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图为相互串联的三个装置,试回答:
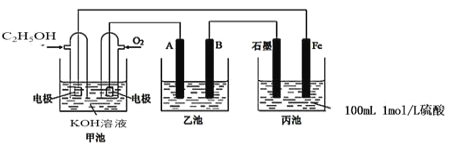
(1)写出甲池负极的电极反应式:________。
(2)若甲池消耗4.6gC2H5OH气体,则丙池中石墨极上生成气体的物质的量为______,反应一段时间后丙池溶液pH_______(填“增大”、“减小”、“不变”)。
(3)若利用乙池在铁片上镀银,则B是_______(填电极材料),电极反应式是______。
(4)若乙池中A、B为石墨电极,电解质溶液为CuCl2。当丙池共产生6.72L(标况)气体时,乙池A极产物_____mol,检验该产物的方法为:______(简述操作)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. Si、P、S、Cl相应的最高价氧化物对应水化物的酸性依次增强
B. 自然界中含有大量的游离态的硅,纯净的硅晶体可用于制作计算机芯片
C. 工业上通常用电解钠、铁、铜对应的氯化物制得该三种金属单质[
D. 钠与氧气反应的产物与反应条件无关
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将甲烷与氯气A按1:2的体积比混合于一试管中,倒立于盛有饱和食盐水的水槽,置于光亮处,下列有关此实验的现象和结论的叙述不正确的是( )
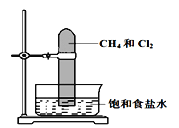
A.试管中气体的黄绿色逐渐变浅,水面上升B.生成物只有三氯甲烷和氯化氢
C.试管内壁有油状液滴形成D.试管内有少量白雾
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I、实验室中常用MnO2氧化浓盐酸的方法制取氯气,实验装置如图所示:
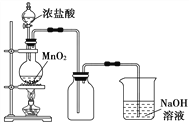
(1)圆底烧瓶中发生反应的化学反应方程式是__________________。
(2)如果将过量二氧化锰与20 mL 12 mol·L-1的盐酸混合加热(忽略盐酸的挥发),充分反应后生成的氯气明显_________(填大于、等于、小于)0.06 mol。其主要原因有_____________________________;
(3)写出尾气处理的离子方程式是_______________________。
II、用Na2CO3·10H2O晶体,配制0.2 mol·L-1的Na2CO3溶液480 mL。
(1)应称取Na2CO3·10H2O晶体的质量:____________。定容时,向容量瓶中加水,至1~2cm时,改用_________加水至刻度,加盖摇匀;
(2)下列操作对所配溶液的浓度可能产生影响
①Na2CO3·10H2O晶体失去了部分结晶水 ②用“左码右物”的称量方法称量晶体(使用游码) ③碳酸钠晶体不纯,其中混有氯化钠 ④容量瓶未经干燥使用。 其中引起所配溶液浓度偏高的有______________(填序号)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】T℃时,在1 L的密闭容器中充入2 mol CO2和6 mol H2,发生反应:
CO2(g) + 3H2(g)![]() CH3OH(g) + H2O(g) H = - 49.0 kJ·mol-1。
CH3OH(g) + H2O(g) H = - 49.0 kJ·mol-1。
测得H2和CH3OH(g)的浓度随时间变化情况如下图所示:
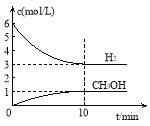
下列说法不正确的是
A.0~10min内v(H2) = 0.3 mol·L-1·min-1
B.T℃时,平衡常数K=1/27,CO2与H2的转化率相等
C.T℃时,当有32 g CH3OH生成时,放出49.0 kJ的热量
D.达到平衡后,升高温度或再充入CO2气体,都可以提高H2的转化率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下将NaOH溶液滴加到己二酸(H2X)溶液中,混合溶液的pH与离子浓度变化的关系如图所示。下列叙述错误的是( )
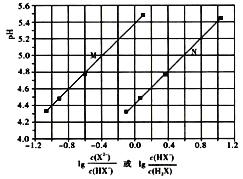
A.Ka2(H2X)的数量级为10-6
B.曲线N表示pH与lg![]() 的变化关系
的变化关系
C.NaHX溶液中c(H+)>c(OH-)
D.当混合溶液呈中性时,c(Na+)>c(HX-)>c(X2-)>c(H+)=c(OH-)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com