
分析 (1)生石灰和水反应生成Ca(OH)2且放出大量热,放出的热量导致溶液温度升高,抑制氨气溶解,氢氧根离子浓度增大抑制一水合氨电离;
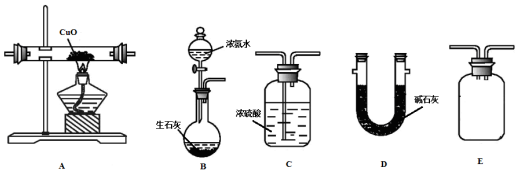
(2)甲同学按B-A-E-C-D的顺序连接装置,过程中生成的水和过量氨气会被装置C吸收;
(3)乙同学按B-A-D-E-C的顺序连接装置,装置C可以吸收多余氨气和防止空气中水蒸气进入D影响测定结果;
(4)丙同学认为乙同学测量的m(H2O)会偏高,可能是氨气中水蒸气进入装置D被吸收,可以用碱石灰吸收干燥生成的氨气再和氧化铜反应;
(5)2NH3+3CuO$\stackrel{△}{→}$N2+3Cu+3H2O,结合化学方程式定量关系计算;
(6)若CuO中混有Cu,氧元素质量减小,测定水质量减小,结合计算定量关系判断结果误差.
解答 解:(1)生石灰和水反应生成Ca(OH)2且放出大量热,放出的热量导致溶液温度升高,温度越高,导致氨气的溶解度越低;氢氧化钙电离生成氢氧根离子,氢氧根离子浓度增大抑制一水合氨电离,则抑制氨气溶解,所以常用氨水滴入生石灰中制取氨气,浓氨水滴入生石灰中能制得NH3的原因是:氨水中存在平衡NH3+H2O?NH3.H2O?NH4++OH-,生石灰吸收浓氨水中的水放出热量,生成OH-均能使平衡向左移动,从而得到氨气,
故答案为:氨水中存在平衡NH3+H2O?NH3.H2O?NH4++OH-,生石灰吸收浓氨水中的水放出热量,生成OH-均能使平衡向左移动,从而得到氨气;
(2)甲同学按B-A-E-C-D的顺序连接装置,该方案不可行,C装置将生成的水和多余的氨气一起吸收,无法测量出生成水的质量,
故答案为:不可行;C装置将生成的水和多余的氨气一起吸收,无法测量出生成水的质量;
(3)乙同学按B-A-D-E-C的顺序连接装置,则装置C的作用是:吸收未反应的NH3;防止空气中的水蒸气进入,
故答案为:吸收未反应的NH3,防止空气中的水蒸气进入;
(4)丙同学认为乙同学测量的m(H2O)会偏高,可能是装置B生成的氨气有混有水,故m(H2O)会偏高,可在装置B和A之间增加装置D吸收氨气中水蒸气,减少误差,
故答案为:装置B生成的氨气有混有水,故m(H2O)会偏高;可在装置B和A之间增加装置D;
(5)反应2NH3+3CuO$\stackrel{△}{→}$N2+3Cu+3H2O,生成水物质的量和氧化铜物质的量相同,若实验中测得m(H2O)=b g,氧化铜物质的量n=$\frac{bg}{18g/mol}$,实验中先称取氧化铜的质量[m(CuO)]为a g,则Cu的摩尔质量=$\frac{ag}{\frac{bg}{18g/mol}}$-16g/mol,Cu的相对原子质量为:$\frac{18a}{b}$-16,
故答案为:$\frac{18a}{b}$-16;
(6)若CuO中混有Cu,氧元素质量减小,测定水质量减小,b减小则$\frac{18a}{b}$-16值增大,所以若CuO中混有Cu,则该实验测定结果偏大,
故答案为:偏大.
点评 本题考查了物质组成和含量的测定,物质成分和实验操作的理解应用、主要是实验过程的设计,掌握基础是解题关键,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 甲苯和水 | B. | 硝酸钾和氯化钠 | ||
| C. | 乙酸乙酯和甘油(丙三醇) | D. | 食盐水和泥沙 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 简单离子半径的大小顺序:rX>rY>rZ>rW | |
| B. | 元素Q和Z能形成QZ2型的共价化合物 | |
| C. | Z元素氢化物的沸点高于W元素氢化物的沸点 | |
| D. | X、Y、Z最高价氧化物的水化物之间两两不能发生反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 最高价氧化物对应水化物的碱性:乙>丙 | |
| B. | 简单气态氢化物的稳定性:丁>甲 | |
| C. | 简单离子半径:乙>丙>丁 | |
| D. | 甲和乙组成的化合物只存在离子键 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子半径:X>Y>Z>Q>W | |
| B. | 最高价氧化物对应的水化物的酸性:Z<Q | |
| C. | Q和W可形成原子个数比为1:1和2:1的化合物 | |
| D. | X、Y和W三种元素形成的化合物的水溶液呈碱性 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 一定量CO2通入某浓度的NaOH溶液得溶液A,向A溶液中逐滴滴入稀盐酸,加入n(HCl)与生成n(CO2)的关系如图所示.下列有关叙述正确的是( )
一定量CO2通入某浓度的NaOH溶液得溶液A,向A溶液中逐滴滴入稀盐酸,加入n(HCl)与生成n(CO2)的关系如图所示.下列有关叙述正确的是( )| A. | 通入的CO2气体为22.4 L | B. | A溶液中n(NaOH)=2n(Na2CO3) | ||
| C. | A溶液中既含Na2CO3,又含NaHCO3 | D. | A溶液中一定只有Na2CO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
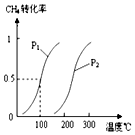 在容积为100L的密闭容器中,加入1.0molCH4和2.0molH2O(g).一定条件下发生反应:CH4(g)+H2O(g)?CO(g)+3H2(g)△H
在容积为100L的密闭容器中,加入1.0molCH4和2.0molH2O(g).一定条件下发生反应:CH4(g)+H2O(g)?CO(g)+3H2(g)△H查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com