
【题目】A、B、C、D、E五瓶透明溶液,分别是Na2CO3、BaCl2、HCl、NaHSO4、AgNO3中的一种。
①A与D反应有气体生成; ②A与E反应有沉淀生成;
③B与E反应有沉淀生成; ④B与C反应有沉淀生成 ;
⑤C与D反应有气体生成; ⑥在②和③的反应中生成的沉淀是同一种物质
请填空:
(1)在②和③的反应中,生成的沉淀物质的化学式是_______________
(2)D为_________________,E为__________________。
(3)B与D反应的离子方程式为____________________________________。
(4)向一定量的Ba(HCO3)2溶液中,逐滴加入C溶液,直至不再生成沉淀,该过程中发生反应的离子方程式为:________________________________,沉淀完全后,继续滴加C溶液,此时发生反应的化学方程式为:__________________________________。
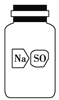
(5)实验室有一瓶标签破损(如图所示)的固体试剂。某同学取试剂瓶中的固体少量于试管中,加适量蒸馏水溶解,在所得溶液中加入过量BaCl2溶液,得到白色沉淀。由此,该同学推断这瓶试剂是硫酸钠。你认为他的结论是否正确?________。若正确,请写出相应的离子反应方程式;若不正确,请给出
进一步验证的实验方案(要求:所用试剂只能从A、B、C、D、E中选择):__________________________________________________。
【答案】AgCl Na2CO3 AgNO3 Ba2++CO32-=BaCO3↓ Ba2++SO42-+H++HCO3-=BaSO4↓+H2O+CO2↑ NaHCO3+NaHSO4=Na2SO4+H2O+CO2↑(或H++HCO3-=H2O+CO2↑) 不正确 将沉淀完全的溶液静置,取上层清液于另一试管中,滴加Na2CO3溶液,如有气体产生,说明固体物质是NaHSO4;若无明显现象,则向除去上层清液的试管中滴加盐酸,若滴加时有气体产生,最终沉淀溶解,则固体物质是Na2SO3;若滴加过程中无明显现象,则固体物质是Na2SO4
【解析】
根据⑥“在②和③的反应中生成的沉淀是同一种物质”这一信息可知,A与B中必然含有相同的离子,容易推断出它们是HCl和BaCl2,都可与银离子反应生成AgCl沉淀;因此,E必然是AgNO3;再根据①,A与D反应有气体生成,推断A一定是HCl,那么,B是BaCl2,D是Na2CO3,剩余的一种物质,即NaHSO4就是C。
(1)在②和③的反应中,HCl和BaCl2与硝酸银离反应生成AgCl沉淀,故答案为:AgCl;
(2)由题意分析可知,A是HCl、B是BaCl2、C是NaHSO4、D是Na2CO3、E是AgNO3,故答案为:Na2CO3;AgNO3;
(3)B与D反应为溶液中BaCl2与Na2CO3反应生成碳酸钡沉淀和氯化钠,反应的离子方程式为:Ba2++CO32-=BaCO3↓,故答案为:Ba2++CO32-=BaCO3↓;
(4)向一定量的Ba(HCO3)2溶液中,逐滴加入NaHSO4溶液,直至不再生成沉淀,说明溶液中Ba2+离子完全沉淀,HCO3—离子过量,反应的离子方程式为:Ba2++SO42-+H++HCO3-=
BaSO4↓+H2O+CO2↑,沉淀完全后,继续滴加NaHSO4溶液,NaHSO4电离出的H+离子与过量的HCO3-离子反应生成二氧化碳和水,反应的离子方程式为:H++HCO3-=H2O+CO2↑,故答案为:Ba2++SO42-+H++HCO3-=BaSO4↓+H2O+CO2↑;H++HCO3-=H2O+CO2↑;
(5)由示意图可知,该试剂可能为硫酸钠或硫酸氢钠或亚硫酸钠,加入过量BaCl2溶液,硫酸钠、硫酸氢钠和亚硫酸钠均可与BaCl2反应得到白色沉淀,故该同学结论不正确,若要进一步验证,应该用碳酸钠确定溶液中是否存在H+离子,用盐酸确定沉淀是否是亚硫酸钡沉淀,实验方案为:将沉淀完全的溶液静置,取上层清液于另一试管中,滴加Na2CO3溶液,如有气体产生,说明固体物质是NaHSO4;若无明显现象,则向除去上层清液的试管中滴加盐酸,若滴加时有气体产生,最终沉淀溶解,则固体物质是Na2SO3;若滴加过程中无明显现象,则固体物质是Na2SO4,故答案为:不正确;将沉淀完全的溶液静置,取上层清液于另一试管中,滴加Na2CO3溶液,如有气体产生,说明固体物质是NaHSO4;若无明显现象,则向除去上层清液的试管中滴加盐酸,若滴加时有气体产生,最终沉淀溶解,则固体物质是Na2SO3;若滴加过程中无明显现象,则固体物质是Na2SO4。


科目:高中化学 来源: 题型:
【题目】下列热化学方程式中△H代表燃烧热的是
A. C6H12O6 (s) + 6O2 (g) = 6CO2 (g) + 6H2O (l);△H1
B. H2(g) + 1/2O2 (g) = H2O (g) ;△H2
C. CH4 (g) + 3/2O2 (g) = 2H2O (l) + CO (g);△H3
D. 2CO (g) + O2 (g) = 2CO2 (g);△H4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示是配制一定物质的量浓度溶液的过程示意图.下列说法中错误的是
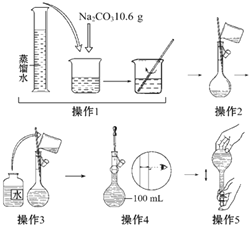
A. 所配制的Na2CO3溶液的物质的量浓度为1.0 molL﹣1
B. 操作2是将溶解的Na2CO3溶液转移到容量瓶中
C. 操作4如果仰视,结果配得溶液浓度偏低
D. 操作5中,定容摇匀后发现液面低于刻度线,要继续加水至液面与刻度线平齐
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列除去括号内杂质的试剂或操作正确的是
A.Al2O3(SiO2):水B.NH4Cl(I2):加热
C.CO2(SO2):饱和NaHSO3溶液D.HCl(Cl2):苯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在同一条件下,体积相同的三个烧瓶中分别盛有NH3、HCl、NO2气体,并分别倒立在水槽中,充分反应后(已知:3NO2+H2O =2HNO3+NO,NO不溶于水),烧瓶内三种溶液的物质的量浓度之比为(设烧瓶中的溶液未扩散到水槽里)
A. 3:3:2 B. 2:2:3 C. 1:1:1 D. 2:2:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业由钛铁矿(主要成分FeTiO3)制备TiCl4的主要工艺流程如下:
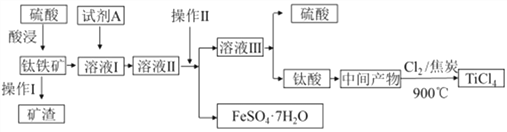
请答下列问题:
(1)已知酸浸反应FeTiO3(s)+2H2SO4(aq)=FeSO4(aq)+TiOSO4(aq)+2H2O,则FeTiO3中钛元素的化合价为_____。
(2)试剂A为____,加入A的目的是____ (填字母)。
A.防止Fe2+被氧化 B.与Fe3+反应 C.防Fe2+水解
“溶液II经“操作II"可得副产品FeSO4·7H2O,则“操作II”包括浓缩、冷却、_____。
(3)若“溶液II中Fe2+的浓度为0.49mol/L,为防止生成Fe(OH)2沉淀,溶液的pH不超过__。(已知Ksp[Fe(OH)2]=4.9×10-17)
(4)钛酸煅烧得中间产物的化学方程式为H2TiO3(s) ![]() TiO2(s)+H2O(g),上述工艺流程中生成TiCl4化学方程式为_____________________。
TiO2(s)+H2O(g),上述工艺流程中生成TiCl4化学方程式为_____________________。
已知TiO2(s)+2Cl2(g)=TiC14(l)+O2(g) △H=+151kJ/mol,该反应极难进行,当向反应体系中加入焦炭后,则反应在高温条件下能顺利发生。从化学平衡的角度解释原因是_______。
(5)TiCl4极易水解,利用此性质可制备纳米级TiO2·xH2O,该反应的化学方程式是_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列因果关系不正确的是( )
选项 | 原因 | 结果 |
A | 植树造林 | 温室效应 |
B | 二氧化硫和二氧化氮大量排放 | 酸雨 |
C | 汽车尾气的排放 | 光化学烟雾 |
D | 含氮、磷等元素的生活废水的大量排放 | 赤潮 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于化合物![]() 说法错误的是( )
说法错误的是( )
A. 1mol该化合在一定条件下加氢最多可消耗5mol H2
B. 该化合物最多有14个原子共面
C. 该化合物能使酸性高锰酸钾溶液褪色
D. 该化合物与![]() 互为同分异构体
互为同分异构体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】据报道,月球上有大量3He存在,以下关于3He的说法正确的是( )
A.是4He的同素异形体
B.比4He多一个中子
C.是4He的同位素
D.比4He少一个质子
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com