
| A、石蕊层仍为紫色 |
| B、石蕊层有两层,上层为紫色,下层为蓝色 |
| C、石蕊层为三层环,由上而下是蓝色、紫色、红色 |
| D、石蕊层为三层环,由上而下是红色、紫色、蓝色. |


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
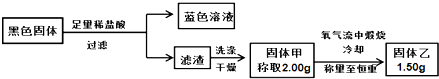
| A、只有CuO |
| B、CuO、Cu2S和CuS |
| C、CuO、CuS |
| D、CuO、Cu2S |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 1 |
| 2 |
| A、m+n>p |
| B、A的转化率增大 |
| C、平衡逆向移动 |
| D、C的体积百分含量增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:
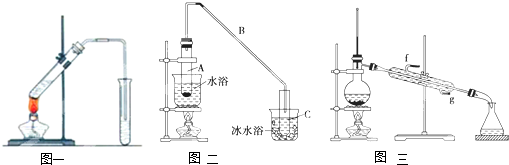
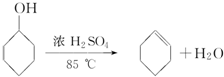
| 密度(g/cm3) | 熔点(℃) | 沸点(℃) | 溶解性 | |
| 环己醇 | 0.96 | 25 | 161 | 能溶于水 |
| 环己烯 | 0.81 | -103 | 83 | 难溶于水 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 某化学兴趣小组在进行钠在空气中燃烧的实验,请写出钠在氧气中燃烧的化学方程式:
某化学兴趣小组在进行钠在空气中燃烧的实验,请写出钠在氧气中燃烧的化学方程式:
| 实验目的 | 实验步骤 | 实验现象 | 结论 |
| 验证猜想1 | 1.将一小块钠从煤油中直接取出加热燃烧 2.取出一小块切去表皮并擦干净煤油的钠加热燃烧 | 黑色物质中含 有碳单质 | |
| 验证猜想3 | 黑色物质中 含有铁元素 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 容器 | 甲 | 乙 | 丙 |
| 反应物投入量 | 1mol N2、3mol H2 | 2mol NH3 | 4mol NH3 |
| NH3的浓度(mol/L) | c1 | c2 | c3 |
| 反应的能量变化 | 放出a kJ | 吸收b kJ | 吸收c kJ |
| 体系压强(Pa) | p1 | p2 | p3 |
| 反应物转化率 | α1 | α2 | α3 |
| A、2c1>c3 |
| B、a+b>92.4 |
| C、2p2<p3 |
| D、α1+α3<1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 为了确认CH3COOH、H2CO3和H2SiO3的酸性强弱,有人设计用如图所示装置,一次实验达到目的(不能再选用其他酸性溶液).
为了确认CH3COOH、H2CO3和H2SiO3的酸性强弱,有人设计用如图所示装置,一次实验达到目的(不能再选用其他酸性溶液).查看答案和解析>>
科目:高中化学 来源: 题型:
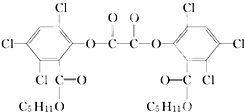 夏日的夜晚,常看见儿童手持发光的“魔棒”在广场上嬉戏.“魔棒”发光原理是利用过氧化氢氧化草酸二酯产生能量,该能量被传递给荧光物质后便发出荧光,草酸二酯(CPPO)结构简式如图.下列有关说法不正确的是( )
夏日的夜晚,常看见儿童手持发光的“魔棒”在广场上嬉戏.“魔棒”发光原理是利用过氧化氢氧化草酸二酯产生能量,该能量被传递给荧光物质后便发出荧光,草酸二酯(CPPO)结构简式如图.下列有关说法不正确的是( )| A、草酸二酯的分子式为C26H24Cl6O8 |
| B、1 mol草酸二酯与氢氧化钠稀溶液反应(苯环上卤素不水解),最多消耗4 mol NaOH |
| C、该有机物能发生加成反应、取代反应、氧化反应 |
| D、1 mol草酸二酯与氢气完全反应,需要氢气6 mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、取羊皮纸袋内液体加入碘水变蓝色 |
| B、取烧杯中液体加入KI溶液不变蓝色 |
| C、取烧杯中液体加入AgNO3溶液产生黄色沉淀 |
| D、取烧杯中液体加入碘水变蓝色 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com