


分析 (1)根据离子完全沉淀的pH值来确定在盐泥中加入稀硫酸调pH为1~2并煮沸的目的;
(2)根据氢氧化镁的Ksp=c(Mg2+)•c(OH-)2来计算;
(3)根据三种化合物的溶解度(S)随温度变化的曲线来回答;
(4)镁离子可以和氢氧化钠发生反应生成氢氧化镁沉淀,过滤,得到纯净的沉淀,再加入硫酸,蒸发结晶可以获得硫酸镁晶体;
(5)根据镁元素守恒结合关系式:MgSO4•7H2O-Mg(OH)2进行计算.
解答 解:(1)根据离子完全沉淀的pH值可以知道,在盐泥中加入稀硫酸调pH为1~2并煮沸的目的是为了提高Mg2+的浸取率,
故答案为:为了提高Mg2+的浸取率;
(2)氢氧化镁的Ksp=c(Mg2+)•c(OH-)2,溶液中Mg2+的浓度为6.0mol•L-1,则溶液的氢氧根浓度=$\sqrt{\frac{6.0×1{0}^{-12}}{6.0}}$mol/L=10-6mol/L,所以氢离子浓度为10-8mol/L,pH为8,故答案为:8;
(3)温度较高时钙盐与镁盐分离得更彻底,或者根据三种化合物的溶解度(S)随温度变化的曲线,可以知道高温下CaSO4•2H2O溶解度小,所得到的滤渣主要成分是:Al(OH)3、Fe(OH)3、CaSO4•2H2O,
故答案为:温度较高时钙盐与镁盐分离得更彻底(或高温下CaSO4•2H2O溶解度小等合理答案均可);Al(OH)3、Fe(OH)3、CaSO4•2H2O;
(4)镁离子可以和氢氧化钠发生反应生成氢氧化镁沉淀,过滤,得到纯净的沉淀,再加入硫酸,蒸发结晶可以获得硫酸镁晶体,
故答案为:NaOH溶液;向沉淀中加足量稀硫酸;
(5)解:设该盐泥中含Mg(OH)2的质量为X,MgSO4•7H2O质量为24.6克,物质的量是0.1mol.
由关系式MgSO4•7H2O-Mg(OH)2
1mol 58克
0.1mol x 解得:x=5.8克
故该盐泥中含Mg(OH)2的百分含量为:$\frac{5.8}{29}$×100%=20%,
故答案为:20.0%.
点评 本题是一道物质的分离和提纯知识的综合实验题,考查学生分析和解决问题的能力,综合性强,题目难度中等.


科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Fe2O3溶于过量的氢酸碘中:Fe2O3+6H+═2Fe3++3H2O | |
| B. | 向NaAlO2溶液中通入过量CO2:AlO2-+CO2+2H2O═Al(OH)3↓+CO32- | |
| C. | 向漂白粉溶液中通入SO2气体:Ca2++2ClO-+SO2+H2O═CaSO3↓+2HClO | |
| D. | 向Fe(NO3)2溶液中加入稀盐酸:3Fe2++4H++NO3-═3Fe3++NO↑+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 时间(s) c(mol/L) | 0 | 20 | 40 | 60 | 80 | 100 |
| c(A) | 0.20 | 0.14 | b | 0.09 | 0.09 | 0.09 |
| c(B) | 0.00 | 0.12 | 0.20 | c | d | e |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 (1)某温度下,在一密闭容器中,X、Y、Z 三种气体的物质的量随时间的变化曲线如图所示.分析有关数据,写出X、Y、Z反应的化学方程式X+3Y
(1)某温度下,在一密闭容器中,X、Y、Z 三种气体的物质的量随时间的变化曲线如图所示.分析有关数据,写出X、Y、Z反应的化学方程式X+3Y 2Z.
2Z.查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 乙酸异戊脂是组成蜜蜂信息素质的成分之一,具有香蕉的香味,实验室制备乙酸异戊酯的反应装置示意图图1和有关数据如下:
乙酸异戊脂是组成蜜蜂信息素质的成分之一,具有香蕉的香味,实验室制备乙酸异戊酯的反应装置示意图图1和有关数据如下: +
+ $?_{△}^{浓H_{2}SO_{4}}$
$?_{△}^{浓H_{2}SO_{4}}$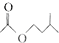 +H2O
+H2O| 相对分子质量 | 密度/(g.cm-3) | 沸点/℃ | 水中溶解性 | |
| 异戊醇 | 88 | 0.8123 | 131 | 微溶 |
| 乙醇 | 60 | 1.0492 | 118 | 溶 |
| 乙醇异戊酯 | 130 | 0.8670 | 142 | 难溶 |

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 如图中相连的两种物质均可归为一类,相交的部分A、B、C、D为其相应的分类标准代号,请回答下列问题:
如图中相连的两种物质均可归为一类,相交的部分A、B、C、D为其相应的分类标准代号,请回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com