
| A、①③ | B、①③④ |
| C、②③④ | D、①②③④ |


 一线名师权威作业本系列答案
一线名师权威作业本系列答案科目:高中化学 来源: 题型:
| A、与水或酸反应置换氢气越来越剧烈 |
| B、对应元素的金属性由弱到强 |
| C、对应金属阳离子氧化性由弱到强 |
| D、原子半径由小到大 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:

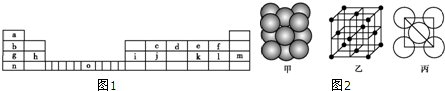
查看答案和解析>>
科目:高中化学 来源: 题型:

| 过程ⅣB中溶液含有的离子 | 过程ⅥB中溶液含有的离子 | |
| 甲 | 有Fe2+,无Fe3+ | 有SO42- |
| 乙 | 既有Fe3+,又有Fe2+ | 有SO42- |
| 丙 | 有Fe3+,无Fe2+ | 有Fe2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用加热NH4Cl的方法制氨气 |
| B、将CuSO4?5H2O置于蒸发皿中加热除去结晶水 |
| C、用金属钠检验酒精中是否含有水 |
| D、用饱和FeCl3溶液和沸水反应制备Fe(OH)3胶体 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 对于可逆反应mA(g)+nB(g)?pC(g)+qD(g),若其它条件都不变,探究催化剂对反应的影响,可得到如下两种v-t图象.下列判断正确的是( )
对于可逆反应mA(g)+nB(g)?pC(g)+qD(g),若其它条件都不变,探究催化剂对反应的影响,可得到如下两种v-t图象.下列判断正确的是( )| A、b1>b2,t1>t2 |
| B、两图中阴影部分面积一定相等 |
| C、A的平衡转化率(Ⅱ)大于(Ⅰ)中A的转化率 |
| D、若m+n<p+q,则压强变化对正反应速率的影响程度比逆反应速率影响程度大 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、向蛋白质溶液中加入CuSO4溶液发生蛋白质变性 |
| B、煤焦油中含有苯、二甲苯等化工原料 |
| C、天然气和可燃冰的主要成分都是甲烷 |
| D、石油裂解的主要目的是为了得到更多的汽油 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、葡萄糖与果糖、淀粉与纤维素均互为同分异构体 |
| B、纤维素、蔗糖、葡萄糖和脂肪在一定条件下都可发生水解反应 |
| C、糖、油脂、蛋白质均不溶于水 |
| D、淀粉、纤维素、蛋白质都是天然高分子化合物 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com