
【题目】下列化合物中,核磁共振氢谱只出现两组峰且峰面积之比为3:2的有
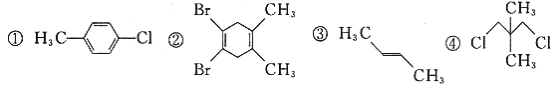
A.0种B.1种C.2种D.3种
【答案】C
【解析】
化合物的核磁共振氢谱中出现2个峰说明有机物中含有2种类型的氢原子,且原子数之比为3:2;①分子中含有三种等效氢原子,应出现三种峰值,故不符合;②分子中含有两种等效氢,出现两种峰值,且不同峰值的氢原子个数比为3:2,故符合;③分子中含有两种等效氢,出现两种峰值,且不同峰值的氢原子个数比为3:1,故不符合;④分子中含有两种等效氢,出现两种峰值,且不同峰值的氢原子个数比为3:2,故符合;核磁共振氢谱只出现两组峰且峰面积之比为3:2的有2个,故选C。
【点晴】
本题考查了有机化合物结构的分析判断,明确分子中的等效氢的判断方法是解题关键。化合物的核磁共振氢谱中出现2个峰说明有机物中含有2种类型的氢原子,根据等效氢判断,分子中等效氢原子一般有如下情况:①分子中同一甲基上连接的氢原子等效,②同一碳原子所连甲基上的氢原子等效,③处于镜面对称位置上的氢原子等效。


科目:高中化学 来源: 题型:
【题目】市场上经常见到的标记为Li-ion的电池称为“锂离子电池”。它的负极材料是金属锂和碳的复合材料(碳作为金属锂的载体),电解质为一种能传导Li+的高分子材料。这种电池的电池反应式为:Li+2Li0.35NiO2![]() 2Li0.85NiO2,下列说法不正确的是( )
2Li0.85NiO2,下列说法不正确的是( )
A.放电时,负极的电极反应式:Li-e-=Li+
B.充电时,Li0.85NiO2既发生氧化反应又发生还原反应
C.该电池不能用水溶液作为电解质溶液
D.放电过程中Li+向负极移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】参考下列图表和有关要求回答问题:
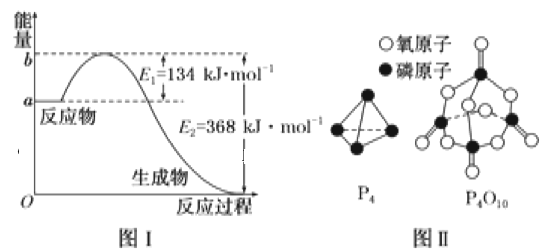
(1)图Ⅰ是1molNO2(g)和1molCO(g)反应生成CO2和NO过程中能量变化示意图,若在反应体系中加入催化剂,反应速率增大,E2的变化是__(填“增大”“减小”或“不变”,下同),ΔH的变化是__。请写出NO2和CO反应的热化学方程式:__。
(2)下表是部分化学键的键能数据:
化学键 | P—P | P—O | O=O | P=O |
键能(kJ·mol-1) | 198 | 360 | 498 | x |
已知1mol白磷(P4)完全燃烧放热为1194kJ,白磷及其完全燃烧的产物结构如图Ⅱ所示,则表中x=__kJ·mol-1。
(3)PCl5是一种重要的含磷化合物,在有机合成中用作氯化剂。某温度时,向2.0L恒温恒容密闭容器中充入1.0molPCl5,发生反应PCl5(g)![]() PCl3(g)+C12(g)ΔH=+124kJ·mol-1。反应过程中测定的部分数据见下表:
PCl3(g)+C12(g)ΔH=+124kJ·mol-1。反应过程中测定的部分数据见下表:
时间t/s | 0 | 50 | 150 | 250 | 350 |
n(PCl3)/mol | 0 | 0.16 | 0.19 | 0.2 | 0.2 |
反应在前50s的平均速率v(PCl5)=__。在该温度下,若起始时充入0.5molPCl5和amolCl2,平衡时PCl5的转化率仍为20%,则a=__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学研究性学习小组为了制取焦亚硫酸钠(![]() ),并对其性质进行研究。特进行如下实验:
),并对其性质进行研究。特进行如下实验:
实验一 制取焦亚硫酸钠。
研究小组采用下图装置(实验前已除尽装置内的空气)制取![]() 。装置Ⅱ中有
。装置Ⅱ中有![]() 晶体析出,发生的反应为:
晶体析出,发生的反应为:![]() 。
。
(1)装置Ⅰ中通常采用70%~80%的浓硫酸与亚硫酸钠固体反应制取![]() ,而不用98%的浓硫酸或极稀的稀硫酸,原因是________________________。
,而不用98%的浓硫酸或极稀的稀硫酸,原因是________________________。
(2)若要从装置Ⅱ中获得已析出的晶体,所采取的分离方法需用到的玻璃仪器有________。
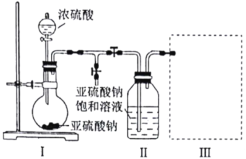
(3)装置Ⅲ用于处理尾气,请画出用来处理尾气并防止发生倒吸的实验装置,注明相应的试剂。
____________________________________________________________
(4)已知![]() 溶于水后,立即生成
溶于水后,立即生成![]() ,该反应的离子方程式为________________________。
,该反应的离子方程式为________________________。
(5)用![]() 试纸测得
试纸测得![]() 溶液呈酸性,其溶液呈酸性的原因是________________________。
溶液呈酸性,其溶液呈酸性的原因是________________________。
(6)取少量焦亚硫酸钠晶体于试管中,其中滴加酸性![]() 溶液,剧烈反应,溶液紫红色很快褪去,经测定溶液中产生
溶液,剧烈反应,溶液紫红色很快褪去,经测定溶液中产生![]() ,该反应的离子方程式是________________________。
,该反应的离子方程式是________________________。
实验三 焦亚硫酸钠的含量测定。
测定产品中焦亚硫酸钠的质量分数常用剩余碘量法。
已知:![]() ;
;![]() 。
。
①精确称取干燥的产品![]() 放入碘量瓶(带磨口塞的锥形瓶)中。
放入碘量瓶(带磨口塞的锥形瓶)中。
②向碘量瓶中准确移取![]() ,
,![]() 的标准碘溶液(过量),振荡,使其与产品中的焦亚硫酸钠充分反应。
的标准碘溶液(过量),振荡,使其与产品中的焦亚硫酸钠充分反应。
③加入![]() 淀粉溶液,用标准
淀粉溶液,用标准![]() 溶液滴定至接近终点,重复操作3次,经计算得消耗标准液平均体积为
溶液滴定至接近终点,重复操作3次,经计算得消耗标准液平均体积为![]() 。
。
(7)上述实验操作滴定终点的现象为________________________;根据上述实验,计算产品中焦亚硫酸钠的质量分数为________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A(C3H6)是基本有机化工原料,由A制备聚合物C和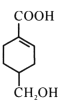 合成路线如图所示(部分条件略去)。
合成路线如图所示(部分条件略去)。
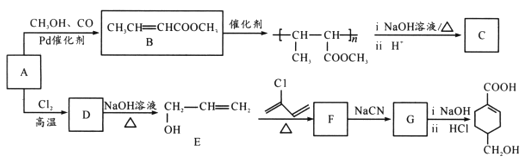
已知: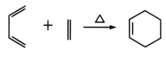
![]() RCOOH
RCOOH
(1)A的结构简式为__________
(2)写出一个题目涉及的非含氧官能团的名称__________
(3)关于C的说法正确的是_______________(填字母代号)
a 有酸性 b 分子中有一个甲基
c 是缩聚产物 d 能发生取代反应
(4) 发生缩聚形成的高聚物的结构简式为_____
发生缩聚形成的高聚物的结构简式为_____
(5)E→F的化学方程式为_______。
(6)以A为起始原料,选用必要的无机试剂合成![]() ,写出合成路线(用结构简式表示有机物),用箭头表示转化关系,箭头上注明试剂和反应条件)_______。
,写出合成路线(用结构简式表示有机物),用箭头表示转化关系,箭头上注明试剂和反应条件)_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列能与文字表述对应且正确的反应方程式是( )
A.甲烷和氯气在光照条件下反应: 2CH4+Cl2![]() 2CH3Cl +H2
2CH3Cl +H2
B.实验室用电石制乙炔:CaC2+2H2O→Ca(OH)2+![]() ↑
↑
C.用NaOH溶液中和苯酚溶液的酸性:H++OH-=H2O
D.向苯酚钠溶液中通入少量CO2:CO2+H2O+2C6H5O-→2 C6H5OH+ CO32-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25°C时,将0.1mol/LNaOH溶液加入20mL0.1mol/LCH3COOH溶液中,所加入溶液体积(V)和混合液的pH关系曲线如图所示。下列结论正确的是
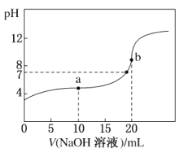
A.pH=7时,c(CH3COO-)+c(CH3COOH)=c(Na+)
B.a点所示的溶液中c(CH3COOH)>c(CH3COO-)
C.b点所示的溶液中c(CH3COOH)+c(H+)=c(OH-)
D.a、b两点所示的溶液中水的电离程度相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定条件下可实现下图所示物质之间的变化:
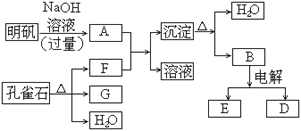
请填写以下空白:
(1)孔雀石的主要成分是CuCO3·Cu(OH)2(碱式碳酸铜),受热易分解。下图中的F是_____。
(2)写出明矾溶液与过量NaOH溶液反应的离子方程式:________。
(3)图中所得G和D都为固体,混和后在高温下可发生反应,写出该反应的化学方程式:____________。
(4)每生成1摩D,同时生成______摩E。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中不正确的是
①质子数相同的微粒一定属于同一种元素
②同位素的性质几乎相同
③质子数相同,电子数也相同的两种微粒,不可能是一种分子和一种离子
④某种元素的相对原子质量取整数,就是其质量数
⑤一种元素只能有一种质量数
⑥电子数相同的微粒不一定是同一种元素。
A.②③⑤⑥B.①②④⑤C.①②⑤⑥D.③④⑤⑥
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com