

分析 (1)第周期容纳2种元素,分别处于第1、18列,二、三周期中ⅡA、ⅢA分别处于2、13列;第一周期均为非金属性,其它周期中,元素原子电子层>最外层电子数为非金属性元素,其余为金属元素;
(2)①最高价氧化物的水化物碱性最强,在元素周期表左下方,放射性元素除外就是金属性最强的 Cs,位于第六周期IA族;
②非金属性越强对应气态氢化物最稳定的越强,在元素周期表的右上方对应的元素是氟,位于第二周期、17列;
(3)对主族元素周期数=电子层数、主族族序数=最外层电子数.
解答 解:(1)第一周期只有2种元素,分别处于第1、18列,二、三周期中ⅡA、ⅢA分别处于2、13列;第一周期均为非金属,金属与非金属的分界线除ⅠA在氢元素下侧,其他各族元素皆处于周期数=主族数的元素的上侧和右侧,用实线画出元素周期表的上边界,且用实线标出金属元素与非金属元素的分界线为: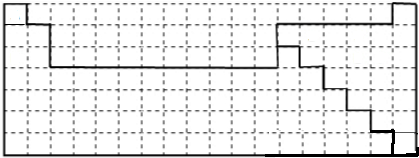 ,
,
故答案为 ;
;
(2)①最高价氧化物的水化物碱性最强,在元素周期表左下方,放射性元素除外就是金属性最强的 Cs,位于第六周期IA族;
②非金属性越强对应气态氢化物最稳定的越强,在元素周期表的右上方对应的元素是氟,位于第二周期、17列,
在周期中的位置为: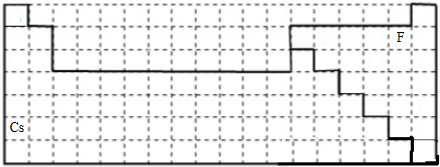 ,
,
故答案为: ;
;
(3)对主族元素,周期数=电子层数、主族族序数=最外层电子数,故答案为:周期数=电子层数;主族族序数=最外层电子数.
点评 本题考查元素周期表、元素周期律、结构与位置关系,比较基础,注意对元素周期表的整体把握.


科目:高中化学 来源: 题型:选择题
| A. | 在溶剂中提高苯的比例,能提高溶液的导电性 | |
| B. | 电解时阳极的电极反应式为2Br--2e-=Br2 | |
| C. | 电解时可用铁作阳极材料 | |
| D. | 汽油样品应加在阴极区 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 与K+距离相等且最近的O2-共有8个 | |
| B. | 与K+距离相等且最近的O2-构成的多面体是正八面体 | |
| C. | 与K+距离相等且最近的K+有8个 | |
| D. | 一个KO2晶胞中的K+和O2-粒子数均为8个 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,22.4L CCl4含有的分子数为NA | |
| B. | 常温常压下,17g NH3所含的原子数目为4NA | |
| C. | 铝与足量盐酸反应,生成2.24L H2时,转移的电子数为0.2NA | |
| D. | 0.1mol/L Na2CO3溶液中含有的Na+数目为0.2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
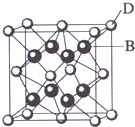 已知A、B、C、D、E都是元素周期表中前36号的元素,其原子序数依次增大.A与其他4种元素既不在同一周期又不在同一族.B和C属同一主族,D和E属同一周期,又
已知A、B、C、D、E都是元素周期表中前36号的元素,其原子序数依次增大.A与其他4种元素既不在同一周期又不在同一族.B和C属同一主族,D和E属同一周期,又查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com