
下列变化中,既有共价键和离子键断裂,又有共价键和离子键形成的是( )
A.2Na2O2+2CO2===2Na2CO3+O2
B.2Na+2H2O===2NaOH+H2↑
C.Cl2+H2OHCl+HClO
D.Na2CO3+BaCl2===BaCO3↓+2NaCl
 星级口算天天练系列答案
星级口算天天练系列答案 芒果教辅达标测试卷系列答案
芒果教辅达标测试卷系列答案科目:高中化学 来源: 题型:
下列说法正确的是( )
A、热化学方程式的计量数可以表示分子的个数
B、热化学方程式中只需标明生成物的状态
C、反应热指的是反应过程中放出或吸收的热量
D、伴随能量变化的一定是化学变化
查看答案和解析>>
科目:高中化学 来源: 题型:
实验室常用的浓盐酸密度为1.17 g·mL-1,物质的量浓度为11.7mol/L,
(1)取此浓盐酸50 mL,用蒸馏水稀释至200 mL后稀盐酸的物质的量浓度?
(2)将13 g锌投入上述实验所得稀盐酸中,充分反应,
求:放出的H2在标准状况下的体积;
(3)此浓盐酸中HCl的质量分数?
查看答案和解析>>
科目:高中化学 来源: 题型:
2011年3月,日本地震和海啸引起的核泄漏引起了全世界范围内核恐慌,据报道碘-131和铯-137是主要的放射性核素。已知铯的原子序数是55,是第6周期ⅠA族元素,试推断下列内容:
(1)铯的原子核外共有________个电子层,最外层电子数为________。
(2)铯跟水剧烈反应,放出________气体,同时生成的溶液使紫色石蕊试液显________色,因为______________________________________________________。
(3)同位素137Cs原子核里有________个中子。
(4)原子序数为54的元素位于元素周期表中第________周期________族,从原子结构来看它的原子核外有________个电子层,最外层电子数为________个。
查看答案和解析>>
科目:高中化学 来源: 题型:
某元素的原子最外层只有一个电子,它跟氯元素结合时( )
A.一定形成共价键
B.一定形成离子键
C.可能形成共价键,也可能形成离子键
D.以上说法都不对
查看答案和解析>>
科目:高中化学 来源: 题型:
下列10种物质:①水 ②空气 ③铁 ④二氧化碳
⑤硫酸 ⑥熟石灰[Ca(OH)2] ⑦胆矾(CuSO4·5H2O) ⑧NaOH溶液 ⑨碱式碳酸铜[Cu2(OH)2CO3] ⑩硫酸氢钠(NaHSO4)
(1)属于混合物的是________。
(2)属于氧化物的是________。
(3)属于碱的是______。
(4)属于酸的是______。
(5)属于盐的是________。(以上空格填物质的序号)
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各项叙述中,错误的是( )
A.普通水泥的主要成分是硅酸三钙、硅酸二钙和铝酸三钙等
B.水泥是一种混合物
C.混凝土常以钢筋做骨架,而不用其他金属,是因为钢筋的硬度大且其热膨胀系数和混凝土相差不大
D.水泥具有水硬性,故不适合水下施工
查看答案和解析>>
科目:高中化学 来源: 题型:
N2和H2合成NH3的能量变化如图所示,该反应的热化学方程式是
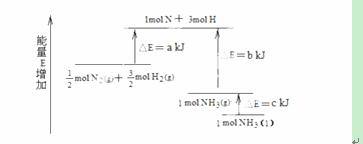
A.N2(g)+3H2(g) = 2NH3(g) ;△H = 2(b—a) kJ/mol
B.N2(g)+3H2(g) = 2NH3(l);△H = 2(a—b—c) kJ/mol
C. N2(g)+
N2(g)+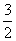 H2(g) = NH3(l) ;△H = (b+c—a) kJ/mol
H2(g) = NH3(l) ;△H = (b+c—a) kJ/mol
D. N2(g)+
N2(g)+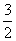 H2(g) =NH3(g) ;△H = (a+b) kJ/mol
H2(g) =NH3(g) ;△H = (a+b) kJ/mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com