
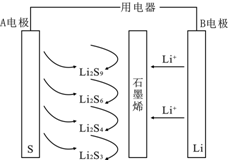
 石墨烯锂硫电池放电时的工作原理示意图如图,电池反应为2Li+nS=Li2Sn,有关该电池说法正确的是( )
石墨烯锂硫电池放电时的工作原理示意图如图,电池反应为2Li+nS=Li2Sn,有关该电池说法正确的是( )| A. | 放电时,Li+向负极迁移 | |
| B. | A电极上发生的一个电极反应为:2Li++6S+2e-=Li2S6 | |
| C. | 若对该电池充电,B电极接电源正极 | |
| D. | B电极发生还原反应 |
分析 在原电池中,电解质里的阳离子移向正极,所以A是正极,发生还原反应:2Li++nS+2e-═Li2Sn,电子从原电池的负极流向正极,根据电极反应式结合电子转移进行计算即可.
解答 解:A.在原电池中,电解质里的阳离子移向正极,则Li+向正极迁移,故A错误;
B.A是正极,发生得电子的还原反应:2Li++Sn+2e-═Li2Sn,故B正确;
C.若对该电池充电,正极与外加电源的正极相连,即A电极接电源正极,故C错误;
D.A是正极,发生还原反应,B是负极,发生氧化反应,故D错误.
故选B.
点评 本题考查新型电池,题目难度中等,注意把握原电池的工作原理以及电极反应式的书写,解答本题的关键是根据离子的流向判断原电池的正负极.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙烯分子中2个碳原子都是sp2杂化 | B. | 乙烯分子存在非极性键 | ||
| C. | 乙烯分子中4个H原子在同一平面上 | D. | 乙烯分子有6个σ键 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 、
、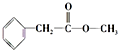 ;
;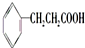 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
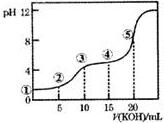 常温下,用0.10mol•L-1的KOH标准溶液滴定10.00mL0.10mol•L-1的H2C2O4(二元弱酸)溶液所得滴定曲线如图所示.下列说法正确的是( )
常温下,用0.10mol•L-1的KOH标准溶液滴定10.00mL0.10mol•L-1的H2C2O4(二元弱酸)溶液所得滴定曲线如图所示.下列说法正确的是( )| A. | 点①所示溶液中:c(H+)/c(OH-)=1012 | |
| B. | 点③所示溶液中:c(K+)>c(HC2O4-)>c(H2C2O4)>c(C2O42-) | |
| C. | 点④所示溶液中:c(K+)+c(H2C2O4)+c(HC2O4-)+c(C2O42-)=0.1mol•L-1 | |
| D. | 点⑤所示溶液中:c(OH-)=c(H+)+c(HC2O4-)+c(H2C2O4) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
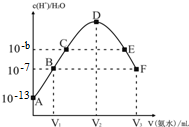
| A. | E溶液中存在:c(NH4+)>c(SO42-)>c(OH-)>c(H+) | |
| B. | 稀硫酸的浓度为0.1mol/L | |
| C. | C点溶液pH=14-b | |
| D. | V2=20 mL |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 化学键 | O=O | C=O | H=O | C=H |
| E/(kJ mol-1) | 496 | 799 | 460 | ? |
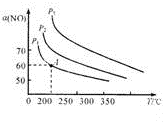 | 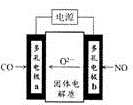 | 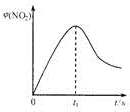 |
| 图1 | 图2 | 图3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com