
| A、容器里气体的密度为40 g/L |
| B、SO3的分解率为20% |
| C、在这10 min内的平均速率为υ(O2)=0.005 mol?L-1?min-1 |
| D、化学反应速率:υ(Ag2SO4)=υ(SO3) |
| 0.4mol/L×1L×80g/mol+0.1mol/L×1L×64g/mol+0.05mol/L×1L×32g/mol |
| 1L |
| 0.1mol/L |
| 0.5mol/L |
| 0.05mol/L |
| 10min |


 习题精选系列答案
习题精选系列答案科目:高中化学 来源: 题型:
A、硝基苯的结构简式: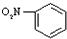 |
| B、葡萄糖的实验式(最简式)为:C6H12O6 |
C、乙酸的分子比例模型图为: |
D、CH3Cl的电子式: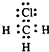 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.1mol、0.2mol、0.1mol |
| B、0.2mol、0.3mol、0.2mol |
| C、0.1mol、0.5mol、0.2mol |
| D、0.1mol、0.3mol、0.1mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、反应放出的热量为0.04a KJ |
| B、平衡时H2O的转化率为40% |
| C、若将容器的体积压缩为1L,有利于该反应平衡正向移动 |
| D、判断该反应达到平衡的依据是CO、H2O、CO2、H2的浓度都相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 反应时间/min | n(CO)/mol | H2O/mol |
| 0 | 1.20 | 0.60 |
| t1 | 0.80 | |
| t2 | 0.20 |
A、反应在t1 min内的平均速率为v(H2)=
| ||
| B、保持其他条件不变,起始时间容器中充入0.60molCO和1.20molH2O,到达平衡时,n(CO2)=0.40mol | ||
| C、保持其他条件不变,向平衡体系中再通入0.20molH2O,与原平衡相比,达到新平衡时CO转化率增大,H2O的体积分数增大 | ||
| D、温度升至800℃时,若上述反应平衡常数为0.64,则正反应为吸热反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
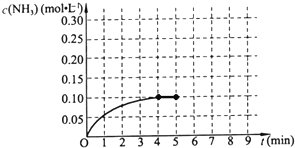 在一容积为2L的密闭容器中,加入0.2mol的N2和0.6mol的H2,在一定条件下发生如下反应:
在一容积为2L的密闭容器中,加入0.2mol的N2和0.6mol的H2,在一定条件下发生如下反应:查看答案和解析>>
科目:高中化学 来源: 题型:
| A、在AgCl的沉淀溶解平衡体系中,加入蒸馏水,Ksp(AgCl)增大 |
| B、可直接根据Ksp的数值大小比较难溶物在水中的溶解度大小 |
| C、在CaCO3的沉淀溶解平衡体系中,加入稀盐酸,平衡不移动 |
| D、25℃时,Ksp(AgCl)>Ksp(AgI),向AgCl的悬浊液中加入KI溶液,有黄色沉淀生成 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com