
| A、Mg2++2HCO3-+2OH-→MgCO3↓+CO32-+2H2O |
| B、Mg2++2HCO3-+2OH-→MgCO3↓+2H2O |
| C、Mg2++2HCO3-+4OH-→Mg(OH)2+2CO32-+2H2O |
| D、HCO3-+OH-→CO32-+2H2O |


 一线名师口算应用题天天练一本全系列答案
一线名师口算应用题天天练一本全系列答案 小学学习好帮手系列答案
小学学习好帮手系列答案科目:高中化学 来源: 题型:
2- 4 |
| 溶解 |
| ① |
| BaCl2 |
| ② |
| NaOH |
| ③ |
| Na2CO3 |
| ④ |
| 过滤 |
| ⑤ |
| 适量盐酸 |
| ⑥ |
| 蒸发、结晶、烘干 |
| ⑦ |
查看答案和解析>>
科目:高中化学 来源: 题型:
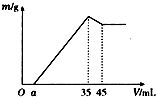 准确称取6g铝土矿样品(含Al2O3、Fe2O3、SiO2),放入100mL某浓度的HCl溶液中(SiO2不溶于HCl溶液),充分反应后过滤,向滤液中加入10mol/L的NaOH溶液,产生沉淀的质量m与加入NaOH溶液的体积的关系如图所示,求:
准确称取6g铝土矿样品(含Al2O3、Fe2O3、SiO2),放入100mL某浓度的HCl溶液中(SiO2不溶于HCl溶液),充分反应后过滤,向滤液中加入10mol/L的NaOH溶液,产生沉淀的质量m与加入NaOH溶液的体积的关系如图所示,求:查看答案和解析>>
科目:高中化学 来源: 题型:
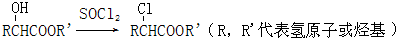
查看答案和解析>>
科目:高中化学 来源: 题型:
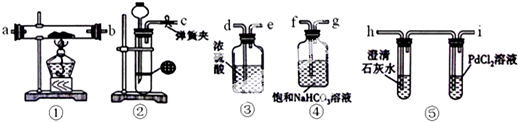
查看答案和解析>>
科目:高中化学 来源: 题型:
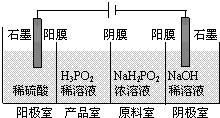
查看答案和解析>>
科目:高中化学 来源: 题型:
 对叔丁基苯酚
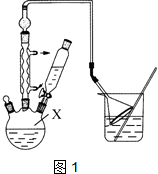
对叔丁基苯酚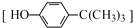 可用于生产油溶性酚醛树脂等.实验室以苯酚、叔丁基氯[(CH3)3CCl]等为原料制备对叔丁基苯酚的实验步骤如下:
可用于生产油溶性酚醛树脂等.实验室以苯酚、叔丁基氯[(CH3)3CCl]等为原料制备对叔丁基苯酚的实验步骤如下: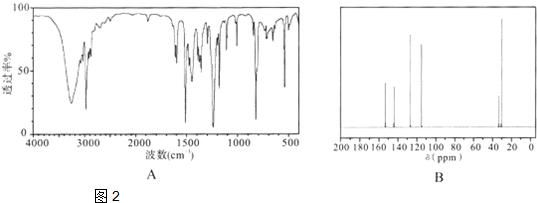
查看答案和解析>>
科目:高中化学 来源: 题型:
40 19 |
40 20 |
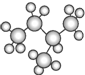 )和新戊烷(
)和新戊烷(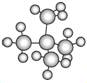 )
) 和
和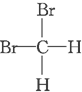
查看答案和解析>>
科目:高中化学 来源: 题型:
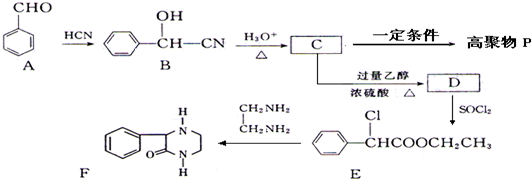
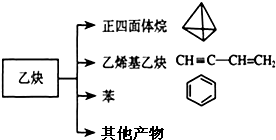 乙炔是一种重要的有机化工原料,以乙炔为原料在不同的反应条件下可以转化成以下化合物.完成下列各题:
乙炔是一种重要的有机化工原料,以乙炔为原料在不同的反应条件下可以转化成以下化合物.完成下列各题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com