
已知299 K时,合成氨反应 N2 (g ) + 3H2 ( g )=2NH3 ( g ) △H = -92.0 kJ/mol,将此温度下的1 mol N2 和3 mol H2 放在一密闭容器中,在催化剂存在时进行反应,达到平衡时,反应放出的热量为(忽略能量损失)( )
A.一定大于92.0 kJ B.一定等于92.0 kJ
C.不能确定 D. 一定小于92.0 kJ
 期末好成绩系列答案
期末好成绩系列答案 99加1领先期末特训卷系列答案
99加1领先期末特训卷系列答案 百强名校期末冲刺100分系列答案
百强名校期末冲刺100分系列答案 好成绩1加1期末冲刺100分系列答案
好成绩1加1期末冲刺100分系列答案科目:高中化学 来源: 题型:
某同学模拟工业“折点加氯法”处理氨氮废水的原理,进行如下研究。
| 装置(气密性良好,试剂已添加) | 操作 | 现象 |
|
| 打开分液漏斗活塞,逐滴加入浓氨水 | ⅰ.C中气体颜色变浅 ⅱ.稍后,C中出现白烟并逐渐增多 |
(1)浓氨水分解可以制氨气,写出A中反应的化学方程式是 。从平衡移动 的角度分析NaOH固体在氨水分解中的作用 。
(2)现象ⅰ,C中发生的反应为:2NH3(g)+3Cl2(g)= N2(g)+6HCl(g) H= —456 kJ·mol-1
已知:
①NH3的电子式是 。
②断开1mol H-N键与断开1molH-Cl键所需能量相差约为 ,
(3)现象ⅱ中产生白烟的化学方程式是 。
(4)为避免生成白烟,该学生设计了下图装置以完成Cl2和NH3的反应。
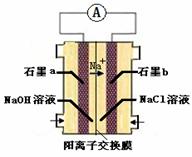
若该装置能实现设计目标,则①石墨b电极上发生的是 反应(填“氧化”或“还原”)
②写出石墨a电极的电极反应式: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
美国海军航空站安装了MCFC型燃料电池,该电池可同时供应电和水蒸气,其工作温度为600 ℃~700 ℃,所用燃料为H2,电解质为熔融的K2CO3,已知该电池的总反应为2H2+O2===2H2O, 负极反应为H2+ CO32--2e- ===H2O+CO2,则下列推断正确的是
A.正极反应为:4OH- ====O2+2H2O+4e- B.放电时CO32- 向负极移动
C.电池供应1 mol水蒸气,转移的电子数为4 mol D.放电时CO32- 向正极移动
查看答案和解析>>
科目:高中化学 来源: 题型:
Ⅰ.设计出燃料电池使汽油氧化直接产生电流是本世纪最富有挑战性的课题之一。最近有人制造了一种燃料电池,一个电极通入空气,另一个电极通入汽油蒸气,电池的电解质是掺杂了Y2O3的ZrO2晶体,它在高温下能传导O2-,回答如下问题:
(1)以戊烷(C5H12)为汽油代表,这个电池正极发生的电极反应方程式是O2 + 4e- = 2O2-,负极发生的反应方程式是: ;固体电解质里O2-向 极移动;
(2)人们追求燃料电池氧化汽油而不在内燃机里燃烧汽油产生动力的主要原因是 ;
Ⅱ.为确定某铝热剂(氧化铁粉末和铝粉)的组成,分别进行下列实验。若取10.7 g样品,向其中加入足量的NaOH溶液,测得生成的气体(标准状况)体积为3.36 L ,反应的化学方程式为 ,样品中铝的质量是 g。若取10.7 g样品将其点燃,恰好完全反应,待反应产物冷却后,加入足量盐酸,测得生成的气体体积为VL,V等于 。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知热化学方程式:2SO2(g)+O2(g)2SO3(g) ΔH=-Q kJ·mol-1(Q>0)。下列说法正确的是 ( )。
A.相同条件下,2 mol SO2(g)和1 mol O2(g)所具有的能量小于2 mol SO3(g)
所具有的能量
B.将2 mol SO2(g)和1 mol O2(g)置于一密闭容器中充分反应后,放出热量为
Q kJ
C.增大压强或升高温度,该反应过程放出更多的热量
D.如将一定量SO2(g)和O2(g)置于某密闭容器中充分反应后放热Q kJ,则此过程中有2 mol SO2(g)被氧化
查看答案和解析>>
科目:高中化学 来源: 题型:
对于可逆反应2SO2(g)+O2(g)  2SO3(g)(正反应为放热反应),下列有关说法正确的是( )
2SO3(g)(正反应为放热反应),下列有关说法正确的是( )
A.升高温度正反应加快,逆反应不变 B.升高温度正逆反应都加快
C.升高温度逆反应加快,正反应不变 D.升高温度逆反应加快,正反应减慢
查看答案和解析>>
科目:高中化学 来源: 题型:
已知:(1)Fe2O3(s) + C(s)===
C(s)=== CO2(g)+2Fe(s) ΔH1=+234.1 kJ·mol-1
CO2(g)+2Fe(s) ΔH1=+234.1 kJ·mol-1
(2)C(s)+O2(g)===CO2(g) ΔH2=-393.5 kJ·mol-1
则2Fe(s)+ O2(g)===Fe2O3(s) 的ΔH是( )
O2(g)===Fe2O3(s) 的ΔH是( )
A.-824.4 kJ·mol-1 B.-627.6 kJ·mol-1
C.-744.7 kJ·mol-1 D.-169.4 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
对于可逆反应:2SO2+O2 2SO3,下列措施能使反应物中活化分子百分数、化学反应速率和化学平衡常数都变化的是( )
2SO3,下列措施能使反应物中活化分子百分数、化学反应速率和化学平衡常数都变化的是( )
A.增大压强 B.升高温度 C.使用催化剂 D.多充O2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com