
研究NO2、SO2、CO等大气污染气体的处理具有重要意义。
(1)一定条件下,将NO2与SO2以体积比1∶2置于密闭容器中发生反应NO2+SO2SO3+NO,平衡时NO2与SO2体积比为1∶6,则平衡常数K= ;多余的NO与空气(设空气中氧气和氮气体积比为1∶4)按一定比例通入水中即可完全吸收,VNO∶V空气= 。NO可以与活性炭发生如下反应C(s)+2NO(g)N2(g)+CO2(g),若温度恒定,提供足量的活性炭,增大NO的浓度,NO的转化

率 (选填“增大”、“减小”、“不变”或“无法确定”)。
(2)CO可以组成燃料电池,用以提供电能,根据右图所示写出正极反应式:
。
 文敬图书课时先锋系列答案
文敬图书课时先锋系列答案科目:高中化学 来源: 题型:
硫化碱法是工业上制备Na2S2O3的方法之一,反应原理为:
2Na2S+Na2CO3+4SO2==3Na2S2O3+CO2 (该反应△H>0)
某研究小组在实验室用硫化碱法制备Na2S2O3·5H2O流程如下。

(1)吸硫装置如图所示。

①装置B的作用是检验装置A中SO2的吸收效率,B中试剂是 ,表明SO2吸收效率低的实验现象是B中溶液 。
②为了使SO2尽可能吸收完全,在不改变A中溶液浓度、体积的条件下,除了及时搅拌反应物外,还可采取的合理措施是 、 。(写出两条)
(2)假设本实验所用的Na2CO3含少量NaCl、NaOH,设计实验方案进行检验。(室温时CaCO3饱和溶液的pH=10.2)
限选试剂及仪器:稀硝酸、AgNO3溶液、CaCl2溶液、Ca(NO3)2溶液、酚酞溶液、蒸馏水、pH计、烧杯、试管、滴管
| 序号 | 实验操作 | 预期现象 | 结论 |
| ① | 取少量样品于试管中,加入适量蒸馏水,充分振荡溶解,___________________。 | _______________ | 样品含NaCl |
| ② | 另取少量样品于烧杯中,加入适量蒸馏水,充分搅拌溶解,___________________。 | _______________ | 样品含NaOH |
(3)Na2S2O3溶液是定量实验中的常用试剂,测定其浓度的过程如下:准确称取a g KIO3(化学式量:214)固体配成溶液,加入过量KI固体和H2SO4溶液,滴加指示剂,用Na2S2O3溶液滴定至终点,消耗Na2S2O3溶液的体积为V mL。则c(Na2S2O3)=_________mol·L-1。(只列出算式,不作运算)
已知:Cr2O72-+6I-+14H+=== 2Cr3++3I2+7H2O 2S2O32-+I2===S4O62-+2I-
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)已知氢气的燃烧热为285.8 kJ/mol,则H2(g)+1/2O2(g)===H2O(l) ΔH= ;
(2)用离子方程式来表示强酸和强碱的中和热(焓变的数值为57.3):
H+(aq)+ === ,ΔH= 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列图示与对应的叙述相符的是
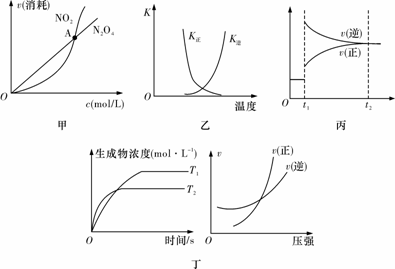
A.图甲表示在恒容密闭容器中,恒温条件下发生的可逆反应2NO2(g)N2O4(g),各物质的浓度与其消耗速率之间的关系,其中交点A对应的状态为化学平衡状态
B.图乙曲线表示反应2A(g)+B(g)2C(g) ΔH>0,正、逆反应的平衡常数K随温度的变化
C.图丙表示对反应2X(g)+Y(g)Z(s)+3W(g) ΔH<0在t1时刻增大压强
D.图丁表示反应aA(g)+bB(g)cC(g)+dD(g):a+b>c+d;T1<T2;ΔH<0
查看答案和解析>>
科目:高中化学 来源: 题型:
用NA表示阿伏加德罗常数的值。下列叙述中正确的是
A. 11.2L NO和11.2L O2混合后的分子总数为NA
B. 1mol苯乙烯中含有的碳碳双键数为4NA
C. 50mL 18.4mol/L浓硫酸与足量铜微热反应,生成SO2分子数目为0.46NA
D. 1mol Fe与足量的稀HNO3反应并放出NO和N2O,转移3 NA个电子
查看答案和解析>>
科目:高中化学 来源: 题型:
“低碳循环”引起各国的高度重视,而如何降低大气中CO2的含量及有效地开发利用CO2,引起了全世界的普遍重视。所以“低碳经济”正成为科学家研究的主要课题:
(1)将不同量的CO(g)和H2O(g)分别通入到体积为2L的恒容密闭容器中,进行反应
CO(g)+H2O(g)  CO2(g)+H2(g),得到如下二组数据:
CO2(g)+H2(g),得到如下二组数据:
实验组 | 温度℃ | 起始量/mol | 平衡量/mol | 达到平衡所需时间/min | ||
CO | H2O | H2 | CO | |||
1 | 650 | 4 | 2 | 1.6 | 2.4 | 6 |
2 | 900 | 2 | 1 | 0.4 | 1.6 | 3 |
①实验1中以v (CO2) 表示的反应速率为 (保留两位小数,下同)。
②该反应为 (填“吸”或“放”)热反应,实验2条件下平衡常数K= 。
(2)已知在常温常压下:
① 2CH3OH(l) + 3O2(g) = 2CO2(g) + 4H2O(g) ΔH = -1275.6 kJ/mol
② 2CO (g)+ O2(g) = 2CO2(g) ΔH = -566.0 kJ/mol
③ H2O(g) = H2O(l) ΔH = -44.0 kJ/mol
写出甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式:______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组离子中,能大量共存,溶液呈现无色,且加入过氧化钠粉末后仍然能大量共存的是
A.K+、MnO4—、SO42—、H+ B.Ba2+、Na+、HCO3—、NO3—
C.Na+、NO3—、K+、Cl— D.Ca2+、NO3—、Cl—、CO32—
查看答案和解析>>
科目:高中化学 来源: 题型:
利用化合价和物质类别推测物质的性质是化学研究的重要手段。
(1)从化合价的角度可以预测物质的性质。
①将 通入酸性
通入酸性 溶液中,溶液由紫色褪至无色。反应结束后,硫元素存在形式合理的是__________A.
溶液中,溶液由紫色褪至无色。反应结束后,硫元素存在形式合理的是__________A.  B.
B.  C.
C.  D.
D. 
②亚硫酸钠中有+4价的硫,它既有氧化性又有还原性,现有试剂:溴水、H2S、稀硫酸。
请选取一种合适的试剂证明Na2SO3具有还原性, 并写出该反应的化学方程式__________________________________
(2)从物质分类的角度可以推测物质的性质。
①已知蛇纹石由 、
、 、
、 、
、 组成。其中属于碱性氧化物的是_________。
组成。其中属于碱性氧化物的是_________。
②现取一份蛇纹石试样进行实验:
I. 先将其溶于过量的盐酸中、过滤,滤渣的主要成分是_________。
II. 再向滤液中加入 溶液至过量、过滤,滤渣中的主要成分是_________。
溶液至过量、过滤,滤渣中的主要成分是_________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com